ツユクサのフラボノイド3’,5’−水酸化酵素遺伝子
【課題】青い花色の作出には、青色色素(デルフィニジン)の合成酵素の一つであるフラボノイド3’,5’−水酸化酵素(F3'5'H)が大きな役割を果たすことが知られており、その酵素をより高発現するF3'5'H遺伝子が求められている。
本発明の課題は、青色コチョウランの作出を可能にする高発現型F3'5'H遺伝子を見出し、青色系の花色を呈するコチョウランを提供することにある。
【解決手段】本発明者は、上記課題を解決するために鋭意検討した結果、ツユクサ由来のF3’5’H遺伝子が既知遺伝子を上回る効果を示すことを見出し、さらに当該遺伝子をコチョウランに導入することにより青系の花色に改変できることを見出し、本発明を完成するに至った。
本発明の課題は、青色コチョウランの作出を可能にする高発現型F3'5'H遺伝子を見出し、青色系の花色を呈するコチョウランを提供することにある。
【解決手段】本発明者は、上記課題を解決するために鋭意検討した結果、ツユクサ由来のF3’5’H遺伝子が既知遺伝子を上回る効果を示すことを見出し、さらに当該遺伝子をコチョウランに導入することにより青系の花色に改変できることを見出し、本発明を完成するに至った。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、遺伝子組換え技術を用いて青い花色を呈する植物を製造する方法に関する。詳しくは、ツユクサの色素合成酵素の一つであるフラボノイド3’,5’―水酸化酵素(F3’5’H)をコードする遺伝子を用いて青い花色を呈するラン科植物を製造する方法に関する。
【背景技術】
【0002】
鑑賞用植物において花の色は特に重要な形質として、古くから様々な色の花が交配育種により作出されてきた。しかし、交配育種の場合、遺伝子資源が交配可能な種内に限定されるため改変可能な色調には限界があった。また、花の色のような特定の形質のみをある特定の品種に導入するためには戻し交雑を何世代も繰り返す必要があり、多大な労力と時間が必要である。さらに、植物によって交配育種の期間は異なり、花が咲くまでに数年から数十年かかる植物もある。特に、コチョウランやシンビジウムのようなラン科植物の多くは、花をつけるまでに長い時間を要し、育種に時間がかかる植物である。そのため、市場の要望にも拘らずコチョウランやシンビジウムにはいまだ新しい花色、特に青い花色の優良品種は存在しない。
【0003】
近年、組換えDNA技術により種や属を越えた育種が可能となり、従来の交配育種では得られなかった色調を持つ新品種の育成に期待が持たれている。
【0004】
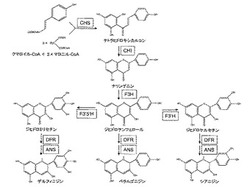
花の色は主にアントシアニン、カロテノイド、ベタレインの3種の色素に起因する。その内で青色を司るのは極大吸収波長幅が最も広いアントシアニン(オレンジ色から青色)である。アントシアニンはフラボノイドの一種で図1に示した代謝経路で生合成される。アントシアニンの色調は、その化学構造に大きく依存し、B環の水酸基の数が多いほど青くなる。B環の水酸化は、フラボノイド3’−水酸化酵素(F3’H)およびフラボノイド3’,5’−水酸化酵素(F3’5’H)によって触媒される。花弁細胞内にて、F3’H活性とF3’5’H活性がない場合にはペラルゴニジン(橙色から赤色)が合成され、F3’H活性がある場合はシアニジン(赤から紅色)が合成され、F3’5’H活性がある場合はデルフィニジン(青色)が合成される。そのため、青い花色の作出には、F3'5'Hが大きな役割を果たすと考えられている。
【0005】
このような観点から、F3'5'Hに着目した遺伝子組換えにより青い花色を呈する植物を作出する研究が進められている。
【0006】
既知のF3’5’Hをコードする遺伝子としては、フウリンソウ、ニチニチソウ、ペチュニア、トルコギキョウ、ニーレンベルギア、バーベナ、リンドウ 、ワタ 、Lycianthes rantonnei 、ジャガイモ 、トレニア等の植物由来のものが知られているが、ツユクサから分離された遺伝子の報告は無い。
公知遺伝子を用いて花色を改変した事例としては、カーネーションDFR欠損品種へペチニュア由来のF3'5'H遺伝子及びDFR遺伝子を導入し青い色のカーネーションを製造する方法(特許文献1)や、内在代謝系を抑制したバラにパンジー由来のF3'5'H遺伝子を導入し青い色のバラを製造する方法(特許文献2)がある。
【0007】
一方、コチョウランに関しては、内在遺伝子の過剰発現による花色改変の報告があるが、青色のコチョウランを作出するには至っていない(非特許文献1)。また、シンビジウムに関しても青色の品種を作出した報告はない。
【先行技術文献】
【特許文献】
【0008】
【特許文献1】国際公開公報 WO 1996/036716
【特許文献2】国際公開公報 WO 2005/017147
【非特許文献】
【0009】
【非特許文献1】Su and Hsu, Biotechnology Letters (2003) 25: 1933-1939.
【発明の概要】
【発明が解決しようとする課題】
【0010】
青い花色の作出には、F3'5'Hが大きな役割を果たすことが知られており、より高発現するF3'5'H遺伝子が求められている。
本発明の第一の課題は、青色コチョウランの作出を可能にする高発現型F3'5'H遺伝子を見出すことにある。また、第二の課題は、その高発現型F3'5'H遺伝子を用いて青い花色を呈するラン科植物を作出することにある。
【課題を解決するための手段】
【0011】
本発明者らは、上記課題を解決するために鋭意検討した結果、ツユクサ由来のF3’5’H遺伝子が既知遺伝子を上回る効果を示すことを見出し、さらに当該遺伝子をコチョウランに導入することにより青い花色に改変できることを見出し、本発明を完成するに至った。
すなわち、本発明は、配列番号2で表されるアミノ酸配列又は同アミノ酸配列に対して少なくとも90%の相同性のアミノ酸配列を有するツユクサのフラボノイド3’,5’−水酸化酵素をコードする遺伝子に関する。
【0012】
また本発明は、上記遺伝子を含んでなるベクターに関する。
【0013】
さらに本発明は、上記遺伝子を植物に導入し、発現させることを特徴とする花色改変植物の製造方法に関する。
【0014】
また、本発明は、上記遺伝子並びにトレニア又はガーベラのジヒドロフラボノール4−還元酵素をコードする遺伝子をラン科植物に導入し、発現させることを特徴とする花色改変植物の製造方法。
【0015】
また、本発明は、上記遺伝子;トレニア又はガーベラのジヒドロフラボノール4−還元酵素をコードする遺伝子;フラバノン3−水酸化酵素をコードする遺伝子;並びにアントシアニジン合成酵素をコードする遺伝子を白い花色のラン科植物に遺伝子導入し、発現させることを特徴とする青い花色のラン科植物の製造方法に関する。
【0016】
さらには、本発明は、上記の製造方法により得られる花色改変植物、若しくは改変された花色と同じ性質を有するその子孫またはその組織に関する。
【0017】
尚、本発明において「フラボノイド3’,5’−水酸化酵素」(F3’5’H)とは、ジヒドロケンフェロールからジヒドロミリセチンを生成する反応を触媒する酵素をいう。又、「フラバノン3−水酸化酵素」(F3H)とは、ナリンゲニンからジヒドロケンフェロールを生成する反応を触媒する酵素をいい、「ジヒドロフラボノール4−還元酵素」(DFR)とは、ジヒドロミリセチンからロイコデルフィニジンを生成する反応を触媒する酵素をいい、「アントシアニジン合成酵素」(ANS)とは、ロイコデルフィニジンからデルフィニジンを生成する反応を触媒する酵素をいう。
【発明の効果】
【0018】
ツユクサのF3’5’H遺伝子を用いることにより、青色系統の多様な花色を持つ植物を作出することができる。より詳しくは、従来の交配育種法では達成できなかった青い花色のラン科植物の作出が本発明により可能となる。
本発明のその他の目的、特徴、優秀性及びその有する観点は、以下の記載より当業者にとっては明白であろう。しかしながら、以下の記載及び具体的な実施例等の記載を含めた本件明細書の記載は本発明の好ましい態様を示すものであり、説明のためにのみ示されていることを理解されたい。本明細書に開示した本発明の意図及び範囲内で、種々の変化及び/又は改変(あるいは装飾)をなすことは、以下の記載及び本明細書のその他の部分からの知識により、当業者には容易に明らかであろう。本明細書で引用されている全ての特許文献及び参考文献は、説明の目的で引用されているもので、それらは本明細書の一部としてその内容はここに含めて解釈されるべきものである。
【図面の簡単な説明】
【0019】
【図1】アントシアニンの合成経路。
【図2】花弁への遺伝子導入に用いるプラスミドベクター。P-CaMV35Sは、カリフラワーモザイクウイルス35Sプロモーターを示す。Ωは、タバコモザイクウイルスのオメガ配列を示す。Tは、カリフラワーモザイクウイルス由来の転写終結配列を示す。
【図3】植物由来の異なるANS遺伝子のPhal. amabilisの花弁への遺伝子導入。
【図4】植物由来の異なるDFR遺伝子のPhal. amabilisの花弁への遺伝子導入。
【図5】植物由来の異なるF3’5’H遺伝子のPhal. amabilisの花弁への遺伝子導入。
【図6】白色コチョウランの花色改変のために必要な遺伝子の特定。
【図7】コチョウランの形質転換を行うDNAの構築手順の概略(1)。
【図8】コチョウランの形質転換を行うDNAの構築手順の概略(2)。
【図9】白色シンビジウムの花弁への遺伝子導入。
【発明を実施するための形態】
【0020】
本発明者らは、青いラン科植物を作出すべく、青色系色素(デルフィニジン)に関与するF3’5’H遺伝子に着目し、カーネーションで実績のある既知のペチュニア由来のF3’5’H遺伝子をコチョウランに導入した。しかし、期待された効果は認められなかった。そこで、より優れた遺伝子を見いだすべく種々の植物のF3’5’H遺伝子を鋭意クローニングした。その結果、ツユクサ由来の遺伝子(配列番号:1)が非常に高い色素生合成能を示すことを見出した。本遺伝子はコチョウランの花弁細胞へ導入した場合、驚くべきことに先行技術であるペチュニア由来の遺伝子と比較して、5倍のデルフィニジンを産生した。又、本発明の遺伝子を赤色コチョウランの花弁細胞に導入したところ、花色は青味がかった紫に変化した。
更に、上記F3’5’H遺伝子に加えて、アントシアニン合成経路においてF3’5’Hよりも上流の反応を触媒するF3Hの遺伝子、並びにF3’5’Hよりも下流の反応を触媒するDFRとANSの遺伝子を白色コチョウランの花弁細胞に導入すると、花色は白色から青色となった。特に、DFR遺伝子をガーベラ若しくはトレニア由来の遺伝子を用いると、その花色は更に濃い青色を呈した。
【0021】
上述のとおり、本発明で見出されたツユクサ由来の遺伝子は既存遺伝子以上に優れた遺伝子であり、本遺伝子を用いることにより青色系コチョウランの作出が可能となる。更に、本遺伝子の優秀性は、コチョウランのみならずシンビジウムにおいても検証され、広く他の花卉植物の花色改変にも応用可能である。
【0022】
F3’5’H遺伝子は、ツユクサ(学名:Commelina communis)のゲノムDNA、またはそこから転写されるmRNAを鋳型としたcDNAから単離され、配列番号:2に記載のタンパク質をコードする配列番号:1に記載の遺伝子である。本発明にかかる遺伝子としては、F3’5’H酵素活性を持つ限りにおいて上記遺伝子と高い類似性を示す遺伝子も含まれる。高い類似性とは、配列番号:2とのアミノ酸配列の相同性が、85%以上、好ましくは90%以上、より好ましくは95%以上、さらに好ましくは98%以上のものが挙げられる。
【0023】
フラバノン3−水酸化酵素(F3H)遺伝子,ジヒドロフラボノール4−還元酵素(DFR)遺伝子及びアントシアニジン合成酵素(ANS)遺伝子は、新規若しくは公知の遺伝子を用いることができる。具体的には、F3H遺伝子としては、GenBankに登録のあるもの(アクセッション番号:DQ394303, AY221246, AJ493133, AY641730, AF184270, AB078956, AB201760, AY669324, AF036093, AB211958, AB187027, AB234905)などが挙げられ、DFR遺伝子としては、GenBankに登録のあるもの(アクセッション番号:AAB62873, AAC17843, AAD49343, AAQ83576, AAU93766, AAY32600, AAY32601, AAY32602, BAB40789, BAE79202)などが挙げられ、ANS遺伝子としては、GenBankに登録のあるもの(アクセッション番号:AY585677, AY228485, AF015885, AY581048, U82432, AY695817, AB208689, AY997840, AY382828, AY256380, AF026058, Y07955, AF384050, AB097216, AB087206, AB198869, AB044091, AY123768, AB234906)などが挙げられる。特に、DFR遺伝子としては、アクセッション番号:Z17221で示されるガーベラ由来の遺伝子、及びアクセッション番号:AB012924で示されるトレニア由来の遺伝子が望ましい。又、本発明によって見出されたコチョウラン由来のF3H遺伝子(配列番号:50)、DFR遺伝子(配列番号:64)及びANS遺伝子(配列番号:74)等の新規遺伝子も用いることができる。
【0024】
また、本発明はこれらの遺伝子を含む組換えベクター、特に発現ベクターに関する。
発現ベクターは該遺伝子を導入すべき宿主の種類に依存して発現制御領域、例えばプロモーターおよびターミネーター、複製起点等を含有する。プロモーターとしては、花弁細胞で遺伝子の発現を誘導するものが挙げられ、例えば、コチョウランのCHS遺伝子由来のプロモーター、カリフラワーモザイクウイルス(CaMV)35S由来のプロモーターなどが挙げられる。又、ターミネーターとしては、例えば、コチョウランのCHS遺伝子由来のターミネーター、カリフラワーモザイクウイルス(CaMV)35S由来のターミネーターなどが挙げられる。
具体的には、ツユクサのF3’5’H遺伝子は、プロモーター配列の3’下流に連結され、F3’5’H遺伝子の3’下流には、転写終結配列が付加されていることが望ましい。
F3H遺伝子、DFR遺伝子及び/又はANSの遺伝子もF3’5’H遺伝子と同様にプロモーター配列の3’下流に連結されて植物に導入することができる。
発現ベクターの作製は制限酵素、リガーゼ等を用いて常法に従って行うことができる。また、発現ベクターによる宿主の形質転換も常法に従って行うことができる。
本発明における花弁細胞で遺伝子を発現させる方法としては、例えば、遺伝子銃法、アグロバクテリウム法、エレクトロポレーション法、PEG法、ウイルス法などが挙げられる。
アグロバクテリウム法を用いてF3’5’H遺伝子で形質転換を行うためのベクターの一例を、図7(pBIH-35S-CcF3'5'H)に示す。更に、F3H、DFR、ANSの遺伝子も、各々独立若しくは一緒にツユクサのF3’5’H遺伝子と同じベクター上に構築することができる(図7、8)。
【0025】
本発明において形質転換可能な植物は、花卉植物であり、好ましくはラン科植物である。ラン科植物としては、コチョウラン、シンビジウム、デンドロビウム、デンドロキルム、オンシジウム、オドントグロッサム、ミルトニア、カトレヤ等が挙げられる。その中でも、コチョウラン及びシンビジウムが好ましい。シンビジウムとはCymbidium属に属する植物をいい、また、コチョウランには、Phalaenopsis属とDoritaenopsis属に属するものをいう。
【実施例】
【0026】
以下に実施例を掲げ、本発明を具体的に説明するが、この実施例は単に本発明の説明のため、その具体的な態様の参考のために提供されているものである。これらの例示は本発明の特定の具体的な態様を説明するためのものであるが、本願で開示する発明の範囲を限定したり、あるいは制限することを表すものではない。本発明では、本明細書の思想に基づく様々な実施形態が可能であることは理解されるべきである。
なお、DNA の切断、連結、大腸菌の形質転換、遺伝子の塩基配列決定、PCR等一般の遺伝子組換えに必要な方法は、各操作に使用する市販の試薬、機械装置等に添付されている説明書や、実験書(例えば「Molecular Cloning: A Laboratory Manual
(Third Edition,Sambrook and Russell,2001,Cold Spring Harbor Laboratory Press) 」)に基本的に従った。PCR反応には、GeneAmp PCR system 9700(PE Applied Biosystems)を使用した。機器の操作は、他に詳細に記載するもの以外は、機器に添付される説明書に記載される標準的な操作方法に従った。全ての実施例は、他に詳細に記載するもの以外は、標準的な技術を用いて実施したもの、又は実施することのできるものであり、これは当業者にとり周知で慣用的なものである。
本発明において新規に取得した遺伝子でコードされるアミノ酸配列と既知のアミノ酸配列との類似性を調べる相同性検索プログラムとしては、BLASTP 2.2.15(http://www.ddbj.nig.ac.jp/search/blast-j.html 文献は、Altschul et al., Nucleic Acids Res. (1997) 25: 3389-3402.)を使用した。ここで言う相同性とは、配列全体に渡るアミノ酸の一致性であり、新規に取得した遺伝子にコードされるアミノ酸配列と既知のアミノ酸配列とを一致性が高い形で並べ、両者で一致したアミノ酸数を比較域のアミノ酸数で割って得た値である。なお、ここで言う一致性が高い形とは、上記BLASTPプログラムのパラメーターをデフォルトにした状態(ギャップ有、期待値10、フィルター有)で出力されたアライメント結果である。本実施例で記載した相同性は、解析時に上記相同性検索解析において最も高い相同性を示した既知アミノ酸配列について記載したものである。
実施例1 コチョウラン花弁への遺伝子導入
本明細書の実施例に特に記述が無い場合は、以下に述べる遺伝子導入方法を用いて、コチョウラン花弁に各種遺伝子を導入し、その機能を評価した。全ての遺伝子は、5’側にプロモーターを、3’側にターミネーターを連結したDNA構造をとり、花弁細胞内で発現する形状で導入された。
コチョウランのつぼみを、1%次亜塩素酸ナトリウム水溶液で5分間滅菌し、滅菌水で3回洗浄した後、このつぼみを分解して、ラテラルセパル、ドーサルセパル、ペタルをNDM塩(Tokuhara and Mii, Plant Cell Reports (1993) 13: 7-11.)と0.6%アガロースを含む寒天培地上に置床した。尚、つぼみは、Phal. amabilisの場合は長さ15mm程度のもの、Dtps. Queen Beer 'Mantenkou'の場合は長さ8mm程度のものを用いた。
導入するDNAはHi Speed Plasmid Midi Kit(QIAGEN)を用いて精製し、該遺伝子は遺伝子銃法にて遺伝子導入を行なった。尚、複数の遺伝子を同時導入する際は、該DNA溶液同士を均等に混ぜたものを用意し、導入用のDNA溶液とした。
その際の金粒子とDNAの吸着は、以下の割合で行った。20μlのTE bufferに溶解したDNA(遺伝子が含まれるプラスミドDNA一種につき2μgを混ぜて溶解したもの)を50μlの金粒子混濁液(粒子直径は1.0μm、60mg/mlの50%グリセロール)と混ぜ、この混合液70μlに50μlの 2.5M塩化カルシウムと10μlの0.2Mスペルミジンを加えて懸濁し、DNAを金粒子に吸着させた。次に、遠心操作により、上清を除去し、70%エタノールと100%エタノールで粒子を洗浄した後、得られた該沈殿物に60μlの100%エタノールを加えた懸濁液を試料溶液とし、その10μlを一回の遺伝子導入に用いた。遺伝子銃は、IDERA GIE-III(TANAKA Co. Ltd.)を用いた。遺伝子導入条件は、銃口から試料までの距離12cm、−80kPaの減圧下、0.3MPaのヘリウムガス圧、0.025秒の噴射時間の条件下で行なった。
遺伝子導入後の花弁は、NDM塩寒天培地上に置床し、明暗サイクル下(光強度23μmol/m2/秒、明期16時間、暗期8時間)、25℃で培養した。
実施例2 ツユクサF3’5’H遺伝子(CcF3'5'H)の探索とクローニング
ツユクサ(Commelina communis)の青く色づいたツボミの花弁から、RNeasy Plant Mini Kit(QIAGEN)を用いて全RNAを抽出し、このRNAを鋳型として、GeneRacer kit(Invitrogen)を用いてcDNAを調製した。
次にこのcDNAを鋳型としてRT-PCRを行った。PCR反応に用いたプライマーは、既知のF3'5'H遺伝子の配列(GenBank accession No.:D14590、AJ011862、AB262585、D14589、AB078514、AY566988、D85184、AY275430、AF313490、AY675558、AB012925)から設計した35FH−1(5'- ATGGTIGTIGARYTIATGAC -3';配列番号:3)と35FH−4(5'- CCRAAIGGIATIARYTCRAA -3';配列番号:4)である。反応は、98℃を10秒、56℃を30秒、72℃を1分のステップを40サイクル繰り返して行った。更に、得られた反応液を鋳型にして、プライマー35FH−2(5'- TGGATGGAYYTICARGGIAT -3';配列番号:5)とプライマー35FH−3(5'- CCDATIGCCCADATRTTIAC -3';配列番号:6)を用いてNested PCRを行った。反応は、98℃を10秒、56℃を30秒、72℃を1分のステップを40サイクル繰り返した。得られた反応産物の末端平滑化処理を行った後、pUC18(タカラバイオ)のHincIIサイトにクローニングし、p35FH23を得て、p35FH23に含まれる部分配列の塩基配列を決定した(CcF3'5'H部分配列)。
上記CcF3'5'H部分配列から、3’下流側の配列と5'上流側の配列をRACE法にて解析した。
3’RACE法は、CcF3'5'H部分配列より設計できるプライマーと、上記のツユクサRNA、そしてGeneRacer kit(Invitrogen)を用いて行った。PCR反応に用いたプライマーは、C35FH-3(5'- ATCTCCCTCGTATCGCAACC -3';配列番号:7)とGeneRacer 3'プライマーである。反応は、98℃を10秒、58℃を30秒、72℃を1分のステップを40サイクル繰り返した。得られた反応液を鋳型にして、プライマーC35FH-4(5'- GAAGCTTGTGAAGCCAATGG -3';配列番号:8)とGeneRacer 3' Nested プライマーを用いてNested PCRを行った。反応は、98℃を10秒、58℃を30秒、72℃を1分のステップを40サイクル繰り返した。得られた反応産物の末端平滑化処理を行った後、pUC18(タカラバイオ)のHincIIサイトにクローニングし、p35FHC43'を得て、p35FHC43'に含まれる3’下流側の配列の塩基配列を決定した(CcF3'5'H 3'RACE配列)。
5’RACE法は、CcF3'5'H部分配列より設計できるプライマーと、上記のツユクサRNA、そしてGeneRacer kit(Invitrogen)を用いて行った。PCR反応に用いたプライマーは、C35FH-6(5'- CGTCGCCTCGTGCTCTCGCAGTATC -3';配列番号:9)とGeneRacer 5'プライマーである。反応は、98℃を10秒、68℃を30秒、72℃を1分のステップを30サイクル繰り返した。得られた反応液を鋳型にして、プライマーC35FH-5(5'- TCTTCGAGAGCACCTTATCGAACCTC -3';配列番号:10)とGeneRacer 5' Nested プライマーを用いてNested PCRを行った。反応は、98℃を10秒、68℃を30秒、72℃を1分のステップを30サイクル繰り返した。得られた反応産物はpCR4/TOPO10(Invitrogen)にクローニングし、p35FH5'5を得て、p35FH5'5に含まれる5’上流側の配列の塩基配列を決定した(CcF3'5'H 5'RACE配列)。
CcF3'5'H 3'RACE配列とCcF3'5'H 5'RACE配列を基にツユクサF3’5’H遺伝子(CcF3'5'H)の全長のクローニングを行った。前記ツユクサRNAを鋳型にして、プライマーC35FH-7(5'- GAAAACCAATACAAAAACATACC -3';配列番号:11)とプライマーC35FH-10(5'- ATTGCTTCAAGTTCCCTAGC -3';配列番号:12)、そしてReady-To-Go RT-PCR Beads(Amersham Biosciences)を用いて、RT-PCRを行った。反応は、94℃を30秒、54℃を30秒、72℃を2分のステップを30サイクル繰り返した。更に、得られた反応液を鋳型にして、プライマーC35FH-7(配列番号:11)とC35FH-9(5'- GTTCCCTAGCCCCGTACCAC -3';配列番号:13)を用いてSemi Nested PCRを行った。反応は、98℃を10秒、54℃を30秒、72℃を1分のステップを30サイクル繰り返した。得られた反応産物はpCR4/TOPO10(Invitrogen)にクローニングし、p35FH79を得た。次に、p35FH79に含まれる全長のツユクサF3’5’H遺伝子の塩基配列を決定した(CcF3'5'H;配列番号:1)。尚、ツユクサから見出された本配列の遺伝子は新規の遺伝子である。該塩基配列でコードされるアミノ酸配列は、相同性解析よりデルフィニウムのF3'5'H遺伝子がコードするアミノ酸配列(GenBank accession No.:AY856345)と61%の相同性を有する。
実施例3 遺伝子導入用の発現ベクター(pBS-P35T35)の作成
pBS-P35T35はpBluescriptIISK-(Stratagene)内にカリフラワーモザイクウイルス35Sプロモーター(Hohn et al., Curent Topics in Microbiology and Immunology (1982) 96: 194-236.)と、タバコモザイクウイルスのオメガ配列(Gallie et al., Nucleic Acids Research (1987) 15: 3257-3273.)、制限酵素SwaIサイト、そしてカリフラワーモザイクウイルス35Sターミネーターをこの順に有するプラスミドである(図2)。このpBS-P35T35と実質的に機能が同等であるプラスミドは、以下のように構築可能である。
オリゴヌクレオチドSAS-S(5'- CTAGCTAGCGGCGCGCCTGCAGGATATCATTTAAATCCCGGG -3';配列番号:14)とオリゴヌクレオチドSAS-AS(5'- CCCGGGATTTAAATGATATCCTGCAGGCGCGCCGCTAGCTAG -3';配列番号:15)を熱変性後、徐々に室温に戻したものをNheI処理し、pBluescriptIISK-(Stratagene)のXbaI−EcoRVサイトへ連結し、制限酵素サイトを改変したプラスミドDNAであるpBS-SASを作製した。カリフラワーモザイクウイルスのゲノムDNA(GenBank accession V00140)を鋳型として、プライマーT-CaMV35S-SseI-F(5'- AACCTGCAGGAAATCACCAGTCTCTCTCTA-3';配列番号:16)と、プライマーT-CaMV35S-AscI-R(5'- GGCGCGCCATCGATAAGGGGTTATTAG -3';配列番号:17)を用いたPCRによって増幅される領域を制限酵素Sse8387IとAscIによって処理した。この断片をpBS-SASのSse8387I−AscIサイトへ連結し、pBS-T35Sを作製した。pJD301(Leon et al., Plant Physiology (1991) 95: 968-972.)より、HindIIIとHincIIによって切り出されるカリフラワーモザイクウイルス35Sプロモーターとタバコモザイクウイルスのオメガ配列をpBS-T35SのHindIII−SmaIサイトに連結し発現ベクター(pBS-P35T35)を作製した。
実施例4 ツユクサF3'5'H遺伝子の発現ベクターへのサブクローニング
前記CcF3'5'H全長配列を含むプラスミドDNA(p35FH79)を鋳型として、PCRにてツユクサF3'5'H遺伝子のORF部分を増幅し、発現ベクターpBS-P35T35にサブクローニングした。CcF35H-F(5'- ATGGTACCCCTTACGTACCTT -3';配列番号:18)とCcF35H-R(5'- TTATGTTGTTTTTATATTCTTATAAACG -3';配列番号:19)をプライマーとして、p35FH79を鋳型にPCRを行った。反応は、94℃を30秒、52℃を30秒、72℃を1分20秒のステップを25サイクル繰り返した。得られた反応産物をpBS-P35T35のSwaIサイトにクローニングし、p35CcF3'5'Hを得た。p35CcF3'5'Hは、植物細胞内でツユクサF3'5'H遺伝子を発現するDNAである。
実施例5 ツユクサF3'5'H遺伝子の機能発現の確認
赤色のコチョウラン(Dtps. Queen Beer 'Mantenkou')の花弁にp35CcF3'5'H 1.2μgを実施例1の方法で遺伝子導入し5日間培養したところ、花弁に濃い紫の細胞が多数出現した。一方、該遺伝子を含まない金粒子を導入した細胞では、変化は観察されなかった。
以上より、単離したツユクサF3'5'H遺伝子は、コチョウラン花弁細胞にフラボノイド3’,5’−水酸化酵素活性を付与し、その結果、青色色素であるデルフィニジンを産生させたものと考えられる。
実施例6 ツユクサF3'5'H遺伝子の酵素活性評価
ツユクサF3’5’H遺伝子の酵素活性を、青色色素であるデルフィニジン量で評価し、青色カーネーションの作出で有用とされている既知遺伝子(ペチュニア遺伝子)と比較した。
(1)ペチュニアF3'5'H遺伝子(PetF3'5'H)の単離
RNeasy Plant Mini Kit(QIAGEN)を用いて、市販のペチュニア(ハイブリッド)の開花前のツボミの花弁より全RNAを抽出した。このRNAを鋳型として、SuperscriptII First-Strand Synthesis System(Invitrogen)を用いてcDNAを調製した。次にこのcDNAを鋳型としてRT-PCRを行った。PCR反応に用いたプライマーは、既知のペチュニアF3'5'H遺伝子(PetF3'5'H)の二つの配列(GenBank accession No.:A29011、A29013)から設計したPetF3'5'H1-F(5'- ATGATGCTACTTACTGAGCTTGGTG -3';配列番号:20)とPetF3'5'H1-R(5'- CAACATGCGCAATTATAGCA -3';配列番号:21)、若しくはPetF3'5'H2-F(5'- ATGGTGCTACTTAGTGAGCTTGC -3';配列番号:22)とPetF3'5'H2-R(5'- AACCAACGTAAAGGCATGTT -3';配列番号:23)を用いた。反応は二種類とも、94℃を30秒、55℃を30秒、72℃を2.5分のステップを45サイクル繰り返した。得られた反応産物を各々pBS-P35T35のSwaIサイトにクローニングし、p35PetF3'5'H1及びp35PetF3'5'H2を得た。
(2)ツユクサF3'5'H遺伝子並びにペチュニアF3'5'H遺伝子の導入
赤色のコチョウラン(Dtps. Queen Beer 'Mantenkou')の花弁にツユクサ由来の遺伝子p35CcF3'5'H若しくは、ペチュニア由来の遺伝子(p35PetF3'5'H1又はp35PetF3'5'H2)それぞれ1.3μgを実施例1の方法に従い遺伝子導入した。又、遺伝子導入の際、遺伝子導入効率を測るための内部標準としてp35luc(ホタルルシフェラーゼ遺伝子)0.17μgも共導入した。このp35lucは、pSP-luc+(Promega)よりBglII−XbaIで切り出されたルシフェラーゼ遺伝子断片の末端を平滑処理した断片を、別途BamHIとSacIで処理して末端を平滑処理したpBI221(CLONTECH)へサブクローニングし、作製したものである。
遺伝子導入した花弁を5日間静置培養した後、液体窒素中で粉砕し、200μlの0.1×Passive Lysis Buffer(Dual-Luciferase Reporter Assay System、Promega)で懸濁したものを試料として、ルシフェラーゼの活性測定及びアントシアニジンの定量分析を行った。
ルシフェラーゼの活性測定
上記試料20μlに5×Passive Lysis Buffer(Promega)を5μlと100μlのLuciferase Assay Substrate(Promega)を加えた後、ルミノメーターflash'n glow LB955(BERTHOLD TECHNOLOGIES)を用いて、測定時間10秒の条件でルシフェラーゼ活性を測定した。
デルフィニジンの定量
上記試料150μlに2N塩酸を400μl加えた後98℃で2時間加水分解処理を行い、200μlのイソアミルアルコールにて抽出し、有機層を下記条件の液体クロマトグラフィー法でデルフィニジン量を測定した。
使用機器:Waters2690(Waters)、
カラム:Nucleosil 100-5C18 4.6×250mm(GL Sciences)
カラム温度:40℃、
溶出条件:1.5%リン酸水溶液(A液)と1.5%リン酸・20%酢酸・25%アセトニトリル水溶液(B液)を用いて、グラジェント(B液20%→85%を40分、B液85%を5分)をかけ、毎分1mlの流速で溶出した。
検出波長:531nm
標準品(デルフィニジン塩酸塩)を用いた絶対検量線法により、デルフィニジン量を定量した。更に、得られたデルフィニジン量は、ルシフェラーゼ活性を用いて補正した。この結果を表1に示す。表1のようにツユクサF3'5'H遺伝子によるデルフィニジンの蓄積量は、ペチュニアF3'5'H2遺伝子のそれと比較して約5倍程度高かった。又、ペチュニアF3'5'H1遺伝子を用いた試料からは、デルフィニジンが検出されなかった。
【0027】
【表1】

【0028】
実施例7 白色コチョウランの花弁へのF3'5'H遺伝子の導入
青色コチョウランを作出すべく白色のコチョウラン(Phal. amabilis)の花弁へ、実施例6(2)と同様にツユクサ由来の遺伝子(p35CcF3'5'H)あるいはペチュニア由来の遺伝子(p35PetF3'5'H1、p35PetF3'5'H2)それぞれ1.6μgを実施例1の方法に従い遺伝子導入した。しかし、該遺伝子を導入しても明確な花弁の色の変化は認められなかった。
そこで、アントシアニジン生合成経路(図1)においてF3’5’Hより上流にある酵素群((1)カルコン合成酵素:CHS、(2)カルコンイソメラーゼ:CHI及び(3)フラバノン3−水酸化酵素:F3H)をコードする遺伝子を単離し、その導入を試みた。
実施例8 コチョウランCHS遺伝子(PhCHS3)の単離
RNeasy Plant Mini Kit(QIAGEN)を用いて、コチョウラン(Dtps. Sogo Vivien×Dtps. Sogo Yenlin)開花直前の花弁より全RNAを抽出し、このRNAを鋳型として、SuperscriptII First-Strand Synthesis System(Invitrogen)を用いてcDNAを調製した。次にこのcDNAを鋳型としてRT-PCRを行った。PCR反応に用いたプライマーは、既知のコチョウランCHS遺伝子(PhCHS)の配列(GenBank accession No.:DQ089652)から設計したPhCHS3 F1(5'- AAGCTTGTGAGAGACGACGGA -3';配列番号:24)とPhCHS3 R1(5'- TGGCCCTAATCCTTCAAATT -3';配列番号:25)である。反応は、94℃を30秒、55℃を30秒、72℃を1分のステップを25サイクル繰り返した。この反応液を鋳型に再度同条件で反応産物を増幅させた。得られた反応産物はpBS-P35T35のSwaIサイトにクローニングし、p35PhCHS3を得た。次に、p35PhCHS3に含まれるコチョウランCHS遺伝子の全長塩基配列を決定した(PhCHS3、配列番号:26)。p35PhCHS3は、植物細胞内でコチョウランCHS遺伝子を発現するDNAである。
実施例9 コチョウランCHI遺伝子(PhCHI1)の単離
RNeasy Plant Mini Kit(QIAGEN)を用いて、コチョウラン(Dtps. Sogo Vivien×Dtps. Sogo Yenlin)開花直前の花弁より全RNAを抽出し、このRNAを鋳型として、SuperscriptII First-Strand Synthesis System(Invitrogen)を用いてcDNAを調製した。
次にこのcDNAを鋳型としてRT-PCRを行った。CHI遺伝子は、様々な植物で報告があり(GenBank accession No.:AY700850, AY086088, DQ160231, AJ004902, AF474923, XM_470129, U03433, AB187026)、PCR反応に用いたプライマーは既知のCHI遺伝子の配列から設計したCHI-dgF1(5'- TTYCTCGSYGGBGCMGGYGWVMGVGG -3';配列番号:28)とCHI-dgR1(5'- CMGGIGAIACVSCRTKYTYICCRATVAT -3';配列番号:29)を用いた。反応は、94℃を30秒、72℃を1分のステップを5サイクル、94℃を30秒、70℃を1分のステップを5サイクル行った後、94℃を30秒、68℃を30秒、72℃を1分のステップを25サイクル繰り返した。更に、得られた反応液を鋳型にして、プライマーCHI-dgF3(5'- TMIKYWCMGGISMITTYGARAARYT -3';配列番号:30)とプライマーCHI-dgR3(5'- TYICCRATVATIGWHTCCARIAYBGC -3';配列番号:31)を用いてNested PCRを行った。反応は、94℃を30秒、60℃を30秒、72℃を1分のステップを25サイクル繰り返した。得られた反応産物はpCR4-TOPO(Invitrogen)にクローニングし、PhCHIfrag16を得て、PhCHIfrag16に含まれる部分配列の塩基配列を決定した(PhCHI部分配列)。
PhCHI部分配列から3’下流側の配列と5'上流側の配列をRACE法にて解析した。
3’RACE法は、PhCHI部分配列より設計できるプライマーと、上記のRNA、そしてGeneRacer kit(Invitrogen)を用いて行った。PCR反応に用いたプライマーは、PhCHI-GSP F1(5'- ATGCTGCTGCCATTAACGGGTCA -3';配列番号:32)とGeneRacer 3'プライマーである。反応は、94℃を30秒、72℃を1分のステップを5サイクル、94℃を30秒、70℃を1分のステップを5サイクル行った後、94℃を30秒、60℃を30秒、72℃を1分のステップを25サイクル繰り返した。更に、得られた反応液を鋳型にして、プライマーPhCHI-GSP F2(5'- TCCGAGAAGGTCTCCGGGAACT -3';配列番号:33)とGeneRacer 3' Nested プライマーを用いてNested PCRを行った。反応は、94℃を30秒、60℃を30秒、72℃を1分のステップを25サイクル繰り返した。得られた反応産物はpCR4-TOPO(Invitrogen)にクローニングし、PhCHI3'RACE23を得て、PhCHI3'RACE23に含まれる3’下流側の配列の塩基配列を決定した(PhCHI 3'RACE配列)。
5’RACE法は、PhCHI部分配列より設計できるプライマーと、上記のRNA、そしてGeneRacer kit(Invitrogen)を用いて行った。PCR反応に用いたプライマーは、PhCHI-GSP R1(5'- GCATTCGTCAGCTTCTTGCTCTCT -3';配列番号:34)とGeneRacer 5'プライマーである。反応は、94℃を30秒、72℃を1分のステップを5サイクル、94℃を30秒、70℃を1分のステップを5サイクル行った後、94℃を30秒、60℃を30秒、72℃を1分のステップを25サイクル繰り返した。更に、得られた反応液を鋳型にして、プライマーPhCHI-GSP R2(5'- ATCACATCAGTCTCAGCCACA -3';配列番号:35)とGeneRacer 5' Nested プライマーを用いてNested PCRを行った。反応は、94℃を30秒、60℃を30秒、72℃を1分のステップを25サイクル繰り返した。得られた反応産物はpCR4-TOPO(Invitrogen)にクローニングし、PhCHI5'RACE54を得て、PhCHI5'RACE54に含まれる5’上流側の配列の塩基配列を決定した(PhCHI 5'RACE配列)。
PhCHI 3'RACE配列とPhCHI 5'RACE配列を基にコチョウランCHI遺伝子(PhCHI)の全長のクローニングを行った。上記のcDNAと、プライマーPhCHI init(5'- ATGGCAGAAACAGTGGCGACGCCCA -3';配列番号:36)とPhCHI term(5'- TCAAACGACTCCATCTTGCTC -3';配列番号:37)を用いてPCRを行った。反応は、94℃を30秒、65℃を30秒、72℃を1.5分のステップを45サイクル繰り返した。得られた反応産物はpBS-P35T35のSwaIサイトにクローニングし、p35PhCHI1を得た。次に、p35PhCHI1に含まれる全長のコチョウランCHI遺伝子の塩基配列を決定した(PhCHI1、配列番号:38)。尚、コチョウランから見出された本配列の遺伝子は新規の遺伝子である。該塩基配列でコードされるアミノ酸配列は、相同性解析よりチャのCHI遺伝子がコードするアミノ酸配列(GenBank accession No.:DQ120521)と54%の相同性を有する。p35PhCHI1は、植物細胞内でコチョウランCHI遺伝子を発現するDNAである。
実施例10 コチョウランF3H遺伝子(PhF3H1)の単離
RNeasy Plant Mini Kit(QIAGEN)を用いて、コチョウラン(Dtps. Sogo Vivien×Dtps. Sogo Yenlin)開花直前の花弁より全RNAを抽出し、このRNAを鋳型として、SuperscriptII First-Strand Synthesis System(Invitrogen)を用いてcDNAを調製した。
次にこのcDNAを鋳型としてRT-PCRを行った。F3H遺伝子は、様々な植物で報告があり(GenBank accession No.:DQ394303, AY221246, AJ493133, AY641730, AF184270, AB078956, AB201760, AY669324, AF036093, AB211958, AB187027, AB234905)、PCR反応に用いたプライマーは既知のF3H遺伝子の配列から設計したプライマーF3H-dgF1(5'- TIVGIGAYGARGABGARMGBCCIAA -3';配列番号:40)とプライマーF3H-dgR1(5'- ACBGCYYGRTGRTCHGCRTTCTTRAA -3';配列番号:41)を用いた。反応は、94℃を30秒、72℃を1分のステップを5サイクル、94℃を30秒、70℃を1分のステップを5サイクル行った後、94℃を30秒、68℃を30秒、72℃を1分のステップを25サイクル繰り返した。更に、得られた反応液を鋳型にして、プライマーF3H-dgF3(5'- AARYTBRGKTTYGAYATGWCHGGIG -3';配列番号:42)とプライマーF3H-dgR3(5'- GGHWSRACVGTDATCCAIGWBTT -3';配列番号:43)を用いてNested PCRを行った。反応は、94℃を30秒、60℃を30秒、72℃を1分のステップを25サイクル繰り返した。得られた反応産物はpCR4-TOPO(Invitrogen)にクローニングし、PhF3Hfrag26を得て、PhF3Hfrag26に含まれる部分配列の塩基配列を決定した(PhF3H部分配列)。
PhF3H部分配列から3’下流側の配列と5'上流側の配列をRACE法にて解析した。
3’RACE法は、PhF3H部分配列より設計できるプライマーと、上記のRNA、そしてGeneRacer kit(Invitrogen)を用いて行った。PCR反応に用いたプライマーは、PhF3H-GSPF1(5'- TTCTCATACCCAATCGGGAG -3';配列番号:44)とGeneRacer 3'プライマーである。反応は、94℃を30秒、72℃を1分のステップを5サイクル、94℃を30秒、70℃を1分のステップを5サイクル行った後、94℃を30秒、60℃を30秒、72℃を1分のステップを25サイクル繰り返した。得られた反応液と、プライマーPhF3H-GSPF2(5'- AATCGGGAGCCGCGATTACT -3';配列番号:45)とGeneRacer 3' Nested プライマーを用いてNested PCRを行った。反応は、94℃を30秒、60℃を30秒、72℃を1分のステップを25サイクル繰り返した。得られた反応産物はpCR4-TOPO(Invitrogen)にクローニングし、PhF3H3'RACE33を得て、PhF3H3'RACE33に含まれる3’下流側の配列の塩基配列を決定した(PhF3H 3'RACE配列)。
5’RACE法は、PhF3H部分配列より設計できるオリゴヌクレオチドと、上記のRNA、そしてGeneRacer kit(Invitrogen)を用いて行った。PCR反応に用いたプライマーは、PhF3H-GSPR1(5'- TCTGTGTGGCGCTTCAGGCC -3';配列番号:46)とGeneRacer 5'プライマーである。反応は、94℃を30秒、72℃を1分のステップを5サイクル、94℃を30秒、70℃を1分のステップを5サイクル行った後、94℃を30秒、60℃を30秒、72℃を1分のステップを25サイクル繰り返した。得られた反応液と、PhF3H-GSPR2(5'- TGAGGTCCGGTTGCGGGCATTTT -3';配列番号:47)とGeneRacer 5' Nested プライマーを用いてNested PCRを行った。反応は、94℃を30秒、60℃を30秒、72℃を1分のステップを25サイクル繰り返した。得られた反応産物はpCR4-TOPO(Invitrogen)にクローニングし、PhF3H5'RACE86を得て、PhF3H5'RACE86に含まれる5’上流側の配列の塩基配列を決定した(PhF3H 5'RACE配列)。
PhF3H 3'RACE配列とPhF3H 5'RACE配列を基にコチョウランF3H遺伝子の全長のクローニングを行った。上記のcDNAと、プライマーPhF3H init.(5'- ATGGCCCCAATACCATTCCTACCGA -3';配列番号:48)とPhF3H term.(5'- CCTTAAGCTAAAATCTCATTTAATGCCTTTGCTCC -3';配列番号:49)を用いてPCRを行った。反応は、94℃を30秒、65℃を30秒、72℃を1.5分のステップを40サイクル繰り返した。得られた反応産物はpBS-P35T35のSwaIサイトにクローニングし、p35PhF3H1を得た。次に、p35PhF3H1に含まれる全長のコチョウランF3H遺伝子の塩基配列を決定した(PhF3H1、配列番号:50)。尚、コチョウランから見出された本配列の遺伝子は新規の遺伝子である。該塩基配列でコードされるアミノ酸配列は、相同性解析よりBromheadia finlaysonianaのF3H遺伝子がコードするアミノ酸配列(GenBank accession No.:X89199)と86%の相同性を有する。p35PhF3H1は、植物細胞内でコチョウランF3H遺伝子を発現するDNAである。
実施例11 白色コチョウランの花弁へのF3'5'H遺伝子とアントシアニン関連遺伝子の導入
白色のコチョウラン(Phal. amabilis)の花弁へ、コチョウラン由来のCHS遺伝子(p35PhCHS3:実施例8)、CHI遺伝子(p35PhCHI1:実施例9)、F3H遺伝子(p35PhF3H1:実施例10)、そしてツユクサ由来のF3’5’H遺伝子(p35CcF3'5'H:実施例2)を実施例1の方法に従い共導入した。しかし、花弁の色の変化は認められなかった。
そこで、更にアントシアニン生合成経路においてF3'5'Hより下流にある酵素((1)ジヒドロフラボノール4−還元酵素:DFR、(2)アントシアニジン合成酵素:ANS)をコードする遺伝子を単離し、その導入を試みた。
実施例12 コチョウランDFR遺伝子(PhDFR)の単離
RNeasy Plant Mini Kit(QIAGEN)を用いて、コチョウラン(Dtps. Queen Beer 'Mantenkou')のツボミの花弁より全RNAを抽出し、このRNAを鋳型として、GeneRacer kit(Invitrogen)を用いてcDNAを調製した。
次にこのcDNAを鋳型としてRT-PCRを行った。DFR遺伝子は、様々な植物で報告がある(GenBank accession No.:AAB62873, AAC17843, AAD49343, AAQ83576, AAU93766, AAY32600, AAY32601, AAY32602, BAB40789, BAE79202)。PCR反応に用いたプライマーは、前述のDFR遺伝子の配列から設計したDFRD-F1(5'- TTYCAYGTIGCIACNCCNATG -3';配列番号:52)とDFRD-R1(5'- DATNGCRTCRTCRAACATYTC -3';配列番号:53)を用いた。反応は、94℃を30秒、48℃を30秒、72℃を1分のステップを40サイクル繰り返した。得られた反応液を鋳型にして、プライマーDFRD-F2(5'- ATGAAYTTYCARWSIRARGAYCC -3';配列番号:54)とプライマーDFRD-R2(5'- RCAIATRTAICKNCIRTTNGC -3';配列番号:55)を用いてNested PCRを行った。反応は、94℃を30秒、48℃を30秒、72℃を1分のステップを40サイクル繰り返した。更に、得られた反応液を鋳型にして、プライマーDFRD-F3(5'- GARAAYGARGTNATHAARCC -3';配列番号:56)とDFRD-R3(5'- RTCRTCIARRTGNACRAAYTG -3';配列番号:57)を用いて再度Nested PCRを行った。反応は、94℃を30秒、48℃を30秒、72℃を30秒のステップを40サイクル繰り返した。得られた反応産物はpCR4-TOPO(Invitrogen)にクローニングし、PhDFR-D/pCR4を得て、PhDFR-D/pCR4に含まれる部分配列の塩基配列を決定した(PhDFR部分配列)。
PhDFR部分配列から3’下流側の配列と5'上流側の配列をRACE法にて解析した。
3’RACE法は、PhDFR部分配列より設計できるプライマーと、上記のRNA、そしてGeneRacer kit(Invitrogen)を用いて行った。PCR反応に用いたプライマーは、PhDFR-F1(5'- GGTCATGCAAAAGGTCGGGCAGCGTAA -3';配列番号:58)とGeneRacer 3'プライマーである。反応は、94℃を30秒、72℃を1分のステップを5サイクル繰り返し、続いて94℃を30秒、70℃を1分のステップを5サイクル繰り返し、続いて94℃を30秒、68℃を30秒、72℃を1分のステップを25サイクル繰り返した。更に、得られた反応液を鋳型にして、PhDFR-F2(5'- GTGATCTTCACATCTTCCGCAGGAACAGT -3';配列番号:59)とGeneRacer 3' Nested プライマーを用いてNested PCRを行った。反応は、94℃を30秒、65℃を30秒、72℃を1分のステップを25サイクル繰り返した。得られた反応産物はpCR4/TOPO10(Invitrogen)にクローニングし、PhDFR 3'RACE/pCR4を得て、PhDFR 3'RACE/pCR4に含まれる3’下流側の配列の塩基配列を決定した(PhDFR3'RACE配列)。
5’RACE法は、PhDFR部分配列より設計できるプライマーと、上記のRNA、そしてGeneRacer kit(Invitrogen)を用いて行った。PCR反応に用いたプライマーは、PhDFR-R4(5'- ATGATTCATTAAAAATCCGAAAAAAAGACCACTACAA -3';配列番号:60)とGeneRacer 5'プライマーである。反応は、94℃を30秒、72℃を1分のステップを5サイクル繰り返し、続いて94℃を30秒、70℃を1分のステップを5サイクル繰り返し、続いて94℃を30秒、68℃を30秒、72℃を1分のステップを25サイクル繰り返した。更に、得られた反応液を鋳型にして、プライマーPhDFR-R3(5'- AACCATGCATAATAAAGCAGATGTGTAAAT -3';配列番号:61)とGeneRacer 5' Nested プライマーを用いてNested PCRを行った。反応は、94℃を30秒、65℃を30秒、72℃を1分のステップを25サイクル繰り返した。得られた反応産物はpCR4-TOPO(Invitrogen)にクローニングし、PhDFR 5'RACE/pCR4を得、PhDFR 5'RACE/pCR4に含まれる5’上流側の配列の塩基配列を決定した(PhDFR 5'RACE配列)。
PhDFR 3'RACE配列とPhDFR 5'RACE配列を基にコチョウランDFR遺伝子の全長のクローニングを行った。上記のRNAと、プライマーPhDFR-F8A5(5'- AAAAAATGGAGGATGTGAGGAAGGGTCCTGTT -3';配列番号:62)とPhDFR-R5(5'- ACATGATTCATTAAAAATCCGAAAAAAAGACCA -3';配列番号:63)、そしてReady-To-Go You Prime First Strand Beads(Amersham Biosciences社)を用いて、RT-PCRを行った。反応は、98℃を30秒、68℃を30秒、72℃を1.5分のステップを35サイクル繰り返した。得られた反応産物はpBS-P35T35にクローニングし、p35PhDFRを得た。次に、p35PhDFRに含まれる全長のDFR遺伝子の塩基配列を決定した(PhDFR、配列番号:64)。尚、コチョウランから見出された本配列の遺伝子は新規の遺伝子である。該塩基配列でコードされるアミノ酸配列は、相同性解析よりBromheadia finlaysonianaのDFR遺伝子がコードするアミノ酸配列(GenBank accession No.:AF007096)と86%の相同性を有する。p35PhDFRは、植物細胞内でコチョウランDFR遺伝子を発現するDNAである。
実施例13 コチョウランANS遺伝子(PhANS1)の単離
RNeasy Plant Mini Kit(QIAGEN)を用いて、コチョウラン(Dtps.Sogo Vivien×Dtps.Sogo Yenlin)開花直前の花弁より全RNAを抽出し、このRNAを鋳型として、SuperscriptII First-Strand Synthesis System(Invitrogen)を用いてcDNAを調製した。
次にこのcDNAを鋳型としてRT-PCRを行った。PCR反応に用いたプライマーは既知のANS遺伝子の配列から設計したANS-dgF2(5'- TICARGGBTAYGGIAGYARRYTIGCIRMYA -3';配列番号:66)とANS-dgR2(5'- GGYTCRCARAAIAYIRCCCAIGADA -3';配列番号:67)を用いた。反応は、94℃を30秒、60℃を30秒、72℃を1.5分のステップを40サイクル繰り返した。得られた反応液を鋳型に再度同じプライマーを用いて、94℃を30秒、56℃を30秒、72℃を1分のステップ30サイクルの反応を行った。得られた反応産物はpCR4-TOPO(Invitrogen)にクローニングし、PhANSfrag10を得て、PhANSfrag10に含まれる部分配列の塩基配列を決定した(PhANS部分配列)。
PhANS部分配列から3’下流側の配列と5'上流側の配列をRACE法にて解析した。
3’RACE法は、PhANS部分配列より設計できるプライマーと、上記のRNA、そしてGeneRacer kit(Invitrogen)を用いて行った。PCR反応に用いたプライマーは、PhANS3RACEGSP1(5'- GCCCACACCGACGTCAGCTCCCTCTCCT -3';配列番号:68)とGeneRacer 3'プライマーである。反応は、94℃を30秒、72℃を1.5分のステップを5サイクル、94℃を30秒、70℃を1.5分のステップを5サイクル行った後、94℃を30秒、70℃を30秒、72℃を1.5分のステップを25サイクル繰り返した。更に、得られた反応液を鋳型にして、プライマーPhANS3RACEGSP2(5'- CGTCGGGGATGCGCTCGAGATCCTCAGC -3';配列番号:69)とGeneRacer 3' Nested プライマーを用いてNested PCRを行った。反応は、94℃を10秒、58℃を10秒、72℃を1分のステップを35サイクル繰り返した。得られた反応産物はpCR4-TOPO(Invitrogen)にクローニングし、PhANS3'RACE37を得て、PhANS3'RACE37に含まれる3’下流側の配列の塩基配列を決定した(PhANS 3'RACE配列)。
5’RACE法は、PhANS部分配列より設計できるプライマーと、上記のRNA、そしてGeneRacer kit(Invitrogen)を用いて行った。PCR反応に用いたプライマーは、PhANS5RACEGSP1(5'- AGTCCGCGGGTTCAGTCGGCCAGATGGT -3';配列番号:70)とGeneRacer 5'プライマーである。反応は、94℃を30秒、72℃を1.5分のステップを5サイクル、94℃を30秒、70℃を1.5分のステップを5サイクル行った後、94℃を30秒、70℃を30秒、72℃を1.5分のステップを25サイクル繰り返した。得られた反応液と、プライマーPhANS5RACEGSP2(5'- CCGTCTTCTCCGGCGGGTAGACGAGGTG -3';配列番号:71)とGeneRacer 5' Nested プライマーを用いてNested PCRを行った。反応は、94℃を10秒、58℃を10秒、72℃を1分のステップを35サイクル繰り返した。得られた反応産物はpCR4-TOPO(Invitrogen)にクローニングし、PhANS5'RACE15を得て、PhANS5'RACE15に含まれる5’上流側の配列の塩基配列を決定した(PhANS 5'RACE配列)。
PhANS 3'RACE配列とPhANS 5'RACE配列を基にコチョウランANS遺伝子の全長のクローニングを行った。上記のcDNAと、プライマーPhANS init(5'- ATGGCCACCAAAGCAATCCCACC -3';配列番号:72)とPhANS term(5'- TCAATCCACAGGCGCCTTCT -3';配列番号:73)を用いてPCRを行った。反応は、94℃を30秒、69℃を30秒、72℃を1.5分のステップを35サイクル繰り返した。得られた反応産物はpBS-P35T35のSwaIサイトにクローニングし、p35PhANS1を得た。次に、p35PhANS1に含まれる全長のANS遺伝子(PhANS1)の塩基配列を決定した(PhANS1、配列番号:74)。尚、コチョウランから見出された本配列の遺伝子は新規の遺伝子である。該塩基配列でコードされるアミノ酸配列は、相同性解析よりアンスリウムのANS遺伝子がコードするアミノ酸配列(GenBank accession No.:EF079869)と58%の相同性を有する。p35PhANS1は、植物細胞内でコチョウランANS遺伝子を発現するDNAである。
実施例14 白色コチョウランの花弁へのF3'5'H遺伝子とアントシアニジン関連遺伝子の導入
白色のコチョウラン(Phal. amabilis)の花弁へ、ツユクサ由来のF3’5’H遺伝子(CcF3'5'H)とコチョウラン由来のCHS(PhCHS3)、CHI(PhCHI1)、F3H(PhF3H1)、DFR(PhDFR)及びANS(PhANS1)遺伝子を実施例1の方法に従い共導入したところ、花弁に薄い青色の細胞が確認された。
この事より、白色コチョウランの青色への花色改変にはDFR及びANS遺伝子が重要であることが判明した。そこで、更に濃い花色に改変すべく他植物のDFR遺伝子並びにANS遺伝子の探索を行なった。
実施例15 ガーベラのDFR遺伝子およびANS遺伝子の単離とその共導入
(1)ガーベラDFR遺伝子(GerDFR)の単離
RNeasy Plant Mini Kit(QIAGEN)を用いて、市販のガーベラハイブリッドのツボミの花弁より全RNAを抽出し、このRNAを鋳型として、SuperscriptII First-Strand Synthesis System(Invitrogen)を用いてcDNAを調製した。次にこのcDNAを鋳型としてRT-PCRを行った。PCR反応に用いたプライマーは、既知のガーベラDFR遺伝子(GerDFR)の配列(GenBank accession No.:Z17221)から設計したGerDFR-F(5'- ATGGAAGAGGATTCTCCGGC -3';配列番号:76)とGerDFR-R(5'- CTATTGGCCTTCTTTTGAACAACAAA -3';配列番号:77)である。反応は、98℃を10秒、55℃を10秒、72℃を1分30秒のステップを45サイクル繰り返した。得られた反応産物をpBS-P35T35のSwaIサイトにクローニングし、ガーベラDFR遺伝子を得た(p35GerDFR)。p35GerDFRは、植物細胞内でガーベラDFR遺伝子を発現するDNAである。
(2)ガーベラANS遺伝子(GerANS)の単離
上記cDNAを鋳型としてRT-PCRを行った。PCR反応に用いたプライマーは、既知のガーベラANS遺伝子(GerANS)の配列(GenBank accession No.:AY997842)から設計したGerANS-F(5'- ATGGTGATTCAAGCAACCACA -3';配列番号:78)とGerANS-R(5'- CTAGTTTTGCATCACTTCGTCTTTAT -3';配列番号:79)である。反応は、94℃を30秒、56℃を30秒、72℃を1分10秒のステップを45サイクル繰り返した。得られた反応産物をpBS-P35T35のSwaIサイトにクローニングし、ガーベラANS遺伝子を得た(p35GerANS)。p35GerANSは、植物細胞内でガーベラANS遺伝子を発現するDNAである。
(3)ガーベラDFR及びガーベラANS遺伝子の共導入
白色のコチョウラン(Phal. amabilis)の花弁へ、コチョウラン由来のCHS(PhCHS3)、CHI(PhCHI1)、F3H(PhF3H1)の各遺伝子と、ツユクサ由来のF3’5’H遺伝子(CcF3'5'H)、そしてガーベラ由来のDFR遺伝子(GerDFR)並びにANS遺伝子(GerANS)を共導入したところ、花弁に実施例14よりも濃い青紫色の細胞が新たに出現した。
実施例16 トレニアのDFR遺伝子およびANS遺伝子の単離とその共導入
(1)トレニアDFR遺伝子(TorDFR)の単離
RNeasy Plant Mini Kit(QIAGEN)を用いて、市販のトレニア(Torenia fournieri)のツボミの花弁より全RNAを抽出し、SuperscriptII First-Strand Synthesis System(Invitrogen)を用いてcDNAを調製した。このcDNAを鋳型としてRT-PCRを行った。PCR反応に用いたプライマーは、既知のトレニアDFR遺伝子(TorDFR)の配列(GenBank accession AB012924)から設計したオリゴヌクレオチドTorDFR-F(5'- ATGAGCATGGAAGTAGTAGTACCA -3';配列番号:80)とTorDFR-R(5'- CTATTCTATCTTATGTTCTCCATGG -3';配列番号:81)である。反応は、94℃を30秒、56℃を30秒、72℃を1分10秒のステップを45サイクル繰り返した。得られた反応産物をpBS-P35T35のSwaIサイトにクローニングし、トレニアのDFR遺伝子を得た(p35TorDFR)。p35TorDFRは、植物細胞内でトレニアDFR遺伝子を発現するDNAである。
(2)トレニアANS遺伝子(TorANS)の単離
上記cDNAを鋳型として、RT-PCRを行った。PCR反応に用いたプライマーは、既知のトレニアANS遺伝子(TorANS)の配列(GenBank accession AB044091)から設計したTorANS-F(5'- ATGGTTTCTCCAGCATCTCCGA -3';配列番号:82)とTorANS-R(5'- TCACTCAACACTCTTATCATCATGCTC -3';配列番号:83)である。反応は、94℃を30秒、56℃を30秒、72℃を1分10秒のステップを45サイクル繰り返した。得られた反応産物をpBS-P35T35のSwaIサイトにクローニングし、トレニアのANS遺伝子を得た(p35TorANS)。p35TorANSは、植物細胞内でトレニアANS遺伝子を発現するDNAである。
(3)トレニアDFR及びトレニアANS遺伝子の共導入
白色のコチョウラン(Phal. amabilis)の花弁へ、コチョウラン由来のCHS(PhCHS3)、CHI(PhCHI1)及びF3H(PhF3H1)の各遺伝子と、ツユクサ由来のF3’5’H遺伝子(CcF3'5'H)、そしてトレニア由来のDFR遺伝子(TorDFR)並びにANS遺伝子(TorANS)を実施例1の方法に従い共導入したところ、花弁に実施例14よりも濃い青紫色の細胞が新たに出現した。
最良のDFR遺伝子及びANS遺伝子の検討
白色コチョウランの青色への改変に関して、最良のDFR遺伝子及びANS遺伝子を見出すべく植物由来の異なる遺伝子を導入し、比較検討した。
実施例17 花弁細胞の着色の観察
花弁細胞の着色は、実体顕微鏡SZX12(オリンパス)及び肉眼観察により行なった。
花弁の着色程度の基準は、肉眼で確認可能なものを”III”、実体顕微鏡の倍率32倍以下にて確認可能なものを”II”、倍率32倍以上でないと確認できないものを”I”、着色が確認できないものを”−”とした。
実施例18 白色コチョウランの花弁におけるANS遺伝子の比較
白色のコチョウラン(Phal. amabilis)の花弁にANS遺伝子のみ異なる下記三種の遺伝子セットを導入し、着色の程度を観察した。
(1)コチョウランANS遺伝子(PhANS1)+コチョウランCHS遺伝子(PhCHS3)+コチョウランCHI遺伝子(PhCHI1)+コチョウランF3H遺伝子(PhF3H1)+ツユクサF3’5’H遺伝子(CcF3'5'H)+ガーベラDFR遺伝子(GerDFR)
(2)ガーベラANS遺伝子(GerANS)+コチョウランCHS遺伝子(PhCHS3)+コチョウランCHI遺伝子(PhCHI1)+コチョウランF3H遺伝子(PhF3H1)+ツユクサF3’5’H遺伝子(CcF3'5'H)+ガーベラDFR遺伝子(GerDFR)
(3)トレニアANS遺伝子(TorANS)+コチョウランCHS遺伝子(PhCHS3)+コチョウランCHI遺伝子(PhCHI1)+コチョウランF3H遺伝子(PhF3H1)+ツユクサF3’5’H遺伝子(CcF3'5'H)+ガーベラDFR遺伝子(GerDFR)
その結果、それぞれの試料で同程度の青紫色の細胞が出現した。それぞれ22枚の花弁について出現した青紫色の細胞の着色程度を比較した結果を図3に示す。
実施例19 白色コチョウランの花弁におけるDFR遺伝子の比較
白色のコチョウラン(Phal. amabilis)の花弁にDFR遺伝子のみ異なる下記三種の遺伝子セットを導入し、着色の程度を観察した。
(1)コチョウランDFR遺伝子(PhDFR)+コチョウランCHS遺伝子(PhCHS3)+コチョウランCHI遺伝子(PhCHI1)+コチョウランF3H遺伝子(PhF3H1)+ツユクサF3’5’H遺伝子(CcF3'5'H)+トレニアANS遺伝子(TorANS)
(2)ガーベラDFR遺伝子(GerDFR)+コチョウランCHS遺伝子(PhCHS3)+コチョウランCHI遺伝子(PhCHI1)+コチョウランF3H遺伝子(PhF3H1)+ツユクサF3’5’H遺伝子(CcF3'5'H)+トレニアANS遺伝子(TorANS)
(3)トレニアDFR遺伝子(TorDFR) +コチョウランCHS遺伝子(PhCHS3)+コチョウランCHI遺伝子(PhCHI1)+コチョウランF3H遺伝子(PhF3H1)+ツユクサF3’5’H遺伝子(CcF3'5'H)+トレニアANS遺伝子(TorANS)
その結果、それぞれの試料で青紫色の細胞が出現した。それぞれ23枚の花弁の着色の濃さを比較した結果を図4に示すが、PhDFR遺伝子を用いた場合は、GerDFR遺伝子やTorDFR遺伝子を用いた場合と比較して、青紫色の着色程度が低くなっていた。濃い青紫の花色を実現するには、コチョウランの内在DFR遺伝子(PhDFR)よりも、ガーベラのDFR遺伝子(GerDFR)やトレニアのDFR遺伝子(TorDFR)のほうが適していると考えられる。
実施例20 ツユクサF3’5’H遺伝子の有用性
白色コチョウランにおけるツユクサF3’5’H遺伝子の有用性を確認すべくペチュニア遺伝子との比較試験を行なった。
コチョウラン由来のCHS遺伝子(PhCHS3)とCHI遺伝子(PhCHI1)とF3H遺伝子(PhF3H1);ガーベラ由来のDFR遺伝子(GerDFR)とANS遺伝子(GerANS)を導入すると共にツユクサF3’5’H遺伝子((1) CcF3’5’H)又はペチュニアF3’5’H遺伝子((2) PetF3’5’H1、または(3) PetF3’5’H2)をそれぞれ共に白色コチョウラン(Phal. amabilis)の花弁へ共導入した。
その結果、ペチュニアF3'5'H1遺伝子(PetF3’5’H1)またはペチュニアF3'5'H2遺伝子(PetF3’5’H2)を用いた場合では殆ど青色の着色は認められなかったが、ツユクサF3'5'H遺伝子(CcF3’5’H)を用いた場合では明らかな着色が確認できた(図5)。
実施例21 F3H、CHI、CHS遺伝子の遺伝子導入の必要性
白色コチョウランの青色改変における各遺伝子の必要性について検討した。
白色のコチョウラン(Phal. amabilis)の花弁を材料に下記四種の遺伝子セットを導入し、着色の程度を観察した。
(1)ツユクサF3’5’H遺伝子(CcF3'5'H) +トレニアDFR遺伝子(TorDFR)+トレニアANS遺伝子(TorANS)
(2)コチョウランF3H遺伝子(PhF3H1)+ツユクサF3’5’H遺伝子(CcF3'5'H) +トレニアDFR遺伝子(TorDFR)+トレニアANS遺伝子(TorANS)
(3)コチョウランCHI遺伝子(PhCHI1)+コチョウランF3H遺伝子(PhF3H1)+ツユクサF3’5’H遺伝子(CcF3'5'H) +トレニアDFR遺伝子(TorDFR)+トレニアANS遺伝子(TorANS)
(4)コチョウランCHS遺伝子(PhCHS3)+コチョウランCHI遺伝子(PhCHI1)+コチョウランF3H遺伝子(PhF3H1)+ツユクサF3’5’H遺伝子(CcF3'5'H) +トレニアDFR遺伝子(TorDFR)+トレニアANS遺伝子(TorANS)
これらをPhal. amabilisの花弁に遺伝子導入し、細胞の着色を観察したところ、(1)以外の試料で青紫色の細胞が出現した。それぞれ試料18枚の着色の程度を比較した結果を図6に示す。この結果より、F3H遺伝子(PhF3H1)は着色に必須であることが分かった。
実施例22 白色コチョウランの花弁への遺伝子導入により出現した色素の分析
前記実験において白色コチョウラン(Phal. amabilis)の花弁に出現した青紫色の細胞に含まれる色素が、デルフィニジン関連色素であるのか確認を行った。白色コチョウラン(Phal. amabilis)の花弁に、コチョウラン由来のCHI遺伝子とF3H遺伝子とANS遺伝子、及びガーベラ由来のDFR遺伝子とツユクサF3’5’H遺伝子とを共導入し、5日間培養した花弁から実施例6と同様の方法でアントシアニジンを抽出し、分析した。その結果、色素の主成分としてデルフィニジンが検出された。検出されたデルフィニジン量は、一試料あたり16ngであった(5試料の平均)。一方、上記遺伝子セットからツユクサF3’5’H遺伝子を除いた群では、デルフィニジンは検出されなかった。この結果より、白色コチョウランへの遺伝子導入で観察された青紫色の細胞は、デルフィニジン誘導体によって着色したものであった。
実施例23 Phal. amabilis以外の白色コチョウランへの適用
純白色の大型コチョウラン(Phal. White Star)の長さ1.7cmのつぼみの花弁に、コチョウラン由来のCHS遺伝子とCHI遺伝子とF3H遺伝子、及びガーベラ由来のDFR遺伝子とANS遺伝子、とツユクサF3’5’H遺伝子を実施例1の方法に従い共導入したところ、花弁に青紫色の細胞が新たに出現した。
実施例24 アグロバクテリウム法によるコチョウラン形質転換用DNAの作製
遺伝子銃法だけでなく、アグロバクテリウム法を用いてもコチョウランの形質転換は可能である(Belarmino and Mii, Plant Cell Reports (2000) 19:435-442.、Mishiba et al., Plant Cell Reports (2005) 24: 297-303.)。これらの方法に従って遺伝子組換え体を得るために形質転換用DNAの構築を行った。それぞれのプラスミドの地図と作製手順を図7と図8に示す。
(1)pBI-SAS1の構築
PCT/JP02/12268に記載のpBI-RHLをNotIとHindIIIで切断した部位へ、実施例04のpBS-SASをNotIとHindIIIで切断して生じる短い断片をサブクローニングし、pBI-SAS1を構築した。pBI-SAS1は、アグロバクテリウムを用いて植物の形質転換を行い、植物にハイグロマイシン耐性を付与できるプラスミドである。
(2)pBS-35S-FTの構築
コチョウランは花が咲くまでに1年以上の期間を要するため、花芽誘導遺伝子FT (Kobayashi et al., Science (1999) 286: 1960-1962.)をコチョウランで発現させるDNAを構築した。
FTcDNAはシロイヌナズナ全植物体から調整した全RNAからRT-PCRにより増幅して調製した。PCRにはAtFT 2nd-F(5'- GAAACCACCTGTTTGTTCAAGA -3';配列番号:84)とAtFT 2nd-R(5'- TCAATTGGTTATAAAGGAAGAAGC -3';配列番号:85)をプライマーに用い、分離できたFT cDNAをpBS-P35T35をSwaIで切断して生じた部位に挿入して、センス方向にcDNAが挿入されたクローンを選抜し、pBS-P35S-FTを構築した。pBS-35S-FTはCaMV 35Sプロモーター、CaMV 35SターミネーターでFTの転写が制御されるプラスミドである。
(3)pBIH-35S-CcF3’5’Hの構築
p35CcF3’5’HをBamHIで切断後、Klenow断片で突出末端を平滑化し、さらにAscIで切断してプラスミドからDNA断片を切り出した。このDNA断片を、pBI-SAS1をAscIとSwaIで切断して生じた部位に挿入してpBIH-35S-CcF3’5’Hを構築した。pBIH-35S-CcF3’5’Hは選抜マーカーであるHPTとCaMV 35Sプロモーター、CaMV 35Sターミネーターで転写が制御されるCcF3'5'Hが順に連結されたT-DNA領域を持つバイナリーベクターである。
(4)pBS-35S-mPhCHS3の構築
PhCHS3 cDNA内にあるSphI切断部位にアミノ酸置換を伴わない塩基置換を導入して、SphIで切断されないcDNAを作成した。塩基置換はPhCHS3-1038F (5'- GTAACATGTCGAGCGCTTGCGTTCTTTTCATACTCG -3';配列番号:86)とPhCHS3-1073R (5'- CGAGTATGAAAAGAACGCAAGCGCTCGACATGTTAC -3';配列番号:87)をプライマーとして用い、pBS-35S- PhCHS3を鋳型にしてPyrobest(タカラバイオ社製)を用いてDNA合成を行なった。その後、DpnI処理によって鋳型プラスミドを消化し、pBS-35S- mPhCHS3を構築した。
(5)pBS-35S-UP1の構築
p35PhCHI1をAscIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断してプラスミドからDNA断片を切り出した。このDNA断片を、p35PhF3H1をXbaIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断して生じた部位に挿入してpBS-35S-UP1を構築した。pBS-35S-UP1はCaMV 35Sプロモーター、CaMV 35Sターミネーターで転写が制御される各cDNAがPhCHI1、PhF3H1の順に連結されたプラスミドである。
(6)pBS-35S-Del1の構築
p35TorANSをAscIで切断後、Klenow断片で突出末端を平滑化し、さらにKpnIで切断してプラスミドからDNA断片を切り出した。このDNA断片を、p35TorDFRをXbaIで切断後、Klenow断片で突出末端を平滑化し、さらにKpnIで切断して生じた部位に挿入してpBS-35S-Del1を構築した。pBS-35S-Del1はCaMV 35Sプロモーター、CaMV 35Sターミネーターで転写が制御される各cDNAがTorANS、TorDFRの順に連結されたプラスミドである。
(7)pBS-35S-Del2の構築
p35CcF3'5'HをAscIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断してプラスミドからDNA断片を切り出した。このDNA断片を、pBS-35S-Del1をXbaIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断して生じた部位に挿入してpBS-35S-Del2を構築した。pBS-35S-Del2はCaMV 35Sプロモーター、CaMV 35Sターミネーターで転写が制御される各cDNAがCcF3'5'H、TorANS、TorDFRの順に連結されたプラスミドである。
(8)pBS-35S-Del8の構築
pBS-35S-UP1をAscIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断してプラスミドからDNA断片を切り出した。このDNA断片を、pBS-35S-Del2をXbaIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断して生じた部位に挿入してpBS-35S-Del8を構築した。pBS-35S-Del8はCaMV 35Sプロモーター、CaMV 35Sターミネーターで転写が制御される各cDNAがPhCHI1、PhF3H1 、CcF3'5'H、TorANS、TorDFRの順に連結されたプラスミドである。
(9)pBS-35S-Del9の構築
pBS-35S-mPhCHS3をAscIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断してプラスミドからDNA断片を切り出した。このDNA断片を、pBS-35S-Del8をXbaIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断して生じた部位に挿入してpBS-35S-Del9を構築した。pBS-35S-Del9はCaMV 35Sプロモーター、CaMV 35Sターミネーターで転写が制御される各cDNAがmPhCHS3、PhCHI1、PhF3H1、CcF3'5'H、TorANS、TorDFRの順に連結されたプラスミドである。
(10)pBS-35S-Del15の構築
p35CcF3'5'HをAscIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断してプラスミドからDNA断片を切り出した。このDNA断片を、pBS-35S-FTをXbaIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断して生じた部位に挿入してpBS-35S-Del15を構築した。pBS-35S-Del15はCaMV 35Sプロモーター、CaMV 35Sターミネーターで転写が制御される各cDNAがCcF3'5'H、FTの順に連結されたプラスミドである。
(11)pBS-35S-Del16の構築
p35TorDFRをAscIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断してプラスミドからDNA断片を切り出した。このDNA断片を、p35PhANS1をXbaIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断して生じた部位に挿入してpBS-35S-Del16を構築した。pBS-35S-Del16はCaMV 35Sプロモーター、CaMV 35Sターミネーターで転写が制御される各cDNAがTorDFR、PhANS1の順に連結されたプラスミドである。
(12)pBS-35S-UP4の構築
pBS-35S-Del16をAscIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断してプラスミドからDNA断片を切り出した。このDNA断片を、pBS-35S-UP1をXbaIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断して生じた部位に挿入してpBS-35S-UP4を構築した。pBS-35S-UP4はCaMV 35Sプロモーター、CaMV 35Sターミネーターで転写が制御される各cDNAがTorDFR、PhANS1 、PhCHI1、PhF3H1の順に連結されたプラスミドである。
(13)pBS-35S-Del17の構築
p35CcF3'5'HをAscIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断してプラスミドからDNA断片を切り出した。このDNA断片を、pBS-35S-UP4をXbaIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断して生じた部位に挿入してpBS-35S-Del17を構築した。pBS-35S-Del17はCaMV 35Sプロモーター、CaMV 35Sターミネーターで転写が制御される各cDNAがCcF3'5'H、TorDFR、PhANS1 、PhCHI1、PhF3H1の順に連結されたプラスミドである。
(14)pBS-35S-Del18の構築
pBS-35S-Del15をAscIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断してプラスミドからDNA断片を切り出した。このDNA断片を、pBS-35S-UP4をXbaIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断して生じた部位に挿入してpBS-35S-Del18を構築した。pBS-35S-Del18はCaMV 35Sプロモーター、CaMV 35Sターミネーターで転写が制御される各cDNAがCcF3'5'H、FT、TorDFR、PhANS1 、PhCHI1、PhF3H1の順に連結されたプラスミドである。
(15)pBIH-35S-Del8の構築
pBS-35S-Del8をSphIで切断後、Klenow断片で突出末端を平滑化し、さらにAscIで切断してプラスミドからDNA断片を切り出した。このDNA断片を、pBI-SAS1をAscIとSwaIで切断して生じた部位に挿入してpBIH-35S-Del8を構築した。pBIH-35S-Del8は選抜マーカーであるHPTとCaMV 35Sプロモーター、CaMV 35Sターミネーターで転写が制御される各cDNAがPhCHI1、PhF3H1、CcF3'5'H、TorANS、TorDFRの順に連結されたT-DNA領域を持つバイナリーベクターである。
(16)pBIH-35S-Del9の構築
pBS-35S-Del9をSphIで切断後、Klenow断片で突出末端を平滑化し、さらにAscIで切断してプラスミドからDNA断片を切り出した。このDNA断片を、pBI-SAS1をAscIとSwaIで切断して生じた部位に挿入してpBIH-35S-Del9を構築した。pBIH-35S-Del9は選抜マーカーであるHPTとCaMV 35Sプロモーター、CaMV 35Sターミネーターで転写が制御される各cDNAがmPhCHS3、PhCHI1、PhF3H1、CcF3'5'H、TorANS、TorDFRの順に連結されたT-DNA領域を持つバイナリーベクターである。
(17)pBIH-35S-Del17の構築
pBS-35S-Del17をSphIで切断後、Klenow断片で突出末端を平滑化し、さらにAscIで切断してプラスミドからDNA断片を切り出した。このDNA断片を、pBI-SAS1をAscIとSwaIで切断して生じた部位に挿入してpBIH-35S-Del17を構築した。pBIH-35S-Del17は選抜マーカーであるHPTとCaMV 35Sプロモーター、CaMV 35Sターミネーターで転写が制御される各cDNAがCcF3'5'H、TorDFR、PhANS1 、PhCHI1、PhF3H1の順に連結されたT-DNA領域を持つバイナリーベクターである。
(18)pBIH-35S-Del18の構築
pBS-35S-Del18をSphIで切断後、Klenow断片で突出末端を平滑化し、さらにAscIで切断してプラスミドからDNA断片を切り出した。このDNA断片を、pBI-SAS1をAscIとSwaIで切断して生じた部位に挿入してpBIH-35S-Del18を構築した。pBIH-35S-Del18は選抜マーカーであるHPTとCaMV 35Sプロモーター、CaMV 35Sターミネーターで転写が制御される各cDNAがCcF3'5'H、FT、TorDFR、PhANS1 、PhCHI1、PhF3H1の順に連結されたT-DNA領域を持つバイナリーベクターである。
実施例25 形質転換コチョウランの作出
バイナリベクターに構築された実施例24のDNA(pBIH-35S-CcF3’5’H、pBIH-35S-Del8、pBIH-35S-Del9、pBIH-35S-Del17、そしてpBIH-35S-Del18)とアグロバクテリウムEHA101株を用いて作製された形質転換コチョウランは、50mg/mlのハイグロマイシンで選抜される。その結果、実施例24で示した遺伝子が染色体上に組み込まれたコチョウランを得ることができる。
得られた形質転換コチョウランからは、花茎の腋芽など植物体の一部を利用してPLBを誘導し、クローン増殖が可能である。得られた形質転換コチョウランを交配親に用いて、交配育種を行い、導入遺伝子を有する後代を得ることができる。
以上のようにツユクサのF3’5’H遺伝子を用いれば、もともと色のついていたコチョウランからは青味がかった品種が、白色のコチョウランからは青色の品種が新たに作出される。
実施例26 シンビジウム花弁におけるツユクサF3'5'H遺伝子の機能評価
白色シンビジウム(Cym. Lovely Angel 'The Two Virgins')の長さ30mm程度のつぼみから採取した花弁10枚へ、下記3種の遺伝子セットを実施例1の方法に従い、共導入した。
(1)ツユクサF3'5'H遺伝子(CcF3'5'H)+コチョウランCHS遺伝子(PhCHS3)+コチョウランCHI遺伝子(PhCHI1)+コチョウランF3H遺伝子(PhF3H1)+ガーベラDFR遺伝子(GerDFR)+ガーベラANS遺伝子(GerANS)
(2)ペチュニアF3'5'H2遺伝子(PetF3'5'H2)+コチョウランCHS遺伝子(PhCHS3)+コチョウランCHI遺伝子(PhCHI1)+コチョウランF3H遺伝子(PhF3H1)+ガーベラDFR遺伝子(GerDFR)+ガーベラANS遺伝子(GerANS)
(3)コチョウランCHS遺伝子(PhCHS3)+コチョウランCHI遺伝子(PhCHI1)+コチョウランF3H遺伝子(PhF3H1)+ガーベラDFR遺伝子(GerDFR)+ガーベラANS遺伝子(GerANS)
遺伝子導入した花弁を5日間静置培養した後、実体顕微鏡にて観察したところ、ツユクサF3'5'H遺伝子(CcF3'5'H)を含む遺伝子セット(1)を導入した花弁に濃い青紫色の細胞が新たに出現した。一方、ペチュニアF3'5'H2遺伝子(PetF3'5'H2)を含む遺伝子セット(2)を導入した花弁では、一部の花弁で薄い紫色の細胞が観察されるにとどまり、F3’5’H遺伝子を含まない遺伝子セット(3)を導入した花弁では全く花色の変化が認められなかった。図9に実施例17に記載の方法で、それぞれの花弁に出現した青紫色の細胞の着色程度を評価した結果を示す。
【配列表フリーテキスト】
【0029】
SEQ ID NO: 1, Nucleotide sequence encoding Commelina communis flavonoid 3',5'-hydroxylase
SEQ ID NO: 2, Amino acid sequence of Commelina communis flavonoid 3',5'-hydroxylase
SEQ ID NO: 3, Primer 35FH-1
SEQ ID NO: 4, Primer 35FH-4
SEQ ID NO: 5, Primer 35FH-2
SEQ ID NO: 6, Primer 35FH-3
SEQ ID NO: 7, Primer C35FH-3
SEQ ID NO: 8, Primer C35FH-4
SEQ ID NO: 9, Primer C35FH-6
SEQ ID NO: 10, Primer C35FH-5
SEQ ID NO: 11, Primer C35FH-7
SEQ ID NO: 12, Primer C35FH-10
SEQ ID NO: 13, Primer C35FH-9
SEQ ID NO: 14, Oligonucleotide SAS-S
SEQ ID NO: 15, Oligonucleotide SAS-AS
SEQ ID NO: 16, Primer T-CaMV35S-SseI-F
SEQ ID NO: 17, Primer T-CaMV35S-AscI-R
SEQ ID NO: 18, Primer CcF35H-F
SEQ ID NO: 19, Primer CcF35H-R
SEQ ID NO: 20, Primer PetF3'5'H1-F
SEQ ID NO: 21, Primer PetF3'5'H1-R
SEQ ID NO: 22, Primer PetF3'5'H2-F
SEQ ID NO: 23, Primer PetF3'5'H2-R
SEQ ID NO: 24, Primer PhCHS3 F1
SEQ ID NO: 25, Primer PhCHS3 R1
SEQ ID NO: 26, Nucleotide sequence encoding Doritaenopsis hybrid cultivar chalcone synthase
SEQ ID NO: 27, Amino acid sequence of Doritaenopsis hybrid cultivar chalcone synthase
SEQ ID NO: 28, Primer CHI-dgF1
SEQ ID NO: 29, Primer CHI-dgR1
SEQ ID NO: 30, Primer CHI-dgF3
SEQ ID NO: 31, Primer CHI-dgR3
SEQ ID NO: 32, Primer PhCHI-GSP F1
SEQ ID NO: 33, Primer PhCHI-GSP F2
SEQ ID NO: 34, Primer PhCHI-GSP R1
SEQ ID NO: 35, Primer PhCHI-GSP R2
SEQ ID NO: 36, Primer PhCHI init
SEQ ID NO: 37, Primer PhCHI term
SEQ ID NO: 38, Nucleotide sequence encoding Doritaenopsis hybrid cultivar chalcone isomerase
SEQ ID NO: 39, Amino acid sequence of Doritaenopsis hybrid cultivar chalcone isomerase
SEQ ID NO: 40, Primer F3H-dgF1
SEQ ID NO: 41, Primer F3H-dgR1
SEQ ID NO: 42, Primer F3H-dgF3
SEQ ID NO: 43, Primer F3H-dgR3
SEQ ID NO: 44, Primer PhF3H-GSPF1
SEQ ID NO: 45, Primer PhF3H-GSPF2
SEQ ID NO: 46, Primer PhF3H-GSPR1
SEQ ID NO: 47, Primer PhF3H-GSPR2
SEQ ID NO: 48, Primer PhF3H init.
SEQ ID NO: 49, Primer PhF3H term.
SEQ ID NO: 50, Nucleotide sequence encoding Doritaenopsis hybrid cultivar flavanone 3-hydroxylase
SEQ ID NO: 51, Amino acid sequence of Doritaenopsis hybrid cultivar flavanone 3-hydroxylase
SEQ ID NO: 52, Primer DFRD-F1
SEQ ID NO: 53, Primer DFRD-R1
SEQ ID NO: 54, Primer DFRD-F2
SEQ ID NO: 55, Primer DFRD-R2
SEQ ID NO: 56, Primer DFRD-F3
SEQ ID NO: 57, Primer DFRD-R3
SEQ ID NO: 58, Primer PhDFR-F1
SEQ ID NO: 59, Primer PhDFR-F2
SEQ ID NO: 60, Primer PhDFR-R4
SEQ ID NO: 61, Primer PhDFR-R3
SEQ ID NO: 62, Primer PhDFR-F8A5
SEQ ID NO: 63, Primer PhDFR-R5
SEQ ID NO: 64, Nucleotide sequence encoding Doritaenopsis hybrid cultivar dihydroflavonol 4-reductase
SEQ ID NO: 65, Amino acid sequence of Doritaenopsis hybrid cultivar dihydroflavonol 4-reductase
SEQ ID NO: 66, Primer ANS-dgF2
SEQ ID NO: 67, Primer ANS-dgR2
SEQ ID NO: 68, Primer PhANS3RACEGSP1
SEQ ID NO: 69, Primer PhANS3RACEGSP2
SEQ ID NO: 70, Primer PhANS5RACEGSP1
SEQ ID NO: 71, Primer PhANS5RACEGSP2
SEQ ID NO: 72, Primer PhANS init
SEQ ID NO: 73, Primer PhANS term
SEQ ID NO: 74, Nucleotide sequence encoding Doritaenopsis hybrid cultivar anthocyanidin synthase
SEQ ID NO: 75, Amino acid sequence of Doritaenopsis hybrid cultivar anthocyanidin synthase
SEQ ID NO: 76, Primer GerDFR-F
SEQ ID NO: 77, Primer GerDFR-R
SEQ ID NO: 78, Primer GerANS-F
SEQ ID NO: 79, Primer GerANS-R
SEQ ID NO: 80, Primer TorDFR-F
SEQ ID NO: 81, Primer TorDFR-R
SEQ ID NO: 82, Primer TorANS-F
SEQ ID NO: 83, Primer TorANS-R
SEQ ID NO: 84, Primer AtFT 2nd-F
SEQ ID NO: 85, Primer AtFT 2nd-R
SEQ ID NO: 86, Primer PhCHS3-1038F
SEQ ID NO: 87, Primer PhCHS3-1073R
【技術分野】
【0001】
本発明は、遺伝子組換え技術を用いて青い花色を呈する植物を製造する方法に関する。詳しくは、ツユクサの色素合成酵素の一つであるフラボノイド3’,5’―水酸化酵素(F3’5’H)をコードする遺伝子を用いて青い花色を呈するラン科植物を製造する方法に関する。
【背景技術】
【0002】
鑑賞用植物において花の色は特に重要な形質として、古くから様々な色の花が交配育種により作出されてきた。しかし、交配育種の場合、遺伝子資源が交配可能な種内に限定されるため改変可能な色調には限界があった。また、花の色のような特定の形質のみをある特定の品種に導入するためには戻し交雑を何世代も繰り返す必要があり、多大な労力と時間が必要である。さらに、植物によって交配育種の期間は異なり、花が咲くまでに数年から数十年かかる植物もある。特に、コチョウランやシンビジウムのようなラン科植物の多くは、花をつけるまでに長い時間を要し、育種に時間がかかる植物である。そのため、市場の要望にも拘らずコチョウランやシンビジウムにはいまだ新しい花色、特に青い花色の優良品種は存在しない。
【0003】
近年、組換えDNA技術により種や属を越えた育種が可能となり、従来の交配育種では得られなかった色調を持つ新品種の育成に期待が持たれている。
【0004】
花の色は主にアントシアニン、カロテノイド、ベタレインの3種の色素に起因する。その内で青色を司るのは極大吸収波長幅が最も広いアントシアニン(オレンジ色から青色)である。アントシアニンはフラボノイドの一種で図1に示した代謝経路で生合成される。アントシアニンの色調は、その化学構造に大きく依存し、B環の水酸基の数が多いほど青くなる。B環の水酸化は、フラボノイド3’−水酸化酵素(F3’H)およびフラボノイド3’,5’−水酸化酵素(F3’5’H)によって触媒される。花弁細胞内にて、F3’H活性とF3’5’H活性がない場合にはペラルゴニジン(橙色から赤色)が合成され、F3’H活性がある場合はシアニジン(赤から紅色)が合成され、F3’5’H活性がある場合はデルフィニジン(青色)が合成される。そのため、青い花色の作出には、F3'5'Hが大きな役割を果たすと考えられている。
【0005】
このような観点から、F3'5'Hに着目した遺伝子組換えにより青い花色を呈する植物を作出する研究が進められている。
【0006】
既知のF3’5’Hをコードする遺伝子としては、フウリンソウ、ニチニチソウ、ペチュニア、トルコギキョウ、ニーレンベルギア、バーベナ、リンドウ 、ワタ 、Lycianthes rantonnei 、ジャガイモ 、トレニア等の植物由来のものが知られているが、ツユクサから分離された遺伝子の報告は無い。
公知遺伝子を用いて花色を改変した事例としては、カーネーションDFR欠損品種へペチニュア由来のF3'5'H遺伝子及びDFR遺伝子を導入し青い色のカーネーションを製造する方法(特許文献1)や、内在代謝系を抑制したバラにパンジー由来のF3'5'H遺伝子を導入し青い色のバラを製造する方法(特許文献2)がある。
【0007】
一方、コチョウランに関しては、内在遺伝子の過剰発現による花色改変の報告があるが、青色のコチョウランを作出するには至っていない(非特許文献1)。また、シンビジウムに関しても青色の品種を作出した報告はない。
【先行技術文献】
【特許文献】
【0008】
【特許文献1】国際公開公報 WO 1996/036716
【特許文献2】国際公開公報 WO 2005/017147
【非特許文献】
【0009】
【非特許文献1】Su and Hsu, Biotechnology Letters (2003) 25: 1933-1939.
【発明の概要】
【発明が解決しようとする課題】
【0010】
青い花色の作出には、F3'5'Hが大きな役割を果たすことが知られており、より高発現するF3'5'H遺伝子が求められている。
本発明の第一の課題は、青色コチョウランの作出を可能にする高発現型F3'5'H遺伝子を見出すことにある。また、第二の課題は、その高発現型F3'5'H遺伝子を用いて青い花色を呈するラン科植物を作出することにある。
【課題を解決するための手段】
【0011】
本発明者らは、上記課題を解決するために鋭意検討した結果、ツユクサ由来のF3’5’H遺伝子が既知遺伝子を上回る効果を示すことを見出し、さらに当該遺伝子をコチョウランに導入することにより青い花色に改変できることを見出し、本発明を完成するに至った。
すなわち、本発明は、配列番号2で表されるアミノ酸配列又は同アミノ酸配列に対して少なくとも90%の相同性のアミノ酸配列を有するツユクサのフラボノイド3’,5’−水酸化酵素をコードする遺伝子に関する。
【0012】
また本発明は、上記遺伝子を含んでなるベクターに関する。
【0013】
さらに本発明は、上記遺伝子を植物に導入し、発現させることを特徴とする花色改変植物の製造方法に関する。
【0014】
また、本発明は、上記遺伝子並びにトレニア又はガーベラのジヒドロフラボノール4−還元酵素をコードする遺伝子をラン科植物に導入し、発現させることを特徴とする花色改変植物の製造方法。
【0015】
また、本発明は、上記遺伝子;トレニア又はガーベラのジヒドロフラボノール4−還元酵素をコードする遺伝子;フラバノン3−水酸化酵素をコードする遺伝子;並びにアントシアニジン合成酵素をコードする遺伝子を白い花色のラン科植物に遺伝子導入し、発現させることを特徴とする青い花色のラン科植物の製造方法に関する。
【0016】
さらには、本発明は、上記の製造方法により得られる花色改変植物、若しくは改変された花色と同じ性質を有するその子孫またはその組織に関する。
【0017】
尚、本発明において「フラボノイド3’,5’−水酸化酵素」(F3’5’H)とは、ジヒドロケンフェロールからジヒドロミリセチンを生成する反応を触媒する酵素をいう。又、「フラバノン3−水酸化酵素」(F3H)とは、ナリンゲニンからジヒドロケンフェロールを生成する反応を触媒する酵素をいい、「ジヒドロフラボノール4−還元酵素」(DFR)とは、ジヒドロミリセチンからロイコデルフィニジンを生成する反応を触媒する酵素をいい、「アントシアニジン合成酵素」(ANS)とは、ロイコデルフィニジンからデルフィニジンを生成する反応を触媒する酵素をいう。
【発明の効果】
【0018】
ツユクサのF3’5’H遺伝子を用いることにより、青色系統の多様な花色を持つ植物を作出することができる。より詳しくは、従来の交配育種法では達成できなかった青い花色のラン科植物の作出が本発明により可能となる。
本発明のその他の目的、特徴、優秀性及びその有する観点は、以下の記載より当業者にとっては明白であろう。しかしながら、以下の記載及び具体的な実施例等の記載を含めた本件明細書の記載は本発明の好ましい態様を示すものであり、説明のためにのみ示されていることを理解されたい。本明細書に開示した本発明の意図及び範囲内で、種々の変化及び/又は改変(あるいは装飾)をなすことは、以下の記載及び本明細書のその他の部分からの知識により、当業者には容易に明らかであろう。本明細書で引用されている全ての特許文献及び参考文献は、説明の目的で引用されているもので、それらは本明細書の一部としてその内容はここに含めて解釈されるべきものである。
【図面の簡単な説明】
【0019】
【図1】アントシアニンの合成経路。
【図2】花弁への遺伝子導入に用いるプラスミドベクター。P-CaMV35Sは、カリフラワーモザイクウイルス35Sプロモーターを示す。Ωは、タバコモザイクウイルスのオメガ配列を示す。Tは、カリフラワーモザイクウイルス由来の転写終結配列を示す。
【図3】植物由来の異なるANS遺伝子のPhal. amabilisの花弁への遺伝子導入。
【図4】植物由来の異なるDFR遺伝子のPhal. amabilisの花弁への遺伝子導入。
【図5】植物由来の異なるF3’5’H遺伝子のPhal. amabilisの花弁への遺伝子導入。
【図6】白色コチョウランの花色改変のために必要な遺伝子の特定。
【図7】コチョウランの形質転換を行うDNAの構築手順の概略(1)。
【図8】コチョウランの形質転換を行うDNAの構築手順の概略(2)。
【図9】白色シンビジウムの花弁への遺伝子導入。
【発明を実施するための形態】
【0020】
本発明者らは、青いラン科植物を作出すべく、青色系色素(デルフィニジン)に関与するF3’5’H遺伝子に着目し、カーネーションで実績のある既知のペチュニア由来のF3’5’H遺伝子をコチョウランに導入した。しかし、期待された効果は認められなかった。そこで、より優れた遺伝子を見いだすべく種々の植物のF3’5’H遺伝子を鋭意クローニングした。その結果、ツユクサ由来の遺伝子(配列番号:1)が非常に高い色素生合成能を示すことを見出した。本遺伝子はコチョウランの花弁細胞へ導入した場合、驚くべきことに先行技術であるペチュニア由来の遺伝子と比較して、5倍のデルフィニジンを産生した。又、本発明の遺伝子を赤色コチョウランの花弁細胞に導入したところ、花色は青味がかった紫に変化した。
更に、上記F3’5’H遺伝子に加えて、アントシアニン合成経路においてF3’5’Hよりも上流の反応を触媒するF3Hの遺伝子、並びにF3’5’Hよりも下流の反応を触媒するDFRとANSの遺伝子を白色コチョウランの花弁細胞に導入すると、花色は白色から青色となった。特に、DFR遺伝子をガーベラ若しくはトレニア由来の遺伝子を用いると、その花色は更に濃い青色を呈した。
【0021】
上述のとおり、本発明で見出されたツユクサ由来の遺伝子は既存遺伝子以上に優れた遺伝子であり、本遺伝子を用いることにより青色系コチョウランの作出が可能となる。更に、本遺伝子の優秀性は、コチョウランのみならずシンビジウムにおいても検証され、広く他の花卉植物の花色改変にも応用可能である。
【0022】
F3’5’H遺伝子は、ツユクサ(学名:Commelina communis)のゲノムDNA、またはそこから転写されるmRNAを鋳型としたcDNAから単離され、配列番号:2に記載のタンパク質をコードする配列番号:1に記載の遺伝子である。本発明にかかる遺伝子としては、F3’5’H酵素活性を持つ限りにおいて上記遺伝子と高い類似性を示す遺伝子も含まれる。高い類似性とは、配列番号:2とのアミノ酸配列の相同性が、85%以上、好ましくは90%以上、より好ましくは95%以上、さらに好ましくは98%以上のものが挙げられる。
【0023】
フラバノン3−水酸化酵素(F3H)遺伝子,ジヒドロフラボノール4−還元酵素(DFR)遺伝子及びアントシアニジン合成酵素(ANS)遺伝子は、新規若しくは公知の遺伝子を用いることができる。具体的には、F3H遺伝子としては、GenBankに登録のあるもの(アクセッション番号:DQ394303, AY221246, AJ493133, AY641730, AF184270, AB078956, AB201760, AY669324, AF036093, AB211958, AB187027, AB234905)などが挙げられ、DFR遺伝子としては、GenBankに登録のあるもの(アクセッション番号:AAB62873, AAC17843, AAD49343, AAQ83576, AAU93766, AAY32600, AAY32601, AAY32602, BAB40789, BAE79202)などが挙げられ、ANS遺伝子としては、GenBankに登録のあるもの(アクセッション番号:AY585677, AY228485, AF015885, AY581048, U82432, AY695817, AB208689, AY997840, AY382828, AY256380, AF026058, Y07955, AF384050, AB097216, AB087206, AB198869, AB044091, AY123768, AB234906)などが挙げられる。特に、DFR遺伝子としては、アクセッション番号:Z17221で示されるガーベラ由来の遺伝子、及びアクセッション番号:AB012924で示されるトレニア由来の遺伝子が望ましい。又、本発明によって見出されたコチョウラン由来のF3H遺伝子(配列番号:50)、DFR遺伝子(配列番号:64)及びANS遺伝子(配列番号:74)等の新規遺伝子も用いることができる。
【0024】
また、本発明はこれらの遺伝子を含む組換えベクター、特に発現ベクターに関する。
発現ベクターは該遺伝子を導入すべき宿主の種類に依存して発現制御領域、例えばプロモーターおよびターミネーター、複製起点等を含有する。プロモーターとしては、花弁細胞で遺伝子の発現を誘導するものが挙げられ、例えば、コチョウランのCHS遺伝子由来のプロモーター、カリフラワーモザイクウイルス(CaMV)35S由来のプロモーターなどが挙げられる。又、ターミネーターとしては、例えば、コチョウランのCHS遺伝子由来のターミネーター、カリフラワーモザイクウイルス(CaMV)35S由来のターミネーターなどが挙げられる。
具体的には、ツユクサのF3’5’H遺伝子は、プロモーター配列の3’下流に連結され、F3’5’H遺伝子の3’下流には、転写終結配列が付加されていることが望ましい。
F3H遺伝子、DFR遺伝子及び/又はANSの遺伝子もF3’5’H遺伝子と同様にプロモーター配列の3’下流に連結されて植物に導入することができる。
発現ベクターの作製は制限酵素、リガーゼ等を用いて常法に従って行うことができる。また、発現ベクターによる宿主の形質転換も常法に従って行うことができる。
本発明における花弁細胞で遺伝子を発現させる方法としては、例えば、遺伝子銃法、アグロバクテリウム法、エレクトロポレーション法、PEG法、ウイルス法などが挙げられる。
アグロバクテリウム法を用いてF3’5’H遺伝子で形質転換を行うためのベクターの一例を、図7(pBIH-35S-CcF3'5'H)に示す。更に、F3H、DFR、ANSの遺伝子も、各々独立若しくは一緒にツユクサのF3’5’H遺伝子と同じベクター上に構築することができる(図7、8)。
【0025】
本発明において形質転換可能な植物は、花卉植物であり、好ましくはラン科植物である。ラン科植物としては、コチョウラン、シンビジウム、デンドロビウム、デンドロキルム、オンシジウム、オドントグロッサム、ミルトニア、カトレヤ等が挙げられる。その中でも、コチョウラン及びシンビジウムが好ましい。シンビジウムとはCymbidium属に属する植物をいい、また、コチョウランには、Phalaenopsis属とDoritaenopsis属に属するものをいう。
【実施例】
【0026】
以下に実施例を掲げ、本発明を具体的に説明するが、この実施例は単に本発明の説明のため、その具体的な態様の参考のために提供されているものである。これらの例示は本発明の特定の具体的な態様を説明するためのものであるが、本願で開示する発明の範囲を限定したり、あるいは制限することを表すものではない。本発明では、本明細書の思想に基づく様々な実施形態が可能であることは理解されるべきである。
なお、DNA の切断、連結、大腸菌の形質転換、遺伝子の塩基配列決定、PCR等一般の遺伝子組換えに必要な方法は、各操作に使用する市販の試薬、機械装置等に添付されている説明書や、実験書(例えば「Molecular Cloning: A Laboratory Manual
(Third Edition,Sambrook and Russell,2001,Cold Spring Harbor Laboratory Press) 」)に基本的に従った。PCR反応には、GeneAmp PCR system 9700(PE Applied Biosystems)を使用した。機器の操作は、他に詳細に記載するもの以外は、機器に添付される説明書に記載される標準的な操作方法に従った。全ての実施例は、他に詳細に記載するもの以外は、標準的な技術を用いて実施したもの、又は実施することのできるものであり、これは当業者にとり周知で慣用的なものである。
本発明において新規に取得した遺伝子でコードされるアミノ酸配列と既知のアミノ酸配列との類似性を調べる相同性検索プログラムとしては、BLASTP 2.2.15(http://www.ddbj.nig.ac.jp/search/blast-j.html 文献は、Altschul et al., Nucleic Acids Res. (1997) 25: 3389-3402.)を使用した。ここで言う相同性とは、配列全体に渡るアミノ酸の一致性であり、新規に取得した遺伝子にコードされるアミノ酸配列と既知のアミノ酸配列とを一致性が高い形で並べ、両者で一致したアミノ酸数を比較域のアミノ酸数で割って得た値である。なお、ここで言う一致性が高い形とは、上記BLASTPプログラムのパラメーターをデフォルトにした状態(ギャップ有、期待値10、フィルター有)で出力されたアライメント結果である。本実施例で記載した相同性は、解析時に上記相同性検索解析において最も高い相同性を示した既知アミノ酸配列について記載したものである。
実施例1 コチョウラン花弁への遺伝子導入
本明細書の実施例に特に記述が無い場合は、以下に述べる遺伝子導入方法を用いて、コチョウラン花弁に各種遺伝子を導入し、その機能を評価した。全ての遺伝子は、5’側にプロモーターを、3’側にターミネーターを連結したDNA構造をとり、花弁細胞内で発現する形状で導入された。
コチョウランのつぼみを、1%次亜塩素酸ナトリウム水溶液で5分間滅菌し、滅菌水で3回洗浄した後、このつぼみを分解して、ラテラルセパル、ドーサルセパル、ペタルをNDM塩(Tokuhara and Mii, Plant Cell Reports (1993) 13: 7-11.)と0.6%アガロースを含む寒天培地上に置床した。尚、つぼみは、Phal. amabilisの場合は長さ15mm程度のもの、Dtps. Queen Beer 'Mantenkou'の場合は長さ8mm程度のものを用いた。
導入するDNAはHi Speed Plasmid Midi Kit(QIAGEN)を用いて精製し、該遺伝子は遺伝子銃法にて遺伝子導入を行なった。尚、複数の遺伝子を同時導入する際は、該DNA溶液同士を均等に混ぜたものを用意し、導入用のDNA溶液とした。
その際の金粒子とDNAの吸着は、以下の割合で行った。20μlのTE bufferに溶解したDNA(遺伝子が含まれるプラスミドDNA一種につき2μgを混ぜて溶解したもの)を50μlの金粒子混濁液(粒子直径は1.0μm、60mg/mlの50%グリセロール)と混ぜ、この混合液70μlに50μlの 2.5M塩化カルシウムと10μlの0.2Mスペルミジンを加えて懸濁し、DNAを金粒子に吸着させた。次に、遠心操作により、上清を除去し、70%エタノールと100%エタノールで粒子を洗浄した後、得られた該沈殿物に60μlの100%エタノールを加えた懸濁液を試料溶液とし、その10μlを一回の遺伝子導入に用いた。遺伝子銃は、IDERA GIE-III(TANAKA Co. Ltd.)を用いた。遺伝子導入条件は、銃口から試料までの距離12cm、−80kPaの減圧下、0.3MPaのヘリウムガス圧、0.025秒の噴射時間の条件下で行なった。
遺伝子導入後の花弁は、NDM塩寒天培地上に置床し、明暗サイクル下(光強度23μmol/m2/秒、明期16時間、暗期8時間)、25℃で培養した。
実施例2 ツユクサF3’5’H遺伝子(CcF3'5'H)の探索とクローニング
ツユクサ(Commelina communis)の青く色づいたツボミの花弁から、RNeasy Plant Mini Kit(QIAGEN)を用いて全RNAを抽出し、このRNAを鋳型として、GeneRacer kit(Invitrogen)を用いてcDNAを調製した。
次にこのcDNAを鋳型としてRT-PCRを行った。PCR反応に用いたプライマーは、既知のF3'5'H遺伝子の配列(GenBank accession No.:D14590、AJ011862、AB262585、D14589、AB078514、AY566988、D85184、AY275430、AF313490、AY675558、AB012925)から設計した35FH−1(5'- ATGGTIGTIGARYTIATGAC -3';配列番号:3)と35FH−4(5'- CCRAAIGGIATIARYTCRAA -3';配列番号:4)である。反応は、98℃を10秒、56℃を30秒、72℃を1分のステップを40サイクル繰り返して行った。更に、得られた反応液を鋳型にして、プライマー35FH−2(5'- TGGATGGAYYTICARGGIAT -3';配列番号:5)とプライマー35FH−3(5'- CCDATIGCCCADATRTTIAC -3';配列番号:6)を用いてNested PCRを行った。反応は、98℃を10秒、56℃を30秒、72℃を1分のステップを40サイクル繰り返した。得られた反応産物の末端平滑化処理を行った後、pUC18(タカラバイオ)のHincIIサイトにクローニングし、p35FH23を得て、p35FH23に含まれる部分配列の塩基配列を決定した(CcF3'5'H部分配列)。
上記CcF3'5'H部分配列から、3’下流側の配列と5'上流側の配列をRACE法にて解析した。
3’RACE法は、CcF3'5'H部分配列より設計できるプライマーと、上記のツユクサRNA、そしてGeneRacer kit(Invitrogen)を用いて行った。PCR反応に用いたプライマーは、C35FH-3(5'- ATCTCCCTCGTATCGCAACC -3';配列番号:7)とGeneRacer 3'プライマーである。反応は、98℃を10秒、58℃を30秒、72℃を1分のステップを40サイクル繰り返した。得られた反応液を鋳型にして、プライマーC35FH-4(5'- GAAGCTTGTGAAGCCAATGG -3';配列番号:8)とGeneRacer 3' Nested プライマーを用いてNested PCRを行った。反応は、98℃を10秒、58℃を30秒、72℃を1分のステップを40サイクル繰り返した。得られた反応産物の末端平滑化処理を行った後、pUC18(タカラバイオ)のHincIIサイトにクローニングし、p35FHC43'を得て、p35FHC43'に含まれる3’下流側の配列の塩基配列を決定した(CcF3'5'H 3'RACE配列)。
5’RACE法は、CcF3'5'H部分配列より設計できるプライマーと、上記のツユクサRNA、そしてGeneRacer kit(Invitrogen)を用いて行った。PCR反応に用いたプライマーは、C35FH-6(5'- CGTCGCCTCGTGCTCTCGCAGTATC -3';配列番号:9)とGeneRacer 5'プライマーである。反応は、98℃を10秒、68℃を30秒、72℃を1分のステップを30サイクル繰り返した。得られた反応液を鋳型にして、プライマーC35FH-5(5'- TCTTCGAGAGCACCTTATCGAACCTC -3';配列番号:10)とGeneRacer 5' Nested プライマーを用いてNested PCRを行った。反応は、98℃を10秒、68℃を30秒、72℃を1分のステップを30サイクル繰り返した。得られた反応産物はpCR4/TOPO10(Invitrogen)にクローニングし、p35FH5'5を得て、p35FH5'5に含まれる5’上流側の配列の塩基配列を決定した(CcF3'5'H 5'RACE配列)。
CcF3'5'H 3'RACE配列とCcF3'5'H 5'RACE配列を基にツユクサF3’5’H遺伝子(CcF3'5'H)の全長のクローニングを行った。前記ツユクサRNAを鋳型にして、プライマーC35FH-7(5'- GAAAACCAATACAAAAACATACC -3';配列番号:11)とプライマーC35FH-10(5'- ATTGCTTCAAGTTCCCTAGC -3';配列番号:12)、そしてReady-To-Go RT-PCR Beads(Amersham Biosciences)を用いて、RT-PCRを行った。反応は、94℃を30秒、54℃を30秒、72℃を2分のステップを30サイクル繰り返した。更に、得られた反応液を鋳型にして、プライマーC35FH-7(配列番号:11)とC35FH-9(5'- GTTCCCTAGCCCCGTACCAC -3';配列番号:13)を用いてSemi Nested PCRを行った。反応は、98℃を10秒、54℃を30秒、72℃を1分のステップを30サイクル繰り返した。得られた反応産物はpCR4/TOPO10(Invitrogen)にクローニングし、p35FH79を得た。次に、p35FH79に含まれる全長のツユクサF3’5’H遺伝子の塩基配列を決定した(CcF3'5'H;配列番号:1)。尚、ツユクサから見出された本配列の遺伝子は新規の遺伝子である。該塩基配列でコードされるアミノ酸配列は、相同性解析よりデルフィニウムのF3'5'H遺伝子がコードするアミノ酸配列(GenBank accession No.:AY856345)と61%の相同性を有する。
実施例3 遺伝子導入用の発現ベクター(pBS-P35T35)の作成
pBS-P35T35はpBluescriptIISK-(Stratagene)内にカリフラワーモザイクウイルス35Sプロモーター(Hohn et al., Curent Topics in Microbiology and Immunology (1982) 96: 194-236.)と、タバコモザイクウイルスのオメガ配列(Gallie et al., Nucleic Acids Research (1987) 15: 3257-3273.)、制限酵素SwaIサイト、そしてカリフラワーモザイクウイルス35Sターミネーターをこの順に有するプラスミドである(図2)。このpBS-P35T35と実質的に機能が同等であるプラスミドは、以下のように構築可能である。
オリゴヌクレオチドSAS-S(5'- CTAGCTAGCGGCGCGCCTGCAGGATATCATTTAAATCCCGGG -3';配列番号:14)とオリゴヌクレオチドSAS-AS(5'- CCCGGGATTTAAATGATATCCTGCAGGCGCGCCGCTAGCTAG -3';配列番号:15)を熱変性後、徐々に室温に戻したものをNheI処理し、pBluescriptIISK-(Stratagene)のXbaI−EcoRVサイトへ連結し、制限酵素サイトを改変したプラスミドDNAであるpBS-SASを作製した。カリフラワーモザイクウイルスのゲノムDNA(GenBank accession V00140)を鋳型として、プライマーT-CaMV35S-SseI-F(5'- AACCTGCAGGAAATCACCAGTCTCTCTCTA-3';配列番号:16)と、プライマーT-CaMV35S-AscI-R(5'- GGCGCGCCATCGATAAGGGGTTATTAG -3';配列番号:17)を用いたPCRによって増幅される領域を制限酵素Sse8387IとAscIによって処理した。この断片をpBS-SASのSse8387I−AscIサイトへ連結し、pBS-T35Sを作製した。pJD301(Leon et al., Plant Physiology (1991) 95: 968-972.)より、HindIIIとHincIIによって切り出されるカリフラワーモザイクウイルス35Sプロモーターとタバコモザイクウイルスのオメガ配列をpBS-T35SのHindIII−SmaIサイトに連結し発現ベクター(pBS-P35T35)を作製した。
実施例4 ツユクサF3'5'H遺伝子の発現ベクターへのサブクローニング
前記CcF3'5'H全長配列を含むプラスミドDNA(p35FH79)を鋳型として、PCRにてツユクサF3'5'H遺伝子のORF部分を増幅し、発現ベクターpBS-P35T35にサブクローニングした。CcF35H-F(5'- ATGGTACCCCTTACGTACCTT -3';配列番号:18)とCcF35H-R(5'- TTATGTTGTTTTTATATTCTTATAAACG -3';配列番号:19)をプライマーとして、p35FH79を鋳型にPCRを行った。反応は、94℃を30秒、52℃を30秒、72℃を1分20秒のステップを25サイクル繰り返した。得られた反応産物をpBS-P35T35のSwaIサイトにクローニングし、p35CcF3'5'Hを得た。p35CcF3'5'Hは、植物細胞内でツユクサF3'5'H遺伝子を発現するDNAである。
実施例5 ツユクサF3'5'H遺伝子の機能発現の確認
赤色のコチョウラン(Dtps. Queen Beer 'Mantenkou')の花弁にp35CcF3'5'H 1.2μgを実施例1の方法で遺伝子導入し5日間培養したところ、花弁に濃い紫の細胞が多数出現した。一方、該遺伝子を含まない金粒子を導入した細胞では、変化は観察されなかった。
以上より、単離したツユクサF3'5'H遺伝子は、コチョウラン花弁細胞にフラボノイド3’,5’−水酸化酵素活性を付与し、その結果、青色色素であるデルフィニジンを産生させたものと考えられる。
実施例6 ツユクサF3'5'H遺伝子の酵素活性評価
ツユクサF3’5’H遺伝子の酵素活性を、青色色素であるデルフィニジン量で評価し、青色カーネーションの作出で有用とされている既知遺伝子(ペチュニア遺伝子)と比較した。
(1)ペチュニアF3'5'H遺伝子(PetF3'5'H)の単離
RNeasy Plant Mini Kit(QIAGEN)を用いて、市販のペチュニア(ハイブリッド)の開花前のツボミの花弁より全RNAを抽出した。このRNAを鋳型として、SuperscriptII First-Strand Synthesis System(Invitrogen)を用いてcDNAを調製した。次にこのcDNAを鋳型としてRT-PCRを行った。PCR反応に用いたプライマーは、既知のペチュニアF3'5'H遺伝子(PetF3'5'H)の二つの配列(GenBank accession No.:A29011、A29013)から設計したPetF3'5'H1-F(5'- ATGATGCTACTTACTGAGCTTGGTG -3';配列番号:20)とPetF3'5'H1-R(5'- CAACATGCGCAATTATAGCA -3';配列番号:21)、若しくはPetF3'5'H2-F(5'- ATGGTGCTACTTAGTGAGCTTGC -3';配列番号:22)とPetF3'5'H2-R(5'- AACCAACGTAAAGGCATGTT -3';配列番号:23)を用いた。反応は二種類とも、94℃を30秒、55℃を30秒、72℃を2.5分のステップを45サイクル繰り返した。得られた反応産物を各々pBS-P35T35のSwaIサイトにクローニングし、p35PetF3'5'H1及びp35PetF3'5'H2を得た。
(2)ツユクサF3'5'H遺伝子並びにペチュニアF3'5'H遺伝子の導入
赤色のコチョウラン(Dtps. Queen Beer 'Mantenkou')の花弁にツユクサ由来の遺伝子p35CcF3'5'H若しくは、ペチュニア由来の遺伝子(p35PetF3'5'H1又はp35PetF3'5'H2)それぞれ1.3μgを実施例1の方法に従い遺伝子導入した。又、遺伝子導入の際、遺伝子導入効率を測るための内部標準としてp35luc(ホタルルシフェラーゼ遺伝子)0.17μgも共導入した。このp35lucは、pSP-luc+(Promega)よりBglII−XbaIで切り出されたルシフェラーゼ遺伝子断片の末端を平滑処理した断片を、別途BamHIとSacIで処理して末端を平滑処理したpBI221(CLONTECH)へサブクローニングし、作製したものである。
遺伝子導入した花弁を5日間静置培養した後、液体窒素中で粉砕し、200μlの0.1×Passive Lysis Buffer(Dual-Luciferase Reporter Assay System、Promega)で懸濁したものを試料として、ルシフェラーゼの活性測定及びアントシアニジンの定量分析を行った。
ルシフェラーゼの活性測定
上記試料20μlに5×Passive Lysis Buffer(Promega)を5μlと100μlのLuciferase Assay Substrate(Promega)を加えた後、ルミノメーターflash'n glow LB955(BERTHOLD TECHNOLOGIES)を用いて、測定時間10秒の条件でルシフェラーゼ活性を測定した。
デルフィニジンの定量
上記試料150μlに2N塩酸を400μl加えた後98℃で2時間加水分解処理を行い、200μlのイソアミルアルコールにて抽出し、有機層を下記条件の液体クロマトグラフィー法でデルフィニジン量を測定した。
使用機器:Waters2690(Waters)、
カラム:Nucleosil 100-5C18 4.6×250mm(GL Sciences)
カラム温度:40℃、
溶出条件:1.5%リン酸水溶液(A液)と1.5%リン酸・20%酢酸・25%アセトニトリル水溶液(B液)を用いて、グラジェント(B液20%→85%を40分、B液85%を5分)をかけ、毎分1mlの流速で溶出した。
検出波長:531nm
標準品(デルフィニジン塩酸塩)を用いた絶対検量線法により、デルフィニジン量を定量した。更に、得られたデルフィニジン量は、ルシフェラーゼ活性を用いて補正した。この結果を表1に示す。表1のようにツユクサF3'5'H遺伝子によるデルフィニジンの蓄積量は、ペチュニアF3'5'H2遺伝子のそれと比較して約5倍程度高かった。又、ペチュニアF3'5'H1遺伝子を用いた試料からは、デルフィニジンが検出されなかった。
【0027】
【表1】

【0028】
実施例7 白色コチョウランの花弁へのF3'5'H遺伝子の導入
青色コチョウランを作出すべく白色のコチョウラン(Phal. amabilis)の花弁へ、実施例6(2)と同様にツユクサ由来の遺伝子(p35CcF3'5'H)あるいはペチュニア由来の遺伝子(p35PetF3'5'H1、p35PetF3'5'H2)それぞれ1.6μgを実施例1の方法に従い遺伝子導入した。しかし、該遺伝子を導入しても明確な花弁の色の変化は認められなかった。
そこで、アントシアニジン生合成経路(図1)においてF3’5’Hより上流にある酵素群((1)カルコン合成酵素:CHS、(2)カルコンイソメラーゼ:CHI及び(3)フラバノン3−水酸化酵素:F3H)をコードする遺伝子を単離し、その導入を試みた。
実施例8 コチョウランCHS遺伝子(PhCHS3)の単離
RNeasy Plant Mini Kit(QIAGEN)を用いて、コチョウラン(Dtps. Sogo Vivien×Dtps. Sogo Yenlin)開花直前の花弁より全RNAを抽出し、このRNAを鋳型として、SuperscriptII First-Strand Synthesis System(Invitrogen)を用いてcDNAを調製した。次にこのcDNAを鋳型としてRT-PCRを行った。PCR反応に用いたプライマーは、既知のコチョウランCHS遺伝子(PhCHS)の配列(GenBank accession No.:DQ089652)から設計したPhCHS3 F1(5'- AAGCTTGTGAGAGACGACGGA -3';配列番号:24)とPhCHS3 R1(5'- TGGCCCTAATCCTTCAAATT -3';配列番号:25)である。反応は、94℃を30秒、55℃を30秒、72℃を1分のステップを25サイクル繰り返した。この反応液を鋳型に再度同条件で反応産物を増幅させた。得られた反応産物はpBS-P35T35のSwaIサイトにクローニングし、p35PhCHS3を得た。次に、p35PhCHS3に含まれるコチョウランCHS遺伝子の全長塩基配列を決定した(PhCHS3、配列番号:26)。p35PhCHS3は、植物細胞内でコチョウランCHS遺伝子を発現するDNAである。
実施例9 コチョウランCHI遺伝子(PhCHI1)の単離
RNeasy Plant Mini Kit(QIAGEN)を用いて、コチョウラン(Dtps. Sogo Vivien×Dtps. Sogo Yenlin)開花直前の花弁より全RNAを抽出し、このRNAを鋳型として、SuperscriptII First-Strand Synthesis System(Invitrogen)を用いてcDNAを調製した。
次にこのcDNAを鋳型としてRT-PCRを行った。CHI遺伝子は、様々な植物で報告があり(GenBank accession No.:AY700850, AY086088, DQ160231, AJ004902, AF474923, XM_470129, U03433, AB187026)、PCR反応に用いたプライマーは既知のCHI遺伝子の配列から設計したCHI-dgF1(5'- TTYCTCGSYGGBGCMGGYGWVMGVGG -3';配列番号:28)とCHI-dgR1(5'- CMGGIGAIACVSCRTKYTYICCRATVAT -3';配列番号:29)を用いた。反応は、94℃を30秒、72℃を1分のステップを5サイクル、94℃を30秒、70℃を1分のステップを5サイクル行った後、94℃を30秒、68℃を30秒、72℃を1分のステップを25サイクル繰り返した。更に、得られた反応液を鋳型にして、プライマーCHI-dgF3(5'- TMIKYWCMGGISMITTYGARAARYT -3';配列番号:30)とプライマーCHI-dgR3(5'- TYICCRATVATIGWHTCCARIAYBGC -3';配列番号:31)を用いてNested PCRを行った。反応は、94℃を30秒、60℃を30秒、72℃を1分のステップを25サイクル繰り返した。得られた反応産物はpCR4-TOPO(Invitrogen)にクローニングし、PhCHIfrag16を得て、PhCHIfrag16に含まれる部分配列の塩基配列を決定した(PhCHI部分配列)。
PhCHI部分配列から3’下流側の配列と5'上流側の配列をRACE法にて解析した。
3’RACE法は、PhCHI部分配列より設計できるプライマーと、上記のRNA、そしてGeneRacer kit(Invitrogen)を用いて行った。PCR反応に用いたプライマーは、PhCHI-GSP F1(5'- ATGCTGCTGCCATTAACGGGTCA -3';配列番号:32)とGeneRacer 3'プライマーである。反応は、94℃を30秒、72℃を1分のステップを5サイクル、94℃を30秒、70℃を1分のステップを5サイクル行った後、94℃を30秒、60℃を30秒、72℃を1分のステップを25サイクル繰り返した。更に、得られた反応液を鋳型にして、プライマーPhCHI-GSP F2(5'- TCCGAGAAGGTCTCCGGGAACT -3';配列番号:33)とGeneRacer 3' Nested プライマーを用いてNested PCRを行った。反応は、94℃を30秒、60℃を30秒、72℃を1分のステップを25サイクル繰り返した。得られた反応産物はpCR4-TOPO(Invitrogen)にクローニングし、PhCHI3'RACE23を得て、PhCHI3'RACE23に含まれる3’下流側の配列の塩基配列を決定した(PhCHI 3'RACE配列)。
5’RACE法は、PhCHI部分配列より設計できるプライマーと、上記のRNA、そしてGeneRacer kit(Invitrogen)を用いて行った。PCR反応に用いたプライマーは、PhCHI-GSP R1(5'- GCATTCGTCAGCTTCTTGCTCTCT -3';配列番号:34)とGeneRacer 5'プライマーである。反応は、94℃を30秒、72℃を1分のステップを5サイクル、94℃を30秒、70℃を1分のステップを5サイクル行った後、94℃を30秒、60℃を30秒、72℃を1分のステップを25サイクル繰り返した。更に、得られた反応液を鋳型にして、プライマーPhCHI-GSP R2(5'- ATCACATCAGTCTCAGCCACA -3';配列番号:35)とGeneRacer 5' Nested プライマーを用いてNested PCRを行った。反応は、94℃を30秒、60℃を30秒、72℃を1分のステップを25サイクル繰り返した。得られた反応産物はpCR4-TOPO(Invitrogen)にクローニングし、PhCHI5'RACE54を得て、PhCHI5'RACE54に含まれる5’上流側の配列の塩基配列を決定した(PhCHI 5'RACE配列)。
PhCHI 3'RACE配列とPhCHI 5'RACE配列を基にコチョウランCHI遺伝子(PhCHI)の全長のクローニングを行った。上記のcDNAと、プライマーPhCHI init(5'- ATGGCAGAAACAGTGGCGACGCCCA -3';配列番号:36)とPhCHI term(5'- TCAAACGACTCCATCTTGCTC -3';配列番号:37)を用いてPCRを行った。反応は、94℃を30秒、65℃を30秒、72℃を1.5分のステップを45サイクル繰り返した。得られた反応産物はpBS-P35T35のSwaIサイトにクローニングし、p35PhCHI1を得た。次に、p35PhCHI1に含まれる全長のコチョウランCHI遺伝子の塩基配列を決定した(PhCHI1、配列番号:38)。尚、コチョウランから見出された本配列の遺伝子は新規の遺伝子である。該塩基配列でコードされるアミノ酸配列は、相同性解析よりチャのCHI遺伝子がコードするアミノ酸配列(GenBank accession No.:DQ120521)と54%の相同性を有する。p35PhCHI1は、植物細胞内でコチョウランCHI遺伝子を発現するDNAである。
実施例10 コチョウランF3H遺伝子(PhF3H1)の単離
RNeasy Plant Mini Kit(QIAGEN)を用いて、コチョウラン(Dtps. Sogo Vivien×Dtps. Sogo Yenlin)開花直前の花弁より全RNAを抽出し、このRNAを鋳型として、SuperscriptII First-Strand Synthesis System(Invitrogen)を用いてcDNAを調製した。
次にこのcDNAを鋳型としてRT-PCRを行った。F3H遺伝子は、様々な植物で報告があり(GenBank accession No.:DQ394303, AY221246, AJ493133, AY641730, AF184270, AB078956, AB201760, AY669324, AF036093, AB211958, AB187027, AB234905)、PCR反応に用いたプライマーは既知のF3H遺伝子の配列から設計したプライマーF3H-dgF1(5'- TIVGIGAYGARGABGARMGBCCIAA -3';配列番号:40)とプライマーF3H-dgR1(5'- ACBGCYYGRTGRTCHGCRTTCTTRAA -3';配列番号:41)を用いた。反応は、94℃を30秒、72℃を1分のステップを5サイクル、94℃を30秒、70℃を1分のステップを5サイクル行った後、94℃を30秒、68℃を30秒、72℃を1分のステップを25サイクル繰り返した。更に、得られた反応液を鋳型にして、プライマーF3H-dgF3(5'- AARYTBRGKTTYGAYATGWCHGGIG -3';配列番号:42)とプライマーF3H-dgR3(5'- GGHWSRACVGTDATCCAIGWBTT -3';配列番号:43)を用いてNested PCRを行った。反応は、94℃を30秒、60℃を30秒、72℃を1分のステップを25サイクル繰り返した。得られた反応産物はpCR4-TOPO(Invitrogen)にクローニングし、PhF3Hfrag26を得て、PhF3Hfrag26に含まれる部分配列の塩基配列を決定した(PhF3H部分配列)。
PhF3H部分配列から3’下流側の配列と5'上流側の配列をRACE法にて解析した。
3’RACE法は、PhF3H部分配列より設計できるプライマーと、上記のRNA、そしてGeneRacer kit(Invitrogen)を用いて行った。PCR反応に用いたプライマーは、PhF3H-GSPF1(5'- TTCTCATACCCAATCGGGAG -3';配列番号:44)とGeneRacer 3'プライマーである。反応は、94℃を30秒、72℃を1分のステップを5サイクル、94℃を30秒、70℃を1分のステップを5サイクル行った後、94℃を30秒、60℃を30秒、72℃を1分のステップを25サイクル繰り返した。得られた反応液と、プライマーPhF3H-GSPF2(5'- AATCGGGAGCCGCGATTACT -3';配列番号:45)とGeneRacer 3' Nested プライマーを用いてNested PCRを行った。反応は、94℃を30秒、60℃を30秒、72℃を1分のステップを25サイクル繰り返した。得られた反応産物はpCR4-TOPO(Invitrogen)にクローニングし、PhF3H3'RACE33を得て、PhF3H3'RACE33に含まれる3’下流側の配列の塩基配列を決定した(PhF3H 3'RACE配列)。
5’RACE法は、PhF3H部分配列より設計できるオリゴヌクレオチドと、上記のRNA、そしてGeneRacer kit(Invitrogen)を用いて行った。PCR反応に用いたプライマーは、PhF3H-GSPR1(5'- TCTGTGTGGCGCTTCAGGCC -3';配列番号:46)とGeneRacer 5'プライマーである。反応は、94℃を30秒、72℃を1分のステップを5サイクル、94℃を30秒、70℃を1分のステップを5サイクル行った後、94℃を30秒、60℃を30秒、72℃を1分のステップを25サイクル繰り返した。得られた反応液と、PhF3H-GSPR2(5'- TGAGGTCCGGTTGCGGGCATTTT -3';配列番号:47)とGeneRacer 5' Nested プライマーを用いてNested PCRを行った。反応は、94℃を30秒、60℃を30秒、72℃を1分のステップを25サイクル繰り返した。得られた反応産物はpCR4-TOPO(Invitrogen)にクローニングし、PhF3H5'RACE86を得て、PhF3H5'RACE86に含まれる5’上流側の配列の塩基配列を決定した(PhF3H 5'RACE配列)。
PhF3H 3'RACE配列とPhF3H 5'RACE配列を基にコチョウランF3H遺伝子の全長のクローニングを行った。上記のcDNAと、プライマーPhF3H init.(5'- ATGGCCCCAATACCATTCCTACCGA -3';配列番号:48)とPhF3H term.(5'- CCTTAAGCTAAAATCTCATTTAATGCCTTTGCTCC -3';配列番号:49)を用いてPCRを行った。反応は、94℃を30秒、65℃を30秒、72℃を1.5分のステップを40サイクル繰り返した。得られた反応産物はpBS-P35T35のSwaIサイトにクローニングし、p35PhF3H1を得た。次に、p35PhF3H1に含まれる全長のコチョウランF3H遺伝子の塩基配列を決定した(PhF3H1、配列番号:50)。尚、コチョウランから見出された本配列の遺伝子は新規の遺伝子である。該塩基配列でコードされるアミノ酸配列は、相同性解析よりBromheadia finlaysonianaのF3H遺伝子がコードするアミノ酸配列(GenBank accession No.:X89199)と86%の相同性を有する。p35PhF3H1は、植物細胞内でコチョウランF3H遺伝子を発現するDNAである。
実施例11 白色コチョウランの花弁へのF3'5'H遺伝子とアントシアニン関連遺伝子の導入
白色のコチョウラン(Phal. amabilis)の花弁へ、コチョウラン由来のCHS遺伝子(p35PhCHS3:実施例8)、CHI遺伝子(p35PhCHI1:実施例9)、F3H遺伝子(p35PhF3H1:実施例10)、そしてツユクサ由来のF3’5’H遺伝子(p35CcF3'5'H:実施例2)を実施例1の方法に従い共導入した。しかし、花弁の色の変化は認められなかった。
そこで、更にアントシアニン生合成経路においてF3'5'Hより下流にある酵素((1)ジヒドロフラボノール4−還元酵素:DFR、(2)アントシアニジン合成酵素:ANS)をコードする遺伝子を単離し、その導入を試みた。
実施例12 コチョウランDFR遺伝子(PhDFR)の単離
RNeasy Plant Mini Kit(QIAGEN)を用いて、コチョウラン(Dtps. Queen Beer 'Mantenkou')のツボミの花弁より全RNAを抽出し、このRNAを鋳型として、GeneRacer kit(Invitrogen)を用いてcDNAを調製した。
次にこのcDNAを鋳型としてRT-PCRを行った。DFR遺伝子は、様々な植物で報告がある(GenBank accession No.:AAB62873, AAC17843, AAD49343, AAQ83576, AAU93766, AAY32600, AAY32601, AAY32602, BAB40789, BAE79202)。PCR反応に用いたプライマーは、前述のDFR遺伝子の配列から設計したDFRD-F1(5'- TTYCAYGTIGCIACNCCNATG -3';配列番号:52)とDFRD-R1(5'- DATNGCRTCRTCRAACATYTC -3';配列番号:53)を用いた。反応は、94℃を30秒、48℃を30秒、72℃を1分のステップを40サイクル繰り返した。得られた反応液を鋳型にして、プライマーDFRD-F2(5'- ATGAAYTTYCARWSIRARGAYCC -3';配列番号:54)とプライマーDFRD-R2(5'- RCAIATRTAICKNCIRTTNGC -3';配列番号:55)を用いてNested PCRを行った。反応は、94℃を30秒、48℃を30秒、72℃を1分のステップを40サイクル繰り返した。更に、得られた反応液を鋳型にして、プライマーDFRD-F3(5'- GARAAYGARGTNATHAARCC -3';配列番号:56)とDFRD-R3(5'- RTCRTCIARRTGNACRAAYTG -3';配列番号:57)を用いて再度Nested PCRを行った。反応は、94℃を30秒、48℃を30秒、72℃を30秒のステップを40サイクル繰り返した。得られた反応産物はpCR4-TOPO(Invitrogen)にクローニングし、PhDFR-D/pCR4を得て、PhDFR-D/pCR4に含まれる部分配列の塩基配列を決定した(PhDFR部分配列)。
PhDFR部分配列から3’下流側の配列と5'上流側の配列をRACE法にて解析した。
3’RACE法は、PhDFR部分配列より設計できるプライマーと、上記のRNA、そしてGeneRacer kit(Invitrogen)を用いて行った。PCR反応に用いたプライマーは、PhDFR-F1(5'- GGTCATGCAAAAGGTCGGGCAGCGTAA -3';配列番号:58)とGeneRacer 3'プライマーである。反応は、94℃を30秒、72℃を1分のステップを5サイクル繰り返し、続いて94℃を30秒、70℃を1分のステップを5サイクル繰り返し、続いて94℃を30秒、68℃を30秒、72℃を1分のステップを25サイクル繰り返した。更に、得られた反応液を鋳型にして、PhDFR-F2(5'- GTGATCTTCACATCTTCCGCAGGAACAGT -3';配列番号:59)とGeneRacer 3' Nested プライマーを用いてNested PCRを行った。反応は、94℃を30秒、65℃を30秒、72℃を1分のステップを25サイクル繰り返した。得られた反応産物はpCR4/TOPO10(Invitrogen)にクローニングし、PhDFR 3'RACE/pCR4を得て、PhDFR 3'RACE/pCR4に含まれる3’下流側の配列の塩基配列を決定した(PhDFR3'RACE配列)。
5’RACE法は、PhDFR部分配列より設計できるプライマーと、上記のRNA、そしてGeneRacer kit(Invitrogen)を用いて行った。PCR反応に用いたプライマーは、PhDFR-R4(5'- ATGATTCATTAAAAATCCGAAAAAAAGACCACTACAA -3';配列番号:60)とGeneRacer 5'プライマーである。反応は、94℃を30秒、72℃を1分のステップを5サイクル繰り返し、続いて94℃を30秒、70℃を1分のステップを5サイクル繰り返し、続いて94℃を30秒、68℃を30秒、72℃を1分のステップを25サイクル繰り返した。更に、得られた反応液を鋳型にして、プライマーPhDFR-R3(5'- AACCATGCATAATAAAGCAGATGTGTAAAT -3';配列番号:61)とGeneRacer 5' Nested プライマーを用いてNested PCRを行った。反応は、94℃を30秒、65℃を30秒、72℃を1分のステップを25サイクル繰り返した。得られた反応産物はpCR4-TOPO(Invitrogen)にクローニングし、PhDFR 5'RACE/pCR4を得、PhDFR 5'RACE/pCR4に含まれる5’上流側の配列の塩基配列を決定した(PhDFR 5'RACE配列)。
PhDFR 3'RACE配列とPhDFR 5'RACE配列を基にコチョウランDFR遺伝子の全長のクローニングを行った。上記のRNAと、プライマーPhDFR-F8A5(5'- AAAAAATGGAGGATGTGAGGAAGGGTCCTGTT -3';配列番号:62)とPhDFR-R5(5'- ACATGATTCATTAAAAATCCGAAAAAAAGACCA -3';配列番号:63)、そしてReady-To-Go You Prime First Strand Beads(Amersham Biosciences社)を用いて、RT-PCRを行った。反応は、98℃を30秒、68℃を30秒、72℃を1.5分のステップを35サイクル繰り返した。得られた反応産物はpBS-P35T35にクローニングし、p35PhDFRを得た。次に、p35PhDFRに含まれる全長のDFR遺伝子の塩基配列を決定した(PhDFR、配列番号:64)。尚、コチョウランから見出された本配列の遺伝子は新規の遺伝子である。該塩基配列でコードされるアミノ酸配列は、相同性解析よりBromheadia finlaysonianaのDFR遺伝子がコードするアミノ酸配列(GenBank accession No.:AF007096)と86%の相同性を有する。p35PhDFRは、植物細胞内でコチョウランDFR遺伝子を発現するDNAである。
実施例13 コチョウランANS遺伝子(PhANS1)の単離
RNeasy Plant Mini Kit(QIAGEN)を用いて、コチョウラン(Dtps.Sogo Vivien×Dtps.Sogo Yenlin)開花直前の花弁より全RNAを抽出し、このRNAを鋳型として、SuperscriptII First-Strand Synthesis System(Invitrogen)を用いてcDNAを調製した。
次にこのcDNAを鋳型としてRT-PCRを行った。PCR反応に用いたプライマーは既知のANS遺伝子の配列から設計したANS-dgF2(5'- TICARGGBTAYGGIAGYARRYTIGCIRMYA -3';配列番号:66)とANS-dgR2(5'- GGYTCRCARAAIAYIRCCCAIGADA -3';配列番号:67)を用いた。反応は、94℃を30秒、60℃を30秒、72℃を1.5分のステップを40サイクル繰り返した。得られた反応液を鋳型に再度同じプライマーを用いて、94℃を30秒、56℃を30秒、72℃を1分のステップ30サイクルの反応を行った。得られた反応産物はpCR4-TOPO(Invitrogen)にクローニングし、PhANSfrag10を得て、PhANSfrag10に含まれる部分配列の塩基配列を決定した(PhANS部分配列)。
PhANS部分配列から3’下流側の配列と5'上流側の配列をRACE法にて解析した。
3’RACE法は、PhANS部分配列より設計できるプライマーと、上記のRNA、そしてGeneRacer kit(Invitrogen)を用いて行った。PCR反応に用いたプライマーは、PhANS3RACEGSP1(5'- GCCCACACCGACGTCAGCTCCCTCTCCT -3';配列番号:68)とGeneRacer 3'プライマーである。反応は、94℃を30秒、72℃を1.5分のステップを5サイクル、94℃を30秒、70℃を1.5分のステップを5サイクル行った後、94℃を30秒、70℃を30秒、72℃を1.5分のステップを25サイクル繰り返した。更に、得られた反応液を鋳型にして、プライマーPhANS3RACEGSP2(5'- CGTCGGGGATGCGCTCGAGATCCTCAGC -3';配列番号:69)とGeneRacer 3' Nested プライマーを用いてNested PCRを行った。反応は、94℃を10秒、58℃を10秒、72℃を1分のステップを35サイクル繰り返した。得られた反応産物はpCR4-TOPO(Invitrogen)にクローニングし、PhANS3'RACE37を得て、PhANS3'RACE37に含まれる3’下流側の配列の塩基配列を決定した(PhANS 3'RACE配列)。
5’RACE法は、PhANS部分配列より設計できるプライマーと、上記のRNA、そしてGeneRacer kit(Invitrogen)を用いて行った。PCR反応に用いたプライマーは、PhANS5RACEGSP1(5'- AGTCCGCGGGTTCAGTCGGCCAGATGGT -3';配列番号:70)とGeneRacer 5'プライマーである。反応は、94℃を30秒、72℃を1.5分のステップを5サイクル、94℃を30秒、70℃を1.5分のステップを5サイクル行った後、94℃を30秒、70℃を30秒、72℃を1.5分のステップを25サイクル繰り返した。得られた反応液と、プライマーPhANS5RACEGSP2(5'- CCGTCTTCTCCGGCGGGTAGACGAGGTG -3';配列番号:71)とGeneRacer 5' Nested プライマーを用いてNested PCRを行った。反応は、94℃を10秒、58℃を10秒、72℃を1分のステップを35サイクル繰り返した。得られた反応産物はpCR4-TOPO(Invitrogen)にクローニングし、PhANS5'RACE15を得て、PhANS5'RACE15に含まれる5’上流側の配列の塩基配列を決定した(PhANS 5'RACE配列)。
PhANS 3'RACE配列とPhANS 5'RACE配列を基にコチョウランANS遺伝子の全長のクローニングを行った。上記のcDNAと、プライマーPhANS init(5'- ATGGCCACCAAAGCAATCCCACC -3';配列番号:72)とPhANS term(5'- TCAATCCACAGGCGCCTTCT -3';配列番号:73)を用いてPCRを行った。反応は、94℃を30秒、69℃を30秒、72℃を1.5分のステップを35サイクル繰り返した。得られた反応産物はpBS-P35T35のSwaIサイトにクローニングし、p35PhANS1を得た。次に、p35PhANS1に含まれる全長のANS遺伝子(PhANS1)の塩基配列を決定した(PhANS1、配列番号:74)。尚、コチョウランから見出された本配列の遺伝子は新規の遺伝子である。該塩基配列でコードされるアミノ酸配列は、相同性解析よりアンスリウムのANS遺伝子がコードするアミノ酸配列(GenBank accession No.:EF079869)と58%の相同性を有する。p35PhANS1は、植物細胞内でコチョウランANS遺伝子を発現するDNAである。
実施例14 白色コチョウランの花弁へのF3'5'H遺伝子とアントシアニジン関連遺伝子の導入
白色のコチョウラン(Phal. amabilis)の花弁へ、ツユクサ由来のF3’5’H遺伝子(CcF3'5'H)とコチョウラン由来のCHS(PhCHS3)、CHI(PhCHI1)、F3H(PhF3H1)、DFR(PhDFR)及びANS(PhANS1)遺伝子を実施例1の方法に従い共導入したところ、花弁に薄い青色の細胞が確認された。
この事より、白色コチョウランの青色への花色改変にはDFR及びANS遺伝子が重要であることが判明した。そこで、更に濃い花色に改変すべく他植物のDFR遺伝子並びにANS遺伝子の探索を行なった。
実施例15 ガーベラのDFR遺伝子およびANS遺伝子の単離とその共導入
(1)ガーベラDFR遺伝子(GerDFR)の単離
RNeasy Plant Mini Kit(QIAGEN)を用いて、市販のガーベラハイブリッドのツボミの花弁より全RNAを抽出し、このRNAを鋳型として、SuperscriptII First-Strand Synthesis System(Invitrogen)を用いてcDNAを調製した。次にこのcDNAを鋳型としてRT-PCRを行った。PCR反応に用いたプライマーは、既知のガーベラDFR遺伝子(GerDFR)の配列(GenBank accession No.:Z17221)から設計したGerDFR-F(5'- ATGGAAGAGGATTCTCCGGC -3';配列番号:76)とGerDFR-R(5'- CTATTGGCCTTCTTTTGAACAACAAA -3';配列番号:77)である。反応は、98℃を10秒、55℃を10秒、72℃を1分30秒のステップを45サイクル繰り返した。得られた反応産物をpBS-P35T35のSwaIサイトにクローニングし、ガーベラDFR遺伝子を得た(p35GerDFR)。p35GerDFRは、植物細胞内でガーベラDFR遺伝子を発現するDNAである。
(2)ガーベラANS遺伝子(GerANS)の単離
上記cDNAを鋳型としてRT-PCRを行った。PCR反応に用いたプライマーは、既知のガーベラANS遺伝子(GerANS)の配列(GenBank accession No.:AY997842)から設計したGerANS-F(5'- ATGGTGATTCAAGCAACCACA -3';配列番号:78)とGerANS-R(5'- CTAGTTTTGCATCACTTCGTCTTTAT -3';配列番号:79)である。反応は、94℃を30秒、56℃を30秒、72℃を1分10秒のステップを45サイクル繰り返した。得られた反応産物をpBS-P35T35のSwaIサイトにクローニングし、ガーベラANS遺伝子を得た(p35GerANS)。p35GerANSは、植物細胞内でガーベラANS遺伝子を発現するDNAである。
(3)ガーベラDFR及びガーベラANS遺伝子の共導入
白色のコチョウラン(Phal. amabilis)の花弁へ、コチョウラン由来のCHS(PhCHS3)、CHI(PhCHI1)、F3H(PhF3H1)の各遺伝子と、ツユクサ由来のF3’5’H遺伝子(CcF3'5'H)、そしてガーベラ由来のDFR遺伝子(GerDFR)並びにANS遺伝子(GerANS)を共導入したところ、花弁に実施例14よりも濃い青紫色の細胞が新たに出現した。
実施例16 トレニアのDFR遺伝子およびANS遺伝子の単離とその共導入
(1)トレニアDFR遺伝子(TorDFR)の単離
RNeasy Plant Mini Kit(QIAGEN)を用いて、市販のトレニア(Torenia fournieri)のツボミの花弁より全RNAを抽出し、SuperscriptII First-Strand Synthesis System(Invitrogen)を用いてcDNAを調製した。このcDNAを鋳型としてRT-PCRを行った。PCR反応に用いたプライマーは、既知のトレニアDFR遺伝子(TorDFR)の配列(GenBank accession AB012924)から設計したオリゴヌクレオチドTorDFR-F(5'- ATGAGCATGGAAGTAGTAGTACCA -3';配列番号:80)とTorDFR-R(5'- CTATTCTATCTTATGTTCTCCATGG -3';配列番号:81)である。反応は、94℃を30秒、56℃を30秒、72℃を1分10秒のステップを45サイクル繰り返した。得られた反応産物をpBS-P35T35のSwaIサイトにクローニングし、トレニアのDFR遺伝子を得た(p35TorDFR)。p35TorDFRは、植物細胞内でトレニアDFR遺伝子を発現するDNAである。
(2)トレニアANS遺伝子(TorANS)の単離
上記cDNAを鋳型として、RT-PCRを行った。PCR反応に用いたプライマーは、既知のトレニアANS遺伝子(TorANS)の配列(GenBank accession AB044091)から設計したTorANS-F(5'- ATGGTTTCTCCAGCATCTCCGA -3';配列番号:82)とTorANS-R(5'- TCACTCAACACTCTTATCATCATGCTC -3';配列番号:83)である。反応は、94℃を30秒、56℃を30秒、72℃を1分10秒のステップを45サイクル繰り返した。得られた反応産物をpBS-P35T35のSwaIサイトにクローニングし、トレニアのANS遺伝子を得た(p35TorANS)。p35TorANSは、植物細胞内でトレニアANS遺伝子を発現するDNAである。
(3)トレニアDFR及びトレニアANS遺伝子の共導入
白色のコチョウラン(Phal. amabilis)の花弁へ、コチョウラン由来のCHS(PhCHS3)、CHI(PhCHI1)及びF3H(PhF3H1)の各遺伝子と、ツユクサ由来のF3’5’H遺伝子(CcF3'5'H)、そしてトレニア由来のDFR遺伝子(TorDFR)並びにANS遺伝子(TorANS)を実施例1の方法に従い共導入したところ、花弁に実施例14よりも濃い青紫色の細胞が新たに出現した。
最良のDFR遺伝子及びANS遺伝子の検討
白色コチョウランの青色への改変に関して、最良のDFR遺伝子及びANS遺伝子を見出すべく植物由来の異なる遺伝子を導入し、比較検討した。
実施例17 花弁細胞の着色の観察
花弁細胞の着色は、実体顕微鏡SZX12(オリンパス)及び肉眼観察により行なった。
花弁の着色程度の基準は、肉眼で確認可能なものを”III”、実体顕微鏡の倍率32倍以下にて確認可能なものを”II”、倍率32倍以上でないと確認できないものを”I”、着色が確認できないものを”−”とした。
実施例18 白色コチョウランの花弁におけるANS遺伝子の比較
白色のコチョウラン(Phal. amabilis)の花弁にANS遺伝子のみ異なる下記三種の遺伝子セットを導入し、着色の程度を観察した。
(1)コチョウランANS遺伝子(PhANS1)+コチョウランCHS遺伝子(PhCHS3)+コチョウランCHI遺伝子(PhCHI1)+コチョウランF3H遺伝子(PhF3H1)+ツユクサF3’5’H遺伝子(CcF3'5'H)+ガーベラDFR遺伝子(GerDFR)
(2)ガーベラANS遺伝子(GerANS)+コチョウランCHS遺伝子(PhCHS3)+コチョウランCHI遺伝子(PhCHI1)+コチョウランF3H遺伝子(PhF3H1)+ツユクサF3’5’H遺伝子(CcF3'5'H)+ガーベラDFR遺伝子(GerDFR)
(3)トレニアANS遺伝子(TorANS)+コチョウランCHS遺伝子(PhCHS3)+コチョウランCHI遺伝子(PhCHI1)+コチョウランF3H遺伝子(PhF3H1)+ツユクサF3’5’H遺伝子(CcF3'5'H)+ガーベラDFR遺伝子(GerDFR)
その結果、それぞれの試料で同程度の青紫色の細胞が出現した。それぞれ22枚の花弁について出現した青紫色の細胞の着色程度を比較した結果を図3に示す。
実施例19 白色コチョウランの花弁におけるDFR遺伝子の比較
白色のコチョウラン(Phal. amabilis)の花弁にDFR遺伝子のみ異なる下記三種の遺伝子セットを導入し、着色の程度を観察した。
(1)コチョウランDFR遺伝子(PhDFR)+コチョウランCHS遺伝子(PhCHS3)+コチョウランCHI遺伝子(PhCHI1)+コチョウランF3H遺伝子(PhF3H1)+ツユクサF3’5’H遺伝子(CcF3'5'H)+トレニアANS遺伝子(TorANS)
(2)ガーベラDFR遺伝子(GerDFR)+コチョウランCHS遺伝子(PhCHS3)+コチョウランCHI遺伝子(PhCHI1)+コチョウランF3H遺伝子(PhF3H1)+ツユクサF3’5’H遺伝子(CcF3'5'H)+トレニアANS遺伝子(TorANS)
(3)トレニアDFR遺伝子(TorDFR) +コチョウランCHS遺伝子(PhCHS3)+コチョウランCHI遺伝子(PhCHI1)+コチョウランF3H遺伝子(PhF3H1)+ツユクサF3’5’H遺伝子(CcF3'5'H)+トレニアANS遺伝子(TorANS)
その結果、それぞれの試料で青紫色の細胞が出現した。それぞれ23枚の花弁の着色の濃さを比較した結果を図4に示すが、PhDFR遺伝子を用いた場合は、GerDFR遺伝子やTorDFR遺伝子を用いた場合と比較して、青紫色の着色程度が低くなっていた。濃い青紫の花色を実現するには、コチョウランの内在DFR遺伝子(PhDFR)よりも、ガーベラのDFR遺伝子(GerDFR)やトレニアのDFR遺伝子(TorDFR)のほうが適していると考えられる。
実施例20 ツユクサF3’5’H遺伝子の有用性
白色コチョウランにおけるツユクサF3’5’H遺伝子の有用性を確認すべくペチュニア遺伝子との比較試験を行なった。
コチョウラン由来のCHS遺伝子(PhCHS3)とCHI遺伝子(PhCHI1)とF3H遺伝子(PhF3H1);ガーベラ由来のDFR遺伝子(GerDFR)とANS遺伝子(GerANS)を導入すると共にツユクサF3’5’H遺伝子((1) CcF3’5’H)又はペチュニアF3’5’H遺伝子((2) PetF3’5’H1、または(3) PetF3’5’H2)をそれぞれ共に白色コチョウラン(Phal. amabilis)の花弁へ共導入した。
その結果、ペチュニアF3'5'H1遺伝子(PetF3’5’H1)またはペチュニアF3'5'H2遺伝子(PetF3’5’H2)を用いた場合では殆ど青色の着色は認められなかったが、ツユクサF3'5'H遺伝子(CcF3’5’H)を用いた場合では明らかな着色が確認できた(図5)。
実施例21 F3H、CHI、CHS遺伝子の遺伝子導入の必要性
白色コチョウランの青色改変における各遺伝子の必要性について検討した。
白色のコチョウラン(Phal. amabilis)の花弁を材料に下記四種の遺伝子セットを導入し、着色の程度を観察した。
(1)ツユクサF3’5’H遺伝子(CcF3'5'H) +トレニアDFR遺伝子(TorDFR)+トレニアANS遺伝子(TorANS)
(2)コチョウランF3H遺伝子(PhF3H1)+ツユクサF3’5’H遺伝子(CcF3'5'H) +トレニアDFR遺伝子(TorDFR)+トレニアANS遺伝子(TorANS)
(3)コチョウランCHI遺伝子(PhCHI1)+コチョウランF3H遺伝子(PhF3H1)+ツユクサF3’5’H遺伝子(CcF3'5'H) +トレニアDFR遺伝子(TorDFR)+トレニアANS遺伝子(TorANS)
(4)コチョウランCHS遺伝子(PhCHS3)+コチョウランCHI遺伝子(PhCHI1)+コチョウランF3H遺伝子(PhF3H1)+ツユクサF3’5’H遺伝子(CcF3'5'H) +トレニアDFR遺伝子(TorDFR)+トレニアANS遺伝子(TorANS)
これらをPhal. amabilisの花弁に遺伝子導入し、細胞の着色を観察したところ、(1)以外の試料で青紫色の細胞が出現した。それぞれ試料18枚の着色の程度を比較した結果を図6に示す。この結果より、F3H遺伝子(PhF3H1)は着色に必須であることが分かった。
実施例22 白色コチョウランの花弁への遺伝子導入により出現した色素の分析
前記実験において白色コチョウラン(Phal. amabilis)の花弁に出現した青紫色の細胞に含まれる色素が、デルフィニジン関連色素であるのか確認を行った。白色コチョウラン(Phal. amabilis)の花弁に、コチョウラン由来のCHI遺伝子とF3H遺伝子とANS遺伝子、及びガーベラ由来のDFR遺伝子とツユクサF3’5’H遺伝子とを共導入し、5日間培養した花弁から実施例6と同様の方法でアントシアニジンを抽出し、分析した。その結果、色素の主成分としてデルフィニジンが検出された。検出されたデルフィニジン量は、一試料あたり16ngであった(5試料の平均)。一方、上記遺伝子セットからツユクサF3’5’H遺伝子を除いた群では、デルフィニジンは検出されなかった。この結果より、白色コチョウランへの遺伝子導入で観察された青紫色の細胞は、デルフィニジン誘導体によって着色したものであった。
実施例23 Phal. amabilis以外の白色コチョウランへの適用
純白色の大型コチョウラン(Phal. White Star)の長さ1.7cmのつぼみの花弁に、コチョウラン由来のCHS遺伝子とCHI遺伝子とF3H遺伝子、及びガーベラ由来のDFR遺伝子とANS遺伝子、とツユクサF3’5’H遺伝子を実施例1の方法に従い共導入したところ、花弁に青紫色の細胞が新たに出現した。
実施例24 アグロバクテリウム法によるコチョウラン形質転換用DNAの作製
遺伝子銃法だけでなく、アグロバクテリウム法を用いてもコチョウランの形質転換は可能である(Belarmino and Mii, Plant Cell Reports (2000) 19:435-442.、Mishiba et al., Plant Cell Reports (2005) 24: 297-303.)。これらの方法に従って遺伝子組換え体を得るために形質転換用DNAの構築を行った。それぞれのプラスミドの地図と作製手順を図7と図8に示す。
(1)pBI-SAS1の構築
PCT/JP02/12268に記載のpBI-RHLをNotIとHindIIIで切断した部位へ、実施例04のpBS-SASをNotIとHindIIIで切断して生じる短い断片をサブクローニングし、pBI-SAS1を構築した。pBI-SAS1は、アグロバクテリウムを用いて植物の形質転換を行い、植物にハイグロマイシン耐性を付与できるプラスミドである。
(2)pBS-35S-FTの構築
コチョウランは花が咲くまでに1年以上の期間を要するため、花芽誘導遺伝子FT (Kobayashi et al., Science (1999) 286: 1960-1962.)をコチョウランで発現させるDNAを構築した。
FTcDNAはシロイヌナズナ全植物体から調整した全RNAからRT-PCRにより増幅して調製した。PCRにはAtFT 2nd-F(5'- GAAACCACCTGTTTGTTCAAGA -3';配列番号:84)とAtFT 2nd-R(5'- TCAATTGGTTATAAAGGAAGAAGC -3';配列番号:85)をプライマーに用い、分離できたFT cDNAをpBS-P35T35をSwaIで切断して生じた部位に挿入して、センス方向にcDNAが挿入されたクローンを選抜し、pBS-P35S-FTを構築した。pBS-35S-FTはCaMV 35Sプロモーター、CaMV 35SターミネーターでFTの転写が制御されるプラスミドである。
(3)pBIH-35S-CcF3’5’Hの構築
p35CcF3’5’HをBamHIで切断後、Klenow断片で突出末端を平滑化し、さらにAscIで切断してプラスミドからDNA断片を切り出した。このDNA断片を、pBI-SAS1をAscIとSwaIで切断して生じた部位に挿入してpBIH-35S-CcF3’5’Hを構築した。pBIH-35S-CcF3’5’Hは選抜マーカーであるHPTとCaMV 35Sプロモーター、CaMV 35Sターミネーターで転写が制御されるCcF3'5'Hが順に連結されたT-DNA領域を持つバイナリーベクターである。
(4)pBS-35S-mPhCHS3の構築
PhCHS3 cDNA内にあるSphI切断部位にアミノ酸置換を伴わない塩基置換を導入して、SphIで切断されないcDNAを作成した。塩基置換はPhCHS3-1038F (5'- GTAACATGTCGAGCGCTTGCGTTCTTTTCATACTCG -3';配列番号:86)とPhCHS3-1073R (5'- CGAGTATGAAAAGAACGCAAGCGCTCGACATGTTAC -3';配列番号:87)をプライマーとして用い、pBS-35S- PhCHS3を鋳型にしてPyrobest(タカラバイオ社製)を用いてDNA合成を行なった。その後、DpnI処理によって鋳型プラスミドを消化し、pBS-35S- mPhCHS3を構築した。
(5)pBS-35S-UP1の構築
p35PhCHI1をAscIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断してプラスミドからDNA断片を切り出した。このDNA断片を、p35PhF3H1をXbaIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断して生じた部位に挿入してpBS-35S-UP1を構築した。pBS-35S-UP1はCaMV 35Sプロモーター、CaMV 35Sターミネーターで転写が制御される各cDNAがPhCHI1、PhF3H1の順に連結されたプラスミドである。
(6)pBS-35S-Del1の構築
p35TorANSをAscIで切断後、Klenow断片で突出末端を平滑化し、さらにKpnIで切断してプラスミドからDNA断片を切り出した。このDNA断片を、p35TorDFRをXbaIで切断後、Klenow断片で突出末端を平滑化し、さらにKpnIで切断して生じた部位に挿入してpBS-35S-Del1を構築した。pBS-35S-Del1はCaMV 35Sプロモーター、CaMV 35Sターミネーターで転写が制御される各cDNAがTorANS、TorDFRの順に連結されたプラスミドである。
(7)pBS-35S-Del2の構築
p35CcF3'5'HをAscIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断してプラスミドからDNA断片を切り出した。このDNA断片を、pBS-35S-Del1をXbaIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断して生じた部位に挿入してpBS-35S-Del2を構築した。pBS-35S-Del2はCaMV 35Sプロモーター、CaMV 35Sターミネーターで転写が制御される各cDNAがCcF3'5'H、TorANS、TorDFRの順に連結されたプラスミドである。
(8)pBS-35S-Del8の構築
pBS-35S-UP1をAscIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断してプラスミドからDNA断片を切り出した。このDNA断片を、pBS-35S-Del2をXbaIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断して生じた部位に挿入してpBS-35S-Del8を構築した。pBS-35S-Del8はCaMV 35Sプロモーター、CaMV 35Sターミネーターで転写が制御される各cDNAがPhCHI1、PhF3H1 、CcF3'5'H、TorANS、TorDFRの順に連結されたプラスミドである。
(9)pBS-35S-Del9の構築
pBS-35S-mPhCHS3をAscIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断してプラスミドからDNA断片を切り出した。このDNA断片を、pBS-35S-Del8をXbaIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断して生じた部位に挿入してpBS-35S-Del9を構築した。pBS-35S-Del9はCaMV 35Sプロモーター、CaMV 35Sターミネーターで転写が制御される各cDNAがmPhCHS3、PhCHI1、PhF3H1、CcF3'5'H、TorANS、TorDFRの順に連結されたプラスミドである。
(10)pBS-35S-Del15の構築
p35CcF3'5'HをAscIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断してプラスミドからDNA断片を切り出した。このDNA断片を、pBS-35S-FTをXbaIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断して生じた部位に挿入してpBS-35S-Del15を構築した。pBS-35S-Del15はCaMV 35Sプロモーター、CaMV 35Sターミネーターで転写が制御される各cDNAがCcF3'5'H、FTの順に連結されたプラスミドである。
(11)pBS-35S-Del16の構築
p35TorDFRをAscIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断してプラスミドからDNA断片を切り出した。このDNA断片を、p35PhANS1をXbaIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断して生じた部位に挿入してpBS-35S-Del16を構築した。pBS-35S-Del16はCaMV 35Sプロモーター、CaMV 35Sターミネーターで転写が制御される各cDNAがTorDFR、PhANS1の順に連結されたプラスミドである。
(12)pBS-35S-UP4の構築
pBS-35S-Del16をAscIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断してプラスミドからDNA断片を切り出した。このDNA断片を、pBS-35S-UP1をXbaIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断して生じた部位に挿入してpBS-35S-UP4を構築した。pBS-35S-UP4はCaMV 35Sプロモーター、CaMV 35Sターミネーターで転写が制御される各cDNAがTorDFR、PhANS1 、PhCHI1、PhF3H1の順に連結されたプラスミドである。
(13)pBS-35S-Del17の構築
p35CcF3'5'HをAscIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断してプラスミドからDNA断片を切り出した。このDNA断片を、pBS-35S-UP4をXbaIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断して生じた部位に挿入してpBS-35S-Del17を構築した。pBS-35S-Del17はCaMV 35Sプロモーター、CaMV 35Sターミネーターで転写が制御される各cDNAがCcF3'5'H、TorDFR、PhANS1 、PhCHI1、PhF3H1の順に連結されたプラスミドである。
(14)pBS-35S-Del18の構築
pBS-35S-Del15をAscIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断してプラスミドからDNA断片を切り出した。このDNA断片を、pBS-35S-UP4をXbaIで切断後、Klenow断片で突出末端を平滑化し、さらにSphIで切断して生じた部位に挿入してpBS-35S-Del18を構築した。pBS-35S-Del18はCaMV 35Sプロモーター、CaMV 35Sターミネーターで転写が制御される各cDNAがCcF3'5'H、FT、TorDFR、PhANS1 、PhCHI1、PhF3H1の順に連結されたプラスミドである。
(15)pBIH-35S-Del8の構築
pBS-35S-Del8をSphIで切断後、Klenow断片で突出末端を平滑化し、さらにAscIで切断してプラスミドからDNA断片を切り出した。このDNA断片を、pBI-SAS1をAscIとSwaIで切断して生じた部位に挿入してpBIH-35S-Del8を構築した。pBIH-35S-Del8は選抜マーカーであるHPTとCaMV 35Sプロモーター、CaMV 35Sターミネーターで転写が制御される各cDNAがPhCHI1、PhF3H1、CcF3'5'H、TorANS、TorDFRの順に連結されたT-DNA領域を持つバイナリーベクターである。
(16)pBIH-35S-Del9の構築
pBS-35S-Del9をSphIで切断後、Klenow断片で突出末端を平滑化し、さらにAscIで切断してプラスミドからDNA断片を切り出した。このDNA断片を、pBI-SAS1をAscIとSwaIで切断して生じた部位に挿入してpBIH-35S-Del9を構築した。pBIH-35S-Del9は選抜マーカーであるHPTとCaMV 35Sプロモーター、CaMV 35Sターミネーターで転写が制御される各cDNAがmPhCHS3、PhCHI1、PhF3H1、CcF3'5'H、TorANS、TorDFRの順に連結されたT-DNA領域を持つバイナリーベクターである。
(17)pBIH-35S-Del17の構築
pBS-35S-Del17をSphIで切断後、Klenow断片で突出末端を平滑化し、さらにAscIで切断してプラスミドからDNA断片を切り出した。このDNA断片を、pBI-SAS1をAscIとSwaIで切断して生じた部位に挿入してpBIH-35S-Del17を構築した。pBIH-35S-Del17は選抜マーカーであるHPTとCaMV 35Sプロモーター、CaMV 35Sターミネーターで転写が制御される各cDNAがCcF3'5'H、TorDFR、PhANS1 、PhCHI1、PhF3H1の順に連結されたT-DNA領域を持つバイナリーベクターである。
(18)pBIH-35S-Del18の構築
pBS-35S-Del18をSphIで切断後、Klenow断片で突出末端を平滑化し、さらにAscIで切断してプラスミドからDNA断片を切り出した。このDNA断片を、pBI-SAS1をAscIとSwaIで切断して生じた部位に挿入してpBIH-35S-Del18を構築した。pBIH-35S-Del18は選抜マーカーであるHPTとCaMV 35Sプロモーター、CaMV 35Sターミネーターで転写が制御される各cDNAがCcF3'5'H、FT、TorDFR、PhANS1 、PhCHI1、PhF3H1の順に連結されたT-DNA領域を持つバイナリーベクターである。
実施例25 形質転換コチョウランの作出
バイナリベクターに構築された実施例24のDNA(pBIH-35S-CcF3’5’H、pBIH-35S-Del8、pBIH-35S-Del9、pBIH-35S-Del17、そしてpBIH-35S-Del18)とアグロバクテリウムEHA101株を用いて作製された形質転換コチョウランは、50mg/mlのハイグロマイシンで選抜される。その結果、実施例24で示した遺伝子が染色体上に組み込まれたコチョウランを得ることができる。
得られた形質転換コチョウランからは、花茎の腋芽など植物体の一部を利用してPLBを誘導し、クローン増殖が可能である。得られた形質転換コチョウランを交配親に用いて、交配育種を行い、導入遺伝子を有する後代を得ることができる。
以上のようにツユクサのF3’5’H遺伝子を用いれば、もともと色のついていたコチョウランからは青味がかった品種が、白色のコチョウランからは青色の品種が新たに作出される。
実施例26 シンビジウム花弁におけるツユクサF3'5'H遺伝子の機能評価
白色シンビジウム(Cym. Lovely Angel 'The Two Virgins')の長さ30mm程度のつぼみから採取した花弁10枚へ、下記3種の遺伝子セットを実施例1の方法に従い、共導入した。
(1)ツユクサF3'5'H遺伝子(CcF3'5'H)+コチョウランCHS遺伝子(PhCHS3)+コチョウランCHI遺伝子(PhCHI1)+コチョウランF3H遺伝子(PhF3H1)+ガーベラDFR遺伝子(GerDFR)+ガーベラANS遺伝子(GerANS)
(2)ペチュニアF3'5'H2遺伝子(PetF3'5'H2)+コチョウランCHS遺伝子(PhCHS3)+コチョウランCHI遺伝子(PhCHI1)+コチョウランF3H遺伝子(PhF3H1)+ガーベラDFR遺伝子(GerDFR)+ガーベラANS遺伝子(GerANS)
(3)コチョウランCHS遺伝子(PhCHS3)+コチョウランCHI遺伝子(PhCHI1)+コチョウランF3H遺伝子(PhF3H1)+ガーベラDFR遺伝子(GerDFR)+ガーベラANS遺伝子(GerANS)
遺伝子導入した花弁を5日間静置培養した後、実体顕微鏡にて観察したところ、ツユクサF3'5'H遺伝子(CcF3'5'H)を含む遺伝子セット(1)を導入した花弁に濃い青紫色の細胞が新たに出現した。一方、ペチュニアF3'5'H2遺伝子(PetF3'5'H2)を含む遺伝子セット(2)を導入した花弁では、一部の花弁で薄い紫色の細胞が観察されるにとどまり、F3’5’H遺伝子を含まない遺伝子セット(3)を導入した花弁では全く花色の変化が認められなかった。図9に実施例17に記載の方法で、それぞれの花弁に出現した青紫色の細胞の着色程度を評価した結果を示す。
【配列表フリーテキスト】
【0029】
SEQ ID NO: 1, Nucleotide sequence encoding Commelina communis flavonoid 3',5'-hydroxylase
SEQ ID NO: 2, Amino acid sequence of Commelina communis flavonoid 3',5'-hydroxylase
SEQ ID NO: 3, Primer 35FH-1
SEQ ID NO: 4, Primer 35FH-4
SEQ ID NO: 5, Primer 35FH-2
SEQ ID NO: 6, Primer 35FH-3
SEQ ID NO: 7, Primer C35FH-3
SEQ ID NO: 8, Primer C35FH-4
SEQ ID NO: 9, Primer C35FH-6
SEQ ID NO: 10, Primer C35FH-5
SEQ ID NO: 11, Primer C35FH-7
SEQ ID NO: 12, Primer C35FH-10
SEQ ID NO: 13, Primer C35FH-9
SEQ ID NO: 14, Oligonucleotide SAS-S
SEQ ID NO: 15, Oligonucleotide SAS-AS
SEQ ID NO: 16, Primer T-CaMV35S-SseI-F
SEQ ID NO: 17, Primer T-CaMV35S-AscI-R
SEQ ID NO: 18, Primer CcF35H-F
SEQ ID NO: 19, Primer CcF35H-R
SEQ ID NO: 20, Primer PetF3'5'H1-F
SEQ ID NO: 21, Primer PetF3'5'H1-R
SEQ ID NO: 22, Primer PetF3'5'H2-F
SEQ ID NO: 23, Primer PetF3'5'H2-R
SEQ ID NO: 24, Primer PhCHS3 F1
SEQ ID NO: 25, Primer PhCHS3 R1
SEQ ID NO: 26, Nucleotide sequence encoding Doritaenopsis hybrid cultivar chalcone synthase
SEQ ID NO: 27, Amino acid sequence of Doritaenopsis hybrid cultivar chalcone synthase
SEQ ID NO: 28, Primer CHI-dgF1
SEQ ID NO: 29, Primer CHI-dgR1
SEQ ID NO: 30, Primer CHI-dgF3
SEQ ID NO: 31, Primer CHI-dgR3
SEQ ID NO: 32, Primer PhCHI-GSP F1
SEQ ID NO: 33, Primer PhCHI-GSP F2
SEQ ID NO: 34, Primer PhCHI-GSP R1
SEQ ID NO: 35, Primer PhCHI-GSP R2
SEQ ID NO: 36, Primer PhCHI init
SEQ ID NO: 37, Primer PhCHI term
SEQ ID NO: 38, Nucleotide sequence encoding Doritaenopsis hybrid cultivar chalcone isomerase
SEQ ID NO: 39, Amino acid sequence of Doritaenopsis hybrid cultivar chalcone isomerase
SEQ ID NO: 40, Primer F3H-dgF1
SEQ ID NO: 41, Primer F3H-dgR1
SEQ ID NO: 42, Primer F3H-dgF3
SEQ ID NO: 43, Primer F3H-dgR3
SEQ ID NO: 44, Primer PhF3H-GSPF1
SEQ ID NO: 45, Primer PhF3H-GSPF2
SEQ ID NO: 46, Primer PhF3H-GSPR1
SEQ ID NO: 47, Primer PhF3H-GSPR2
SEQ ID NO: 48, Primer PhF3H init.
SEQ ID NO: 49, Primer PhF3H term.
SEQ ID NO: 50, Nucleotide sequence encoding Doritaenopsis hybrid cultivar flavanone 3-hydroxylase
SEQ ID NO: 51, Amino acid sequence of Doritaenopsis hybrid cultivar flavanone 3-hydroxylase
SEQ ID NO: 52, Primer DFRD-F1
SEQ ID NO: 53, Primer DFRD-R1
SEQ ID NO: 54, Primer DFRD-F2
SEQ ID NO: 55, Primer DFRD-R2
SEQ ID NO: 56, Primer DFRD-F3
SEQ ID NO: 57, Primer DFRD-R3
SEQ ID NO: 58, Primer PhDFR-F1
SEQ ID NO: 59, Primer PhDFR-F2
SEQ ID NO: 60, Primer PhDFR-R4
SEQ ID NO: 61, Primer PhDFR-R3
SEQ ID NO: 62, Primer PhDFR-F8A5
SEQ ID NO: 63, Primer PhDFR-R5
SEQ ID NO: 64, Nucleotide sequence encoding Doritaenopsis hybrid cultivar dihydroflavonol 4-reductase
SEQ ID NO: 65, Amino acid sequence of Doritaenopsis hybrid cultivar dihydroflavonol 4-reductase
SEQ ID NO: 66, Primer ANS-dgF2
SEQ ID NO: 67, Primer ANS-dgR2
SEQ ID NO: 68, Primer PhANS3RACEGSP1
SEQ ID NO: 69, Primer PhANS3RACEGSP2
SEQ ID NO: 70, Primer PhANS5RACEGSP1
SEQ ID NO: 71, Primer PhANS5RACEGSP2
SEQ ID NO: 72, Primer PhANS init
SEQ ID NO: 73, Primer PhANS term
SEQ ID NO: 74, Nucleotide sequence encoding Doritaenopsis hybrid cultivar anthocyanidin synthase
SEQ ID NO: 75, Amino acid sequence of Doritaenopsis hybrid cultivar anthocyanidin synthase
SEQ ID NO: 76, Primer GerDFR-F
SEQ ID NO: 77, Primer GerDFR-R
SEQ ID NO: 78, Primer GerANS-F
SEQ ID NO: 79, Primer GerANS-R
SEQ ID NO: 80, Primer TorDFR-F
SEQ ID NO: 81, Primer TorDFR-R
SEQ ID NO: 82, Primer TorANS-F
SEQ ID NO: 83, Primer TorANS-R
SEQ ID NO: 84, Primer AtFT 2nd-F
SEQ ID NO: 85, Primer AtFT 2nd-R
SEQ ID NO: 86, Primer PhCHS3-1038F
SEQ ID NO: 87, Primer PhCHS3-1073R
【特許請求の範囲】
【請求項1】
配列番号2で表されるアミノ酸配列又は同アミノ酸配列に対して少なくとも90%の相同性のアミノ酸配列を有するツユクサのフラボノイド3’,5’−水酸化酵素をコードする遺伝子。
【請求項2】
請求項1に記載の遺伝子を含んでなるベクター。
【請求項3】
請求項1に記載の遺伝子を赤い花色のコチョウランに導入し、発現させることを特徴とする青い花色のコチョウランの製造方法。
【請求項4】
請求項3に記載の方法により得られる青い花色のコチョウラン、若しくは改変された花色と同じ性質を有するその子孫またはその組織。
【請求項1】
配列番号2で表されるアミノ酸配列又は同アミノ酸配列に対して少なくとも90%の相同性のアミノ酸配列を有するツユクサのフラボノイド3’,5’−水酸化酵素をコードする遺伝子。
【請求項2】
請求項1に記載の遺伝子を含んでなるベクター。
【請求項3】
請求項1に記載の遺伝子を赤い花色のコチョウランに導入し、発現させることを特徴とする青い花色のコチョウランの製造方法。
【請求項4】
請求項3に記載の方法により得られる青い花色のコチョウラン、若しくは改変された花色と同じ性質を有するその子孫またはその組織。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【公開番号】特開2013−55955(P2013−55955A)
【公開日】平成25年3月28日(2013.3.28)
【国際特許分類】
【出願番号】特願2012−268349(P2012−268349)
【出願日】平成24年12月7日(2012.12.7)
【分割の表示】特願2008−54251(P2008−54251)の分割
【原出願日】平成20年3月5日(2008.3.5)
【出願人】(000000354)石原産業株式会社 (289)
【Fターム(参考)】
【公開日】平成25年3月28日(2013.3.28)
【国際特許分類】
【出願日】平成24年12月7日(2012.12.7)
【分割の表示】特願2008−54251(P2008−54251)の分割
【原出願日】平成20年3月5日(2008.3.5)
【出願人】(000000354)石原産業株式会社 (289)
【Fターム(参考)】
[ Back to top ]

