細菌を検出する方法およびその装置
【課題】迅速、簡便、かつ十分な感度および精度で、試料中の細菌、特に大腸菌および大腸菌群を、酵素活性法によって検出・定量するための方法及び装置を提供する。
【解決手段】被検試料液を、孔径0.6〜5.0μm及び/又は蒸留水通水流量が50〜500mL/min・cm2であるニトロセルロース製濾過膜11に通水して、試料液中の細菌を濾過膜11上に捕集する。捕集された細菌に、溶菌剤と、β−グルクロニダーゼ等の酵素に対する基質液を供給して、酵素基質反応を行わせ、測定装置33で酵素活性値を測定することによって、試料液中の細菌数を定量する方法、ならびに上記の一連の工程を行うための装置。
【解決手段】被検試料液を、孔径0.6〜5.0μm及び/又は蒸留水通水流量が50〜500mL/min・cm2であるニトロセルロース製濾過膜11に通水して、試料液中の細菌を濾過膜11上に捕集する。捕集された細菌に、溶菌剤と、β−グルクロニダーゼ等の酵素に対する基質液を供給して、酵素基質反応を行わせ、測定装置33で酵素活性値を測定することによって、試料液中の細菌数を定量する方法、ならびに上記の一連の工程を行うための装置。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、試料中の細菌を検出・定量する方法及び装置に関する。特に、本発明は、試料水中の大腸菌や大腸菌群などを迅速且つ簡便且つ高感度に検出・定量する方法として有用である。
【背景技術】
【0002】
大腸菌は、糞便性汚染の指標として重要である。また大腸菌群は、糞便性汚染の衛生学的指標として重要であると同時に、消毒効果確認の指標としても用いられている。
大腸菌群(Coliforms)は、グラム陰性、無芽胞の桿菌であり、乳糖ブイヨン−ブリリアントグリーン乳糖胆汁ブイヨン培地法(LB−BGLB法)によって乳糖を分解して酸とガスを生じるか、或いは特定酵素基質培地法によって指定の酵素基質を分解して発色物質を生じる好気性又は嫌気性の細菌と定義されるものであり、Escherichia属、Citrobacter属、Enterobacter属、Klebsiella属から主として構成される。大腸菌群は、病原細菌が存在すると存在する;水界で顕著に増減しない;病原細菌よりも多数存在する;病原細菌よりも消毒剤に対して抵抗性がある;簡単な培地で容易に増殖し、判定が明確にできる;検査すべき試料中にランダムに分布している;培地接種時に他の細菌によって増殖抑制されない;などの特徴を有しているので、古くから糞便性病原細菌(消化器系病原細菌)の汚染指標として広く利用されてきた。しかしながら、大腸菌群は、糞便性病原細菌の他に土壌等の自然由来の細菌も含むため、大腸菌群の検出によっては、温血動物の糞便由来の細菌のみを判別してはいない。
【0003】
大腸菌(Escherichia coli)は、特定酵素基質培地法によってβ−グルクロニダーゼ活性を有すると判定された細菌と定義される。大腸菌は、ヒトや温血動物の腸管内に常在し、糞便由来でない大腸菌群と比べて、糞便汚染の指標として信頼できる。また、単独の菌種であるばかりでなく、他の糞便性指標細菌と比較して、自然界では生存期間が短いため、糞便性汚染のより特異的な指標として用いることができる。
【0004】
また、糞便性大腸菌群(Faecal coliforms)は、大腸菌群にあって、44.5℃で24時間培養したときに、M−FC培地に青色の集落を形成するか、EC培地にガスを生じる細菌と定義されるものであり、Escherichia属、並びに、一部のCitrobacter属、Enterobacter属及びKlebsiella属から主として構成される。糞便汚染のない環境中では、大腸菌群が存在しても糞便性大腸菌群が存在することは少ない。したがって、糞便性大腸菌群は、糞便汚染の指標としては大腸菌よりも信頼性は薄いが、大部分の環境下では、糞便性大腸菌群の濃度が大腸菌の濃度に密接に関連する。このため、糞便性大腸菌群は、糞便汚染の指標として大腸菌群よりも優れていると考えられている。
【0005】
厚生労働省は上水中微生物の基準として大腸菌を採用しており、国土交通省は下水処理場の放流基準値として大腸菌群を採用している。各々の測定対象に応じて検査が義務付けられており、試験方法も定められている。したがって、被検試料の種類に応じて定められた基準に基づいて、試料中の大腸菌数或いは大腸菌群数を測定する必要がある。
【0006】
上記のような試料中の大腸菌或いは大腸菌群の検査において定められている試験方法とは、試料中の細菌を液体培地中あるいは寒天培地上で培養してコロニー数を計数するという検出法である。しかしながらこれらの検出法では、大腸菌数あるいは大腸菌群数の判定に24時間以上を要していた。また、多数の発酵管あるいは培地を調製する必要があり、作業効率が悪かった。
【0007】
試料中の細菌数を判定する方法として、時間の短縮および作業効率の向上を目的としてさまざまな方法が提唱されている。たとえば、大腸菌に特徴的な遺伝子をポリメラーゼ連鎖反応で増幅させた後に検出することによって試料中の大腸菌数を算出する方法(PCR法)や、大腸菌と抗体とを結合させて目印の酵素量を蛍光又は化学発光反応によって測定することによって試料中の大腸菌数を計数する方法(酵素免疫抗体法)などが提案されている。しかしながら、これらの方法は、死菌を生菌と同レベルで扱うため生死の区別が出来ず、したがって測定結果を衛生学的指標として用いることが難しい。また、試料中の細菌を液体培地中あるいは寒天培地上で簡易培養してミクロコロニーを形成して、形成したミクロコロニーを化学発光や蛍光を利用して計数するという方法も提案されている。しかしながらこの方法は、検出可能な大きさまでミクロコロニーを形成させるために4時間以上、前培養する必要がある。更に、デソキシコレート培地のような大腸菌群以外の細菌の生育を抑制する培地の入った密閉容器中に試料を入れて、大腸菌群の呼吸に基づく容器内の酸素又は二酸化炭素の変化を測定することによって大腸菌群の有無を測定する方法(呼吸活性法)も提案されているが、この方法は、菌数に反比例して測定感度が低下するため、低濃度試料の迅速な検出が不可能である。
【0008】
これらの問題を解決する手段として、Fiksdalらにより、試料中の大腸菌数の測定方法として、大腸菌が固有に持つ酵素であるβ−グルクロニダーゼの活性を測定することによって迅速に大腸菌数を算出する方法が提案された(非特許文献1)。この方法は、測定対象の試料に、まず必要に応じて濃縮処理を行い、次に溶菌処理を行って試料中の大腸菌から酵素(β−グルクロニダーゼ)を抽出し、次にこのβ−グルクロニダーゼに対する酵素反応基質を加えることで蛍光などを起こさせてこれを測定することにより試料中の大腸菌数を定量するというものである。このFiksdalらにより提案された方法(酵素活性法)は現在に至るまで様々な改良がなされている(非特許文献2,3)。Rompreらは、PCR法や免疫抗体法等の大腸菌・大腸菌群迅速測定法と比較して、Fiksdalらにより提唱された酵素活性法を「従来法の代替手段として適している」と評価した(非特許文献4)。
【0009】
Fiksdalらによって提唱された酵素活性法を実用化するにあたっての最大の問題点は、検出感度の向上であった。大腸菌群の下水放流基準値は3×103CFU/mLである。一般に、分析方法は、基準値の1/10の測定感度が求められている。また、下水放流水中の大腸菌数は、大腸菌群数の約1/10である。したがって、大腸菌に対しては、3×101CFU/mLの検出感度が求められている。しかし、従来の酵素活性法による大腸菌測定法では、十分な感度が得られなかった。大腸菌のグルクロニダーゼ活性測定用の酵素反応基質として最も広く用いられているのは、蛍光性反応基質である、4−メチルウンベリフェリル−β−D−グルクロニド(MUGlu)である。しかし、MUGluを用いた手法(非特許文献3)では、検出下限値が1×103CFU/mLであり、社会的に求められている検出感度が得られていない。一般的に、蛍光測定よりも発光測定の方が高感度が得られるとされている。そこで、感度を改善するために新規のβ−グルクロニダーゼ向けの発光性酵素反応基質が提案された(特許文献1)。しかし特許文献1で提案された測定法でも、検出下限値が2×105CFU/mLと極めて高く、実用に適さない。更に、ミクロコロニー法における検出下限値をより改善するため、3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−グルクロニド(グルクロン(Glucuron):登録商標(トロピックス社(Tropix,Inc.)))(以下グルクロン(登録商標)と記す)を用いた手法が提案された(特許文献2)。しかしこの手法は、6.5時間の前培養をして菌数を増やす(ミクロコロニーを形成する)必要があり、迅速性に問題があった。
【0010】
また、大腸菌や大腸菌群のような細菌を検出・定量する際に、細菌を含む試料液を濾過膜に通水して細菌を濾過膜上に捕集することにより試料の濃縮を行い、この捕集(濃縮)された細菌に対して分析を行うことによって、分析感度を向上させる試みが行われている。この目的で用いる濾過膜としては、従来は0.2〜0.45μm程度の孔径の濾過膜を用いるのが通常であった(特許文献2、特許文献3)。これは、大腸菌の大きさが通常1〜2μm×0.2〜0.4μm程度であり、上述の範囲の孔径の濾過膜でなければ細菌を高収率で捕集することができないと考えられていたためである。
【0011】
しかしながら、上述の範囲の孔径の濾過膜によって試料水中の細菌を捕集して分析を行った場合、分析結果のバックグラウンド値が高く、検出下限値が高かった。これは、上述の範囲の孔径の濾過膜では、分析対象の細菌に加えて、試料中に含まれている分析に悪影響を与える物質、即ち酵素反応基質と反応して試料の酵素活性測定値に影響を与える夾雑物質(バックグラウンド)も濾過膜上に捕集してしまうためであると考えられる。このため、特に低濃度の大腸菌を含む試料に対しては、この分析手法によって大腸菌の検出・定量を行うことは難しかった。
【0012】
【特許文献1】特開2000−270894
【特許文献2】特表平11−505405
【特許文献3】特開平5−273217
【非特許文献1】Fiksdal, L., Pommepuy, M., Caprais, M.-P., and Midttun, I., Monitoring of fecal pollution in coastal waters by use of rapid enzymatic techniques, Appl. Environ. Microbiol., 60, 1581-1584 (1994)
【非特許文献2】Van Poucke, S.O., and Nelis, H.J., Rapid detection of fluorescent and chemiluminescent total coliforms and Escherichia coli on membrane filters, J. Appl. Microbiol., 42, 233-244 (2000)
【非特許文献3】George, I., Crop, P., and Servais, P., Use of β-D-galactosidase and β-D-gulucuronidase activities for quantitative detection of total and fecal coliforms in wastewater, Can. J. Microbiol., 47, 670-675 (2001)
【非特許文献4】Rompre, A., Servais, P., Baudart, J., de-Roubin, M.-R., and Laurent, P., Detection and enumeration of coliforms in drinking water: current methods and emerging approaches, J. Microbiol. Meth., 49, 31-54 (2002)
【非特許文献5】Bronstein, I., Fortin, J.J., Voyta, J.C., Juo, R.-R., Edwards, B., Olesen, C.E.M., Lijam, N., and Kricka, L.J., Chemiluminescent reporter gene assay: sensitive detection of the GUS and SEAP gene products, BioTechniques, 17, 172-177 (1994)
【発明の開示】
【発明が解決しようとする課題】
【0013】
本発明は、上述の従来技術の問題点を解消し、迅速且つ簡便な方法により高感度で試料中の細菌、特に大腸菌、大腸菌群などを検出及び定量することのできる方法並びに装置を提供することを目的とする。
【課題を解決するための手段】
【0014】
本発明者らは、大腸菌及び大腸菌群などの細菌を濾過膜によって捕集して酵素活性法によって分析(検出・定量)する技術における濾過膜の孔径と検出性能との関係に注目して鋭意研究を行った結果、特定の孔径の濾過膜を用いることで、夾雑物の存在による分析のバックグラウンド値を大幅に小さくすることができ、高感度に細菌の検出及び定量が可能になることを見出し、本発明を完成するに至った。具体的には、本発明者らは、大腸菌などの捕集には、濾過膜の孔径だけではなく濾過膜の吸着性も影響することを見出し、これまでの常識(大腸菌などの捕集には0.2〜0.45μm程度の孔径の濾過膜が最適と考えられていた)に反する孔径0.6〜5.0μm、好ましくは孔径0.8〜3.0μmの吸着性を有する濾過膜が夾雑物を除去し大腸菌だけを選択的に捕集するために最適であることを知見し、本発明を完成するに至ったものである。
【0015】
したがって、本発明によれば、孔径0.6〜5.0μmの濾過膜及び/又はASTM F317-72で測定した場合の蒸留水通水流量が50〜500mL/min・cm2である濾過膜に試料液を通水することによって試料液中の細菌を濾過膜上に捕集し、細菌を捕集した濾過膜を溶菌剤及び酵素反応基質に接触させ、ターゲット細菌中酵素の酵素反応基質に対する酵素活性値を求めことによってる試料液中の細菌数を定量することを特徴とする細菌の検出方法が提供される。酵素活性値は、ターゲット細菌中酵素と酵素反応基質との反応生成物の発光量、蛍光量、発色量などに基づいて求めることができる。濾過膜と溶菌剤及び酵素反応基質との接触は、濾過膜と溶菌剤と酵素反応基質とを同時に接触させても、濾過膜をまず溶菌剤と接触させ、その後、酵素反応基質と接触させてもよい。
【0016】
更に、本発明者らは、上述の特定の濾過膜を用いて細菌を捕集して酵素活性法によって検出・定量を行う際に、細菌を捕集した濾過膜を界面活性剤で通水洗浄することによって分析感度を更に向上させることができることを見出した。
【0017】
即ち、本発明の他の態様は、細菌を捕集した濾過膜に界面活性剤を通水することによって濾過膜を洗浄した後に、濾過膜上に捕集された細菌の酵素活性値を測定することを更なる特徴とする上記記載の試料液中の細菌を検出する方法に関する。
【0018】
更に本発明者らは、酵素反応基質として3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−グルクロニドまたはその誘導体(例えばグルクロン(登録商標)など)を用いてβ−グルクロニダーゼ活性を測定し、測定されたβ−グルクロニダーゼ活性から試料中の大腸菌数及び/又は大腸菌群数及び/又は糞便性大腸菌群数を算出することにより、高感度で大腸菌数及び/又は大腸菌群数及び/又は糞便性大腸菌群数を検出することができることを見出した。本発明方法によるβ−グルクロニダーゼ活性の測定時間は約10分間〜約1時間で、特許文献2で開示されている従来方法での測定時間(6.5時間)を大幅に短縮することができた。また、測定感度(検出下限値)は、大腸菌数で0.1CFU/mL〜2.5×101CFU/mLと非常に高く、特許文献2で開示された方法の検出下限値(1,000CFU/mL)よりも大幅に向上した。
【0019】
即ち、本発明の他の態様は、酵素反応基質として3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−グルクロニドまたはその誘導体(例えばグルクロン(登録商標)など)を用いてβ−グルクロニダーゼ活性を測定することを更なる特徴とする上記記載の試料液中の細菌、特に大腸菌などを検出する方法に関する。
【0020】
更に本発明者らは、β−ガラクトシダーゼに特異的な酵素反応基質、例えば化学発光性酵素反応基質である3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−ガラクトピラノシドまたはその誘導体、特にクロロ誘導体(例えばガラクトン(Galacton):登録商標(トロピックス社(Tropix, Inc.))など)、を用いてβ−ガラクトシダーゼ活性を測定し、測定されたβ−ガラクトシダーゼ活性から試料中の大腸菌群数を算出することにより、高感度で大腸菌群数を検出することができることを見出した。
【0021】
本発明の方法においては、まず被検対象の水試料を、孔径0.6〜5.0μmの濾過膜及び/又はASTM F317-72で測定した場合の蒸留水通水流量が50〜500mL/min・cm2である濾過膜に通水することによって試料液中の細菌、特に大腸菌、大腸菌群及び/又は糞便性大腸菌群を濾過膜上に捕集する。次に、所望の場合には細菌、特に大腸菌、大腸菌群及び/又は糞便性大腸菌群を捕集した濾過膜を界面活性剤で洗浄する。次に、この濾過膜に、溶菌剤と一緒に又は溶菌剤を予め添加した後、測定対象の細菌に特異な酵素(例えば、大腸菌の場合にはβ−グルクロニダーゼ、大腸菌群の場合にはβ−ガラクトシダーゼなど)に対する酵素反応基質を接触させる。これにより、酵素基質反応が起こり、発光性、蛍光性、発色性などの定量測定可能な特性を有する化合物が産生される。そして、発光などを促進させる促進剤を加えて発光などの量を測定することによって、試料の酵素活性値を測定する。一方、被検対象の系において、試料中の測定対象の細菌数(大腸菌、大腸菌群及び/又は糞便性大腸菌群など)と酵素活性値との相関関係を予め求めて検量線を作成しておく。そして、この予め求めておいた細菌数と酵素活性値との相関関係(検量線)に基づいて、測定された酵素活性の測定値から試料中の細菌数を算出する。
【0022】
本発明の方法においては、水試料をそのまま用いても良いが、No.5Aろ紙(有効孔径7μm相当)あるいはこれに相当するフィルターで粗濾過して大きな粒子をあらかじめ除去することが望ましい。フィルターを通す場合は、事前に超音波等の手段を用いて試料を分散させることが望ましく、また通液後に吸引・空洗等の操作で回収率を向上させることが望ましい。
【0023】
必要により粗濾過を行った濾液(水試料)を、孔径0.6〜5.0μmの濾過膜に通水することによって試料液中の細菌を濾過膜上に捕集する。本発明者らの研究により、大腸菌などの細菌を捕集する目的で従来は用いられていなかった孔径(平均孔径)0.6〜5.0μmの濾過膜を用いて大腸菌などを高収率で捕集できることが見出された。本発明においては0.8〜3.0μmの孔径(平均孔径)の濾過膜をこの目的で用いることがより好ましい。なお、濾過膜の孔径(平均孔径)は、製造メーカーから±30%程度の許容範囲で公称値が示されている。濾過膜の材質としては、ニトロセルロース(セルロースナイトレートとセルロースアセテートとの混合物:セルロース混合エステル)製のメンブレンフィルター、セルロースアセテート製のメンブレンフィルター、セラミックフィルター、金属メッシュフィルター、ファブリックフィルターなどを使用することができるが、吸着力の優れているニトロセルロースが最も好ましい。
【0024】
メンブレンフィルターの孔径は、蒸留水通水流量と相関があることが知られており、計測方法も規定されている。本発明では、メンブレンフィルターの製品規格に用いられている試験方法であるASTM F317−72"Standard Test Method for Liquid Flow Rate of Membrane Filters"(孔径が0.10μmのメンブレンフィルターで濾過して粒子を除去した25℃の蒸留水を−0.069MPaの減圧下で濾過し、その流量を1cm2あたり毎分のmL数で表す)で測定した場合に蒸留水通水流量が50〜500mL/min・cm2である濾過膜が適していることを見出した。
【0025】
本発明者らが研究した結果、本発明に従って大腸菌などを高収率で捕集するのに用いることができる濾過膜としては、前述の方法を用いた通水試験ASTM F317-72における蒸留水通水水量が50〜500mL/min・cm2、好ましくは120〜300mL/min・cm2の通水流量を有するものが好適であることが見出された。
【0026】
なお、孔径の大きなメンブレンフィルター(通水流量200mL/min・cm2を超えるもの)を用いる場合には、フィルターを複数枚重ねて使用することによって細菌の捕集効率を向上させることができ、かかる形態も本発明の範囲内に含まれる。
【0027】
なお、厚さの薄いフィルター(厚さ50μm以下、特に10μm以下のもの)を用いる場合には、細菌の回収率が低下するため、孔径の小さなメンブレンフィルターを用いることが好ましい(孔径の大きなメンブレンフィルター(通水流量150mL/min・cm2を超えるもの)は用いないことが好ましい)。
【0028】
次いで、濾過膜を溶菌剤及び酵素反応基質と接触させて、濾過膜上に捕集された細菌(大腸菌及び/又は大腸菌群)から抽出した酵素の活性を測定する。濾過膜と溶菌剤及び酵素反応基質との接触は、濾過膜と溶菌剤と酵素反応基質とを一緒に接触させても、先ず濾過膜に溶菌剤を接触させて酵素を抽出した後に酵素反応基質と接触させてもよい。
本発明においては、濾過膜を溶菌剤及び酵素反応基質と接触させる前に、菌体が溶菌しない濃度の界面活性剤で洗浄することが好ましい。本発明者らの研究により、細菌を捕集した濾過膜を界面活性剤で洗浄することにより、酵素活性法による分析におけるバックグラウンドをより低減させることができ、分析感度を大幅に向上することができることが見出された。この目的で用いることのできる界面活性剤としては、例えば、Triton−X100のような非イオン界面活性剤、ドデシル硫酸ナトリウム(SDS)のような陰イオン界面活性剤などがあり、これらを単独または混合して使用することが好ましい。界面活性剤の濃度は、例えばTriton−X100の場合には、0.01〜0.1vol%であることが好ましい。
【0029】
濾過膜と溶菌剤及び酵素反応基質とを接触させることにより、分析対象の細菌数と相関のある酵素を抽出して特有の酵素反応を起こさせ、酵素反応生成物を指標として酵素活性値を測定することによって細菌を検出・定量することができる。細菌数と相関のある酵素としては、例えば、分析対象の細菌が大腸菌の場合にはβ−グルクロニダーゼ、大腸菌群及び/又は糞便性大腸菌群の場合にはβ−ガラクトシダーゼ及び/又はβ−グルクロニダーゼを用いることができる。
【0030】
溶菌剤としては、菌体を溶菌することができる濃度のTriton−X100のような非イオン界面活性剤やドデシル硫酸ナトリウム(SDS)のような陰イオン界面活性剤を単独または混合して用いることが望ましい。菌体を溶菌することができる界面活性剤の濃度としては、例えば大腸菌及び大腸菌群の場合には0.05〜0.5vol%の範囲を好ましく挙げることができる。溶菌剤として界面活性剤を添加して溶菌する場合には、室温でも良いが、20〜45℃の間の一定温度で溶菌させるのが望ましい。上述のように濾過膜上に細菌を捕捉して、捕捉した細菌に対して酵素活性試験を行う場合、界面活性剤による溶菌処理は、細菌を捕捉した濾過膜を界面活性剤中に浸漬した状態で5〜60分間、好ましくは10〜30分間保持することによって行うことが好ましい。酵素反応基質は、溶菌処理中に溶菌剤と一緒に添加しても、溶菌処理後に別に添加してもよい。
【0031】
また、溶菌剤及び酵素反応基質を添加する前に、超音波破砕を行うこともできる。超音波によって溶菌処理を行う場合には、超音波処理した液に更に界面活性剤を加えた後に酵素反応基質を加えて酵素基質反応を行わせると、菌体残渣が可溶化し、抽出された酵素の分散が進むことでより感度が向上するので好ましい。この場合、超音波処理した液に、酵素を分散でき且つ酵素反応を阻害しない0.01〜0.1%の濃度となるような量の界面活性剤を加えることが好ましい。
【0032】
酵素基質反応(酵素と酵素反応基質との反応)は、緩衝液中で行うことが好ましい。この目的で用いることのできる緩衝液としては、pH6.0〜8.5に調整したリン酸緩衝液あるいはPBS(リン酸緩衝生理食塩水)などを用いることができ、必要に応じて10〜200mMのEDTAと0.02〜2%のBSA(ウシ血清アルブミン)を添加したものも用いることができる。酵素を抽出した試料に、酵素反応基質を混合し、一定温度で5〜60分間反応させることが好ましい。反応温度は20℃〜45℃の間であればいずれも良いが、30℃〜40℃が望ましい。
【0033】
酵素反応基質としては、例えば、分析対象の細菌と相関性のある酵素がβ−グルクロニダーゼである場合、蛍光性酵素反応基質として、4−メチルウンベリフェリル−β−D−グルクロニド、5−ブロモ−4−クロロ−3−インドリル−β−D−グルクロニド、4−トリフロウンベリフェリル−β−D−グルクロニド、化学発光性酵素反応基質として、3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−グルクロニド、グルクロン(登録商標)、D−ルシフェリン−O−β−D−グルクロニド;発色性酵素反応基質として、p−ニトロフェニルグルクロニドなどを用いることができる。また、分析対象の細菌数と相関性のある酵素がβ−ガラクトシダーゼである場合、蛍光性酵素反応基質として、4−メチルウンベリフェリル−β−D−ガラクトピラノシド、4−トリフルオロメチルウンベリフェリル−β−D−ガラクトピラノシド、化学発光性酵素反応基質として3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−ガラクトピラノシドまたはその誘導体、特にクロロ誘導体(ガラクトン(Galacton):登録商標(トロピックス社(Tropix, Inc.)))(以下ガラクトン(登録商標)と記す)、D−ルシフェリン−O−β−D−ガラクトシド;などを用いることができる。
【0034】
濾過膜は酵素反応基質を含む緩衝液(以下、「酵素反応基質液」ともいう)に浸漬させ、一定温度で5〜60分間反応させるが、この際、添加する酵素反応基質液の量は0.1〜5mlが好ましい。この場合、濾過膜よりもわずかに大きな底面積を有する反応容器を用い、容器内に濾過膜を水平に置くことにより、より少量の酵素反応基質液で濾過膜を浸漬させることができるので好ましい。この時、反応温度は20℃〜45℃の間であればいずれでも良いが、30℃〜40℃が望ましく、適度な撹拌を加えることが好ましい。
【0035】
酵素と酵素反応基質との反応によって、発光性、蛍光性或いは発色性の化合物が産生する。反応後、必要に応じて促進剤(発光促進剤、蛍光促進剤、発色促進剤)を加えて、発光などを起こさせてその量を測定する。化学発光を測定する場合、促進剤との混合時間は10秒以内、望ましくは1秒以内とすることが好ましい。促進剤添加から化学発光量などを測定するまでの待ち時間は、1秒〜1分間、望ましくは2秒〜10秒とすることが好ましい。化学発光量などの測定時間は、1秒〜1分間、望ましくは2秒〜10秒間とすることが好ましい。混合時間、待ち時間および測定時間は、サンプル間で常に一定とする。
【0036】
化学発光量の測定は光電子増倍管を用いるフォトンカウンターを用い、酵素反応後の反応液の一部、または全量を発光促進剤と混合して測定することが可能である。この際、酵素反応後の反応液の一部を分取し、発光促進剤を添加してから発光強度を測定することも可能であるが、酵素反応基質液に浸漬した濾過膜に直接発光促進剤を添加し、濾過膜からの発光量を測定することがより望ましい。このとき、測光方向は限定されないが、濾過膜に対向する方向からの測光が望ましい。蛍光や比色強度を利用した方法では、試料液に励起光や透過光を照射する必要があり、反応液中に濾過膜のような光の透過を妨害する固形物を共存させることが出来ないが、化学発光を測定する場合は励起光などを照射する必要がなく、さらに発生する光が濾過膜に反射するため、より効率的に、安定して測定できる。なお、濾過膜は白色のものが好ましいが、非特異的な発光(バックグラウンド)が認められる場合には、黒色の膜を使用することが好ましい。
【0037】
また、本発明者らは、被検試料中のβ−グルクロニダーゼ活性測定値と大腸菌数との相関性に基づいて大腸菌数を測定する酵素活性法において、β−グルクロニダーゼ活性値を測定するための酵素反応基質として、3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−グルクロニド及びその誘導体、例えば、グルクロン(登録商標)などを用いてこれをβ−グルクロニダーゼと反応させて発光性化合物を産生し、産生された発光性化合物を、陽イオン性ポリマーおよびアルカリを含む促進剤を用いて発光させて発光量を定量してβ−グルクロニダーゼ活性を測定し、測定されたβ−グルクロニダーゼ活性から試料中の大腸菌数を算出することにより、高感度で大腸菌数を定量することができることを見出した。なお、大腸菌は大腸菌群やふん便性大腸菌群の中に含まれ、大腸菌群やふん便性大腸菌群中の大腸菌の存在割合は試料の種類によってほぼ一定であることから、大腸菌濃度を測定することで大腸菌群やふん便性大腸菌群数を推定できる。
【0038】
また、本発明者らは、被検試料中のβ−ガラクトシダーゼ活性測定値と大腸菌群数及び/又は糞便性大腸菌群数との相関性に基づいて大腸菌群数及び/又は糞便性大腸菌群数を推定する酵素活性法において、β−ガラクトシダーゼ活性値を測定するための酵素反応基質として、3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−ガラクトピラノシド及びその誘導体、例えばガラクトン(登録商標)などを用いてβ−ガラクトシダーゼと反応させて発光性化合物を産生し、産生された発光性化合物を、陽イオン性ポリマーおよびアルカリを含む発光促進剤、例えばアクセラレータII(商標)を用いて発光させて発光量を定量してβ−ガラクトシダーゼ活性を測定し、測定されたβ−ガラクトシダーゼ活性から高感度で大腸菌群数及び/又は糞便性大腸菌群数を推定することができることを見出した。
【0039】
以上のような3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−グルクロニド及びその誘導体、例えばグルクロン(登録商標)を酵素反応基質として用いてβ−グルクロニダーゼ活性を測定する態様、及び3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−ガラクトピラノシド及びその誘導体、例えばガラクトン(登録商標)を酵素反応基質として用いてβ−ガラクトシダーゼ活性を測定する態様も本発明の範囲内に包含される。即ち、本発明の更に好ましい態様は、上記に説明した酵素活性法による試料中の細菌の検出方法において、
測定対象の細菌が大腸菌であり、大腸菌から抽出されるβ−グルクロニダーゼに対する酵素反応基質として3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−グルクロニド及びその誘導体を用いることを更に特徴とする方法、及び測定対象の細菌が大腸菌群及び/又は糞便性大腸菌群であり、これらから抽出されるβ−ガラクトシダーゼに対する酵素反応基質として3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−ガラクトピラノシド及びその誘導体、例えばガラクトン(登録商標)を用いることを更に特徴とする方法に関する。
【0040】
酵素反応基質として3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−グルクロニド及びその誘導体を用いてβ−グルクロニダーゼ活性を測定する態様又は3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−ガラクトピラノシド及びその誘導体、例えばガラクトン(登録商標)を酵素反応基質として用いてβ−ガラクトシダーゼ活性を測定する態様においては、酵素基質反応の後、発光促進剤を添加して、発光性化合物の化学発光を起こさせ、発光量を測定することが好ましい。かかる態様において用いることのできる発光促進剤としては、陽イオン性ポリマーとアルカリから構成される薬剤ポリ(ビニルベンジルベンジルジメチル)アンモニウムクロライド含有アルカリ溶液を使用することができ、例えばトロピクス(Tropix)社からアクセラレーター2(Accelerator II)として市販されているものを使用することができる。尚、β−ガラクトシダーゼに対する酵素反応基質として3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−ガラクトピラノシドのクロロ誘導体、たとえばガラクトン−スター(登録商標:トロピックス社(Tropix, Inc.))などを用いる場合は、発光促進剤を使用せずに発光量を測定することが可能である。
【0041】
測定された発光量、蛍光量、発色量などから酵素活性値を算出する方法は、当該技術において公知の手法を採用することができる。なお、一般に酵素活性値は、単位時間当たりに生成・増加する反応生成物の量を単位として表す。しかし酵素反応基質として3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−グルクロニド及びその誘導体、例えばグルクロン(登録商標)を用いた場合、反応生成物を直接定量することが困難であることから、単位時間当たりの生成物量で酵素活性値を表すのが極めて難しい。そこで本発明では、反応生成物の量を光量で置き換え、単位時間当たりに増加する光の量で酵素活性値を表す。具体的には、RLU/min(1分間当たりに増加した相対的光量;Relative Light Unit)で表す。以下、単位時間当たりに増加した光量(RLU/min)を、酵素活性値とする。また、同一測定条件下においては、一定時間反応後の発光強度をもって、酵素活性値とすることも可能である。
【0042】
検量線の作成は、測定対象の被検試料と同じ系において、予め種々の所定濃度の細菌試料を用いて、同じ酵素活性測定法により求めたβ−グルクロニダーゼ活性の測定値と、試料中の細菌を液体培地中あるいは寒天培地上で培養してコロニー数を計数することによって求めた菌数との関係をプロットすることによって行うことができる。そして、この検量線に基づいて、上述の酵素活性測定法による未知試料に関する酵素活性の測定値から測定対象の細菌数を定量することができる。
【0043】
以上のように、本発明によれば、孔径0.6〜5.0μmの濾過膜及び/又は蒸留水通水流量が50〜500mL/min・cm2である濾過膜に試料液を通水することによって試料液中の細菌を濾過膜上に捕集し、細菌を捕集した濾過膜を溶菌剤及び酵素反応基質に接触させ、細菌の酵素反応による酵素活性値を測定することによって、夾雑物の存在による分析のバックグラウンド値を大幅に小さくすることができ、試料中の細菌、例えば、大腸菌や大腸菌群を迅速、簡便、且つ高感度で検出・定量することができる。
また、本発明は、上記に説明した試料中の細菌を検出する方法を実施するための装置にも関する。
【0044】
本発明によれば、孔径0.6〜5.0μmの濾過膜及び/又はASTM F317-72で測定した場合の蒸留水通水流量が50〜500mL/min・cm2である濾過膜を収容する捕集容器と、該濾過膜の一次側に試料液を供給する試料液供給機構と、酵素反応基質を供給する酵素反応基質供給機構と、酵素活性値を測定する酵素活性値測定装置と、を含む細菌(好ましくは大腸菌及び/又は大腸菌群)の検出装置が提供される。本発明の細菌の検出装置は、洗浄剤供給機構、溶菌剤供給機構及び/又は促進剤供給機構をさらに具備していてもよい。試料液供給機構及び酵素反応基質供給機構、並びに洗浄剤供給機構、溶菌剤供給機構及び/又は促進剤供給機構は、捕集容器に各流体を必要に応じて供給できるように、好ましくは定量供給できるように、バルブなどを有する配管によって接続されていることが好ましい。また、本発明の細菌の検出装置は、捕集容器とは別に酵素反応を進行させる反応容器を具備していてもよい。あるいは、捕集容器中で酵素反応を進行させてもよい。酵素反応を進行させるには、30℃〜40℃に維持することが必要であるから、恒温槽中に捕集容器及び/又は反応容器を設置することが好ましい。
【0045】
また、本発明によれば、孔径0.6〜5.0μmの濾過膜及び/又はASTM F317-72で測定した場合の蒸留水通水流量が50〜500mL/min・cm2である濾過膜を収容する濾過装置を具備する捕集ユニットと、捕集ユニットから供給される液を受容して酵素基質反応を行う反応ユニットとから構成され、捕集ユニットは、濾過膜の一次側に試料液を供給する試料供給装置、濾過膜の一次側に洗浄液を供給する洗浄液供給装置、細菌を捕集した濾過膜から細菌中の酵素を抽出する手段、抽出処理によって得られる酵素抽出液を反応ユニットに送る手段を具備し、反応ユニットは、捕集ユニットから供給される酵素抽出液に酵素反応基質を供給する酵素反応基質添加装置、酵素反応基質が添加された反応液に促進剤を加える促進剤添加装置、促進剤が加えられた反応液の発光又は蛍光又は発色の量を測定する測定装置を具備する、試料液中の細菌を検出するための装置が提供される。
【0046】
さらに本発明によれば、孔径0.6〜5.0μmの濾過膜及び/又はASTM F317-72で測定した場合の蒸留水通水流量が50〜500mL/min・cm2である濾過膜を収容する濾過装置、濾過膜の一次側に試料液を供給する試料供給装置、濾過膜の一次側に洗浄液を供給する洗浄液供給装置、溶菌酵素反応基質を供給する溶菌酵素反応基質添加装置、濾過膜を浸漬した状態で溶菌酵素反応基質液を一定温度に保持する恒温装置により構成される濾過反応ユニットと、酵素反応後の反応液を測定装置に送る手段を具備し、測定装置に供給する酵素反応後の反応液に促進剤を加える促進剤添加装置、促進剤が加えられた反応液の発光又は蛍光又は発色の量を測定する測定ユニットを具備する、試料液中の細菌(好ましくは大腸菌及び/又は大腸菌群)を検出するための装置が提供される。
【0047】
またさらに、本発明によれば、供給口及び排出口を具備するケーシング内に、孔径0.6〜5.0μmの濾過膜及び/又はASTM F317-72で測定した場合の蒸留水通水流量が50〜500mL/min・cm2である濾過膜を収容する捕集容器と、酵素反応基質液供給ユニットと、酵素活性値を測定する酵素活性値測定装置を含む細菌(好ましくは大腸菌及び/又は大腸菌群)簡易測定キットが提供される。本キットは、洗浄剤供給ユニット、溶菌剤供給ユニット及び/又は促進剤供給ユニットをさらに具備していてもよい。
【好ましい実施形態の説明】
【0048】
以下、本発明の好ましい実施形態を説明する。
本発明の一実施態様は、孔径0.6〜5.0μm及び/又は前述条件下における蒸留水の通水流量50〜500mL/min・cm2の濾過膜を収容し、試料液供給管が濾過膜の一次側に接続されている濾過装置;濾過装置の濾過膜上の捕集物に対して溶菌処理を行う溶菌装置;溶菌処理によって得られる酵素抽出液を受容し、特定の酵素に対する酵素反応基質を酵素抽出液に加えて酵素基質反応を行わせる手段を具備する酵素基質反応装置;酵素反応基質が加えられた反応液に促進剤を加える促進剤添加装置;促進剤が加えられた反応液の発光又は蛍光又は発色の量を測定する測定装置;を具備することを特徴とする試料液中の細菌を検出するための装置である。この実施態様にかかる装置の概念を図1に示す。図1において、試料液1はまず濾過装置2に受容される。濾過装置2は、内部に濾過膜を具備しており、試料液1は濾過膜の一次側に供給されて、濾過膜を通過することによって濾過される。次に、溶菌装置3によって濾過膜上に捕集された物質に溶菌処理が施される。溶菌装置3の具体例としては、濾過膜上の捕集物に超音波を照射する超音波照射装置や、試料液を濾過した濾過膜を界面活性剤中に浸漬して酵素を抽出する装置などを採用することができる。溶菌処理が施された試料は、次に酵素基質反応装置4において、特定の酵素に対する酵素反応基質5が添加され、次に促進剤添加装置6から、酵素基質反応によって産生する発光性、蛍光性又は発色性の化合物の発光、蛍光又は発色を促進する促進剤が添加される。これによって発光などが起こされ、発光などの量を測定装置7によって測定する。このようにして測定された発光量に基づいて、上記に説明した手法によって試料中の特定の細菌を検出・定量することができる。
【0049】
濾過装置2は、試料液を濾過した濾過装置の濾過膜の一次側に界面活性剤洗浄液を供給する濾過膜洗浄液供給装置を更に具備することが好ましい。更に、濾過膜の一次側に濾過膜を空気洗浄するための配管を更に具備することが好ましい。
【0050】
また、本発明方法を実施することのできる装置のより具体的な形態として、本発明の他の態様は、孔径0.6〜5.0μm及び/又は前述条件下における蒸留水の通水流量50〜500mL/min・cm2の濾過膜を収容する濾過装置を具備する捕集ユニットと、捕集ユニットから供給される液を受容して酵素基質反応を行う反応ユニットとから構成され、捕集ユニットは、濾過膜の一次側に試料液を供給する試料供給装置、濾過膜の一次側に洗浄液を供給する洗浄液供給装置、細菌を捕集した濾過膜から細菌中の酵素を抽出する手段、抽出処理によって得られる酵素抽出液を反応ユニットに送る手段を具備し、反応ユニットは、捕集ユニットから供給される酵素抽出液に酵素反応基質を供給する酵素反応基質添加装置、酵素反応基質が供給された反応液に促進剤を加える促進剤添加装置、促進剤が加えられた反応液の発光又は蛍光又は発色の量を測定する測定装置を具備する、試料液中の細菌を検出するための装置に関する。
【0051】
本発明のかかる形態に関する装置の一具体例を図2に示す。図2に示す試料中の細菌を検出するための装置は、試料中の細菌を捕集して溶菌処理を行う捕集ユニット(A)と、捕集ユニット(A)で溶菌処理がされた試料に対して酵素基質反応を行なって発光などの量の定量測定を行う反応ユニット(B)とから構成される。図2においては、反応ユニット(B)として、二種類のタイプが示されている。反応ユニット1では、1検体毎に反応を行うため、検体数が少ない場合に適している。また反応ユニット2では、連続して反応を行うため、連続測定に適している。測定の目的に適した反応ユニットを選択することが可能である。
【0052】
図2において、捕集ユニットAにおける濾過装置17は、内部に、孔径0.6〜5.0μm及び/又は前述条件下での蒸留水の通水流量50〜500mL/min・cm2の濾過膜11と濾過膜の通水量を一定にするための目皿41を収容している。濾過膜11の一次側には、供給配管20が接続され、切り替え弁16を介して、空気供給装置12、試料供給装置13、溶菌剤供給装置14、洗浄液供給装置15が接続されている。また、濾過膜11の下には目皿41、目皿41の二次側には排出管21が接続されている。濾過装置17は、恒温槽18内に配置され、例えば37℃で保持されることが好ましい。
【0053】
まず、試料供給装置13から測定対象の試料液が濾過膜11の一次側に一定流量で供給され、濾過膜を通過することにより濾過される。これにより、試料液中の細菌などは濾過膜11上に捕集される。濾過膜11を通過した液は排出管21を通って、バルブ19を介してドレインとして排出される。次に、切り替え弁16を切り替えて、洗浄液供給装置15から洗浄液を濾過膜11の一次側に供給して、通水洗浄を行うことができる。洗浄液としては、例えば、Triton−Xのような非イオン性界面活性剤が好ましい。濾過膜11を通過した洗浄液は排出管21を通って、バルブ19を介してドレインとして排出される。
【0054】
次に、切り替え弁16を切り替えて、空気供給装置12から空気を吹き込むことができる。これによって、まず、捕集ユニットをパージして、濾過膜上に残った洗浄液を排出管からドレインとして排出することができる。次に、切り替え弁19を切り替えて、空気を反応ユニットBに供給して反応ユニット内をパージすることができる。
【0055】
次に、切り替え弁16を切り替えて、溶菌剤供給装置14から溶菌剤(溶菌液)を濾過装置17に供給する。この際、切り替え弁19を閉止して、濾過装置内に溶菌液を保持して、濾過膜11を溶菌液によって湿潤させた状態で一定時間保持する。次に、切り替え弁19を切り替えて排出管21を反応ユニットBに接続すると共に、切り替え弁16を切り替えて空気供給装置12から空気を吹き込むことによって溶菌処理がされた試料液を反応ユニットBに流す。
【0056】
(b)に示す形態の反応ユニット1は、捕集ユニットAから供給される溶菌処理がされた試料液を受容する反応容器37と、反応容器に酵素反応基質を加える酵素反応基質添加装置31と、反応容器に促進剤を加える促進剤添加装置32、酵素基質反応によって産生する発光性又は蛍光性又は発色性化合物の発光などの量を測定する測定装置33を具備する。反応容器37は、恒温槽39内に配置され、例えば37℃で保持されることが好ましい。
【0057】
捕集ユニットAから供給される溶菌処理がされた試料液は、配管34を通って反応容器37に供給される。次に、酵素反応基質添加装置31から供給管35を通して反応容器37に酵素反応基質が添加される。これによって酵素と基質との反応が行われ、発光性などの特性を有する物質が産生される。図2(b)に示す装置においては、反応容器37には試料送り装置42が配置されており、例えば、一つ目の反応容器37へは酵素反応基質添加から10分後、二つ目の反応容器37へは酵素反応基質添加から15分後、三つ目の反応容器37へは酵素反応基質添加から20分後、というように時間差を付けて測定装置33に送られ、促進剤添加装置32から促進剤が配管36を通して各反応容器に供給される。促進剤を添加して所定時間(例えば2秒)経過後に、産生された物質の発光などの強度を測定装置33、例えばルミノメーターによって測定する。このようにして、幾つかの酵素基質反応時間に対する発光などの強度を測定し、上記に説明した手法によって試料の酵素活性値を算出することができる。
【0058】
(c)に示す形態の反応ユニット2は、捕集ユニットAから供給される溶菌処理がされた試料液を流す配管40と、配管40を流れる溶菌処理がされた試料液に酵素反応基質を加える酵素反応基質添加装置31と、酵素反応基質が加えられた試料液に促進剤を加える促進剤添加装置32と、酵素基質反応によって産生する発光性又は蛍光性又は発色性化合物の発光などの量を測定する測定装置33とを具備する。配管40は、恒温槽39内に配置され、例えば37℃で保持されることが好ましい。
【0059】
捕集ユニットAから供給される溶菌処理がされた試料液は、配管40内を流れ、酵素反応基質添加装置31から酵素反応基質が添加される。これによって酵素と基質との反応が行われ、発光性などの特性を有する物質が産生される。図2(c)に示す装置においては、酵素反応基質添加装置31は、配管の三箇所に接続されており、例えば、酵素反応基質添加装置の一つ目の接続部、二つ目の接続部、及び三つ目の接続部から促進剤添加装置の接続部まで試料液が流れる時間が、それぞれ20分、15分、10分となるように、各接続部の位置及び配管内の試料液の流速を調整する。また、促進剤添加装置32の接続部から測定装置33まで試料液が流れる時間が、例えば2秒となるように、それぞれの位置及び配管内の試料液の流速を調整する。試料液が三つの酵素反応基質添加装置接続部の全てに達した後に、酵素反応基質を三つの接続部に同時に供給する。そして、酵素反応基質の添加後、10分経過後、15分経過後、20分経過後に、促進剤添加装置32から促進剤を添加し、その2秒後に測定装置33によって発光などの強度を測定することによって、酵素基質反応時間が10分、15分、20分の場合の発光などの強度を測定することができ、得られた測定値に基づいて上記に説明した手法によって試料の酵素活性値を算出することができる。
【0060】
また、本発明は、孔径0.6〜5.0μmの濾過膜及び/又はASTM F317-72で測定した場合の蒸留水通水流量が50〜500mL/min・cm2である濾過膜を収容する捕集容器と、該濾過膜の一次側に試料液を供給する試料液供給機構と、酵素反応基質を供給する酵素反応基質供給機構と、酵素活性値を測定する酵素活性値測定装置と、を含む細菌(好ましくは大腸菌及び/又は大腸菌群)の検出装置に係る。この実施態様の概略を図3〜図8に示す。
【0061】
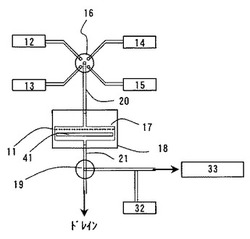
図3において、検出装置は、孔径0.6〜5.0μmの濾過膜及び/又は蒸留水通水流量が50〜500mL/min・cm2である濾過膜11及び濾過膜11の通水量を一定にするための目皿41を収容する捕集容器17と、酵素活性値を測定する酵素活性値測定装置33と、を含む。捕集容器17は、恒温槽18内に配置されており、30℃〜45℃、好ましくは37℃に維持され得る。また、捕集容器17は、捕集された細菌(大腸菌など)と酵素反応基質液及び溶菌剤とを充分に接触させるために撹拌装置又は振動装置(図示せず)などを具備することが好ましい。捕集容器17の濾過膜11の一次側には、捕集容器17の内部をパージするためのパージ用流体(空気、純水など)を供給するパージ用流体供給機構12と、濾過膜11の一次側に被検液を供給する試料液供給機構13と、酵素反応基質及び場合によっては溶菌剤を供給する酵素反応基質供給機構14と、洗浄剤を供給する洗浄剤供給機構15と、が切替弁16を有する配管を介して接続されており、所望量の各液を所望時に供給できるように構成されている。捕集容器17の濾過膜11の二次側には、三方バルブ19を有する配管21が接続されており、濾液や過剰の洗浄剤や溶菌剤などをドレインとして排出し、酵素反応生成物(ジオキセタン誘導体)を含む酵素活性値測定用試料液は酵素活性値測定装置33へ送るように構成されている。配管21には、促進剤供給機構32が接続されており、酵素活性値測定用試料に発光促進剤などを添加してから酵素活性値測定装置33に送ることもできる。酵素活性値測定装置33は、光電子増倍管やフォトダイオードを有するルミノメータやCCDカメラなど公知の発光測定装置でよい。
【0062】
次に、図3に示す検出装置を用いて細菌の検出を行う方法を説明する。まず、被検液を試料液供給機構13から濾過膜11の一次側に一定流量で供給する。被検液は、濾過膜11により濾過され、測定対象の細菌(大腸菌など)は濾過膜11上に捕集され、濾液は、配管21を通ってバルブ19を介してドレインとして排出される。次に、切り替え弁16を切り替えて、洗浄液(例えば、Triton−Xのような非イオン性界面活性剤を含む溶液)を洗浄液供給機構15から濾過膜11の一次側に供給して、通水洗浄を行う。濾過膜11を通過した洗浄液は配管21を通って、バルブ19を介してドレインとして排出される。次に、切り替え弁16を切り替えて、パージ用流体供給機構12からパージ用流体(例えば、空気又は純水)を吹き込み、捕集容器17内部をパージして、濾過膜11上に残った洗浄液を配管21を通してドレインとして排出させる。次に、切替弁16を切り替えて、酵素反応基質供給機構14から酵素反応基質液を捕集容器17に供給する。このとき、酵素反応基質液は、酵素反応基質(例えば、3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−グルクロニドまたはその誘導体)と溶菌剤(例えば、Triton X100などの非イオン系界面活性剤やドデシル硫酸ナトリウムなどの陰イオン界面活性剤)の混合物であることが好ましい。濾過膜11上に捕集された細菌の細胞壁は溶菌剤によって溶かされて酵素が露出する。酵素は酵素反応基質と反応して、発光性などの特性を有する酵素反応生成物(例えば、ジオキセタン誘導体)を産生する。次に、この酵素反応液に、促進剤供給機構32から発光を促進する発光促進剤(例えば、Accelerator II(Tropix社、商標))などを供給して、所定時間(例えば10秒以内)接触させた後、酵素活性値測定用試料液をフォトダイオードや光電子増倍管などを有するルミノメータやCCDカメラなどの酵素活性値測定装置33に送り、ここで発光量などが測定される。発光量などの測定値から、予め作成しておいた検量線を用いて酵素活性値を算出することができる。
【0063】
さて、図4〜図8に本発明の測定装置の数種の変形態様を示す。図4〜図8に示す装置は、基本的に図3に示す装置と同じ構成であり、同じ構成要素には同じ参照符号を付して説明を割愛し、異なる構成について説明する。
【0064】
図4に示す実施態様では、捕集容器17の下流側に反応容器37を設けている。反応容器37は恒温槽(図示せず)内部に設けられており、反応容器37内の温度を30℃〜45℃、好ましくは37℃、に維持することが望ましい。この場合、捕集容器17では酵素反応が十分に進行する必要はないので、捕集容器17を恒温槽18内に位置づけても位置づけなくてもどちらでもよい。反応容器37は、ループ状に形成した配管を恒温槽内に設置したもの用いることができる。反応容器37は、酵素と酵素反応基質との接触を良好にして反応を促進させるために、撹拌装置又は振動装置を具備することが好ましい。パージ用流体供給機構12からパージ用流体(空気が好ましい)を送り、反応容器37から測定対象物質を含む試料流体を測定装置33に送り出してもよい。図4に示す実施態様では、捕集容器17とは別に反応容器37を具備することで、捕集容器17では主として溶菌作用による酵素の抽出を行い、反応容器37では主として酵素と酵素反応基質との反応を進行させることができる。さらに細菌(酵素)と酵素反応基質との接触時間が長くなり反応が進行するため、測定感度がさらに向上するという利点がある。
【0065】
図5に示す実施態様では、反応容器37の下流に、循環ライン50と循環ポンプ51とを位置づけて、測定対象試料となる物質、酵素、酵素反応基質などを含む試料流体を捕集容器17に返送する。試料流体を捕集容器17に再循環させることによって、試料流体の撹拌が行なわれ、濾過膜11上に残留している細菌の溶菌が促進され、酵素、酵素反応基質などを試料流体中に洗い出すことができ、酵素と酵素反応基質との接触時間が長くなり反応が更に進行するので酵素反応生成物の濃度が上昇し、測定感度を向上させることができると共に、添加する酵素反応基質の総量が少量で済むという利点がある。
【0066】
図6に示す実施態様は、捕集容器17を透明樹脂又は透明ガラス製などの光透過性物質で構成し、捕集容器17をそのまま測定セルとして利用する態様である。促進剤供給機構32は、促進剤を濾過膜11の一次側に供給するように捕集容器17の上流に配置されている。また、酵素活性値測定装置33は、捕集容器17の濾過膜11の一次側から発光量を測定するように配置されている。この態様では、濾過膜11の一次側に被検液、溶菌剤及び酵素反応基質を供給して、酵素反応を進行させ、測定対象物質を産生させた後、発光性促進剤などを供給して発光を促進させ、濾過膜11の一次側濾過面を酵素活性値測定装置33で測定する。本実施態様では、捕集容器17において、酵素反応及び酵素活性値測定を行うことができるので、装置構成上及び測定作業上の両面において著しく簡易化できる。
【0067】
図7に示す実施態様は、図6とほぼ同じであるが、捕集容器17の濾過膜11の二次側濾過面を測定するように酵素活性値測定装置33を配置する。酵素反応の際に反応液の循環を行わないタイプの測定装置においては、図9のようにろ過ユニットの一次側に一定の空間を設け、そこに反応基質液を供給して反応ユニットを攪拌しながら溶菌酵素反応を進行させることが好ましい。この場合、反応液や膜と測定装置33との距離が長くなり、発光強度が低くなる。また、酵素反応中に反応液が二次側に漏洩する場合には、一次側の反応液量がばらつき、誤差を生じやすくなる。一方、二次側から測光すると、試料までの距離が短い上、過膜表面を直接測光するため、光が白色のろ紙に反射して高い発光強度が得られる。
【0068】
図8に示す実施態様は、濾過膜11の一次側に被検液及び洗浄液を供給し、二次側に酵素反応基質液及び促進剤を供給(圧入)し、二次側濾過面を測定する態様である。試料液供給機構13及び洗浄液供給機構15を濾過膜11の一次側で捕集容器17に配管20を介して接続し、酵素反応基質液供給機構14及び促進剤供給機構32を濾過膜11の二次側で捕集容器17に配管21(20)を介して接続し、捕集容器17下部に酵素活性値測定装置33を配置する。この実施態様では、配管21は、捕集容器17から被検液及び洗浄液を排出する排出ラインとして作用すると共に、捕集容器17に酵素反応基質液及び促進剤を供給する供給ラインとしても作用する。濾過膜11上には測定対象となる細菌が捕集され、濾過膜11の二次側から供給(圧入)された酵素反応基質液及び促進剤は濾過膜11に浸透し、濾過膜11の一次側まで移動して、濾過膜11上に捕集されている細菌と接触する。
【0069】
図9に、捕集容器17の一具体例を示す。捕集容器17は、恒温槽18内に位置づけられており、捕集容器17を振とうさせる振とう装置22が取り付けられている。捕集容器17内には、濾過膜11及び目皿41が取り付けられている。捕集容器17には、反応液を保持した状態で反応液を混合できるように、一次側に一定の空間を有している。捕集容器17には、液の供給及び排出のための配管が濾過膜11の一次側及び二次側に取り付けられている。図示した具体例では、二次側の配管にバルブ25を取り付け、液の流出を防止している。しかし、図2〜5に示したように、配管に三方バルブなどを取り付ける場合には、バルブ25はなくてもよい。
【0070】
図10に、濾過膜11が脱着可能に取り付けられている捕集容器17を用いる捕集ユニット及び反応・測定ユニットを具備する検査装置の一例を示す。捕集ユニットは、捕集容器17と、配管及び切替弁16を介して捕集容器17に接続されている試料液供給機構13、洗浄液供給機構15及びパージ用流体供給機構12を具備する。捕集容器17は適宜態様で開閉可能に構成されており、濾過膜11を脱着可能に取り付けることができる。反応・測定ユニットは、恒温槽18内に位置づけられている反応容器37と、反応容器37に配管20及び切替弁16を介して接続されている酵素反応基質液供給機構14及び促進剤供給機構32と、反応容器37の底部から測定するように位置づけられている酵素活性値測定装置33を具備する。被検液から細菌捕集後、濾過膜11を捕集容器17から取りだして、反応容器37に移し、酵素反応基質液及び促進剤を供給して、発光性物質の発光量などを酵素活性値測定装置33で測定する。
【0071】
図11に、測定キットの実施態様を示す。測定キットは、孔径0.6〜5.0μmの濾過膜及び/又は蒸留水通水流量が50〜500mL/min・cm2である濾過膜11及び濾過膜11の通水量を一定にするための目皿41を収容する捕集容器17と、酵素反応基質液供給容器15と、洗浄液供給容器14と、促進剤供給容器32を含む。各液の供給容器は、例えば、蓋部分をシリコンゴム性としてシリンジの針を突き刺して液を採取する態様、蓋部分にスポイトを取り付ける態様など液の計量採取に適する構成であることが好ましい。測定キットは、手作業での簡易測定に適している。
【0072】
本発明の実施態様は以下の通りである。
1.試料液を、孔径0.6〜5.0μm及び/又は蒸留水通水流量が50〜500mL/min・cm2である濾過膜に通水することによって試料液中の細菌を濾過膜上に捕集し、濾過膜上に捕集された細菌を溶菌処理にかけることによって酵素を抽出し、抽出液に所定の酵素反応基質を加えて酵素基質反応を行わせて酵素活性値を測定することによって試料液中の細菌数を定量することを特徴とする細菌の検出方法。
2.細菌を捕集した濾過膜に界面活性剤を通水することによって濾過膜を洗浄した後に、濾過膜上に捕集された細菌を溶菌処理にかける上記第1項に記載の方法。
3.試料液を、孔径0.6〜5.0μm及び/又はASTM F317-72で測定した場合の蒸留水通水流量が50〜500mL/min・cm2である濾過膜に通水することによって試料液中の細菌を濾過膜上に捕集し、細菌を捕集した濾過膜を溶菌剤と酵素反応基質を含む液に接触させ、酵素反応を行わせて酵素活性値を測定することによって所定の酵素反応基質を加えて酵素基質反応を行わせて酵素活性値を測定することによって試料液中の細菌数を定量することを特徴とする細菌の検出方法。
4.細菌を捕集した濾過膜に界面活性剤を通水することによって濾過膜を洗浄した後に、濾過膜上に捕集された細菌の酵素活性値を測定する上記第3項に記載の方法。
5.濾過膜に捕集した細菌由来の酵素活性値を発光強度によって測定する細菌の測定方法において、濾過膜を濾過面以上の底面積を有する反応室内で酵素基質液に浸漬して酵素反応を行い、その底面より濾過膜全面からの発光量を測定する上記請求項第3項又は第4項に記載の方法。 6.測定対象の細菌が大腸菌、大腸菌群及び/又は糞便性大腸菌群であり、大腸菌から抽出されるβ−グルクロニダーゼの酵素活性値に基づいて試料液中の大腸菌数を定量する上記第1項〜第5項のいずれかに記載の方法。
7.酵素反応基質として3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−グルクロニド(グルクロン(Glucuron):登録商標)またはその誘導体を用いる、上記第6項に記載の方法。
8.測定対象の細菌が大腸菌群及び/又は糞便性大腸菌群であり、大腸菌群から抽出されるβ−ガラクトシダーゼの酵素活性値に基づいて試料液中の大腸菌群数を定量する上記第1項〜第5項のいずれかに記載の方法。
9.酵素反応基質として3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−ガラクトピラノシド及びその誘導体を用いる、上記第8項に記載の方法。
10.孔径0.6〜5.0μmの濾過膜及び/又は蒸留水通水流量が50〜500mL/min・cm2である濾過膜を収容する濾過装置を具備する捕集ユニットと、捕集ユニットから供給される液を受容して酵素基質反応を行う反応ユニットとから構成され、捕集ユニットは、濾過膜の一次側に試料液を供給する試料供給装置、濾過膜の一次側に洗浄液を供給する洗浄液供給装置、細菌を捕集した濾過膜から細菌中の酵素を抽出する手段、抽出処理によって得られる酵素抽出液を反応ユニットに送る手段を具備し、反応ユニットは、捕集ユニットから供給される酵素抽出液に酵素反応基質を供給する酵素反応基質添加装置、酵素反応基質が添加された反応液に促進剤を加える促進剤添加装置、促進剤が加えられた反応液の発光又は蛍光又は発色の量を測定する測定装置を具備する、試料液中の細菌を検出するための装置。
11.孔径0.6〜5.0μmの濾過膜及び/又は蒸留水通水流量が50〜500mL/min・cm2である濾過膜を収容する濾過装置、濾過膜の一次側に試料液を供給する試料供給装置、濾過膜の一次側に洗浄液を供給する洗浄液供給装置、酵素反応基質を供給する酵素反応基質添加装置、濾過膜を浸漬した状態で酵素反応基質液を一定温度に保持する恒温装置により構成される濾過反応ユニットと、酵素反応後の反応液を測定装置に送る手段を具備し、測定装置に供給する酵素反応後の反応液に促進剤を加える促進剤添加装置、促進剤が加えられた反応液の発光又は蛍光又は発色の量を測定する測定ユニットを具備する、試料液中の細菌を検出するための装置。
【実施例】
【0073】
以下の実施例により本発明を更に具体的に説明する。本発明は以下の記載に限定されるものではない。
【0074】
[実施例1]:大腸菌捕集に用いるメンブレンフィルターの材質および孔径と、大腸菌およびバックグラウンドに影響する夾雑物の捕集効率との関係
本実施例では、市販されている種々の孔径(平均孔径)を有するメンブレンフィルター(ニトロセルロースメンブレンフィルター、セルロースアセテートメンブレンフィルター及びポリカーボネートメンブレンフィルター)を用いて、各種メンブレンフィルターにおける孔径と、細菌捕集効果、酵素活性試験におけるバックグラウンドとの関係を調べた。実験に使用した各種メンブレンフィルターの物性値(メーカーによる公表値)を表1に示す。表1から分かるとおり、メンブレンフィルターの規格は孔径で表しても良いし、蒸留水通水流量で表しても良い。実施例では便宜上、孔径で表すが、これらの数字は、表1を用いて蒸留水通水流量で換算しても良い。
【0075】
【表1】

【0076】
上記の各種メンブレンフィルターの細菌捕集効率を調べた。下水流入水を1/50に希釈して試料を調製し、φ47mmのメンブレンフィルターに通水した。通水量は、孔径0.2μmのフィルターで50mL,0.40〜0.45μmのフィルターで100mL,0.65μm以上のフィルターで200mLとした。ろ過前の試料及びろ液を、コロニー試験にかけ、試料及びろ液中のβ−ガラクトシダーゼ活性を有する細菌(GALase(+)),およびβ−グルクロニダーゼ活性を有する細菌(GLUase(+))を、3M社製ペトリフィルム(登録商標)を用いて計数した。具体的には、「E−coli・大腸菌群数測定用ECプレート」を用いて、試料及びろ液中の細菌を37℃で20時間培養した後、赤色コロニーを形成したものをGALase(+),青色コロニーを形成したものをGLUase(+)として、それぞれ計数した。
【0077】
ろ過前の試料中のGALase(+)は3,600CFU/mL,GLUase(+)は360CFU/mLであった。ろ液中のGALase(+)およびGLUase(+)の計数結果を表2および図12に示した。
【0078】
【表2】

【0079】
膜厚が100μm以上あり、且つ吸着性が低いセルロースアセテートでは、孔径が0.8μmから細菌のリークが始まり、孔径が大きくなるにしたがって細菌捕集効率が低下したが、網目状構造の中に大腸菌が入り込む形で捕集されるため、1μm以上の孔径を用いた場合でも捕集効率が高く、実用可能な範囲であった。
【0080】
膜厚が100μm以上あり、且つ吸着性が高いニトロセルロースでは、孔径が1.0μmから細菌のリークが始まったが、孔径が大きくなっても細菌捕集効率がほとんど低下しなかった。吸着性が高いため、同様の網目状構造を有するセルロースアセテートよりも捕集効率が高くなった。
【0081】
膜厚が10μm以下と薄く、且つ吸着性が低いポリカーボネートでは、孔径が0.8μmから細菌のリークが始まり、1μmになると細菌捕集効率が急激に低下した。これより、大腸菌捕集にポリカーボネートを用いる場合は、0.8μm以下の孔径を用いることが好ましいことが分かった。
【0082】
上記の結果から、孔径(平均孔径)が0.6〜5.0μm、より好ましくは0.8〜3.0μmのメンブレンフィルターを用いることによって、大腸菌などを実用的な範囲で高収率に捕集できることが見出された。
【0083】
また、膜厚が10μm以下のフィルターを用いる場合は、0.8μm以下の孔径であれば大腸菌などを実用的な範囲で高収率に捕集できることが見出された。
【0084】
次に、酵素活性試験のバックグラウンドを高くして定量下限値に悪影響を与える夾雑物を、前述のメンブレンフィルターを用いて排除する実験を行った。大腸菌が含まれていないことを前述のペトリフィルムを用いた測定であらかじめ確認してある環境水を用いて、孔径および材質の差による変化を調べた。上記で用いたニトロセルロースメンブレンフィルター、セルロースアセテートメンブレンフィルター及びポリカーボネートメンブレンフィルター)を用いて試験を行った。
【0085】
β−グルクロニダーゼに対する酵素反応基質溶液としては、グルクロン(登録商標)1vol%,リン酸ナトリウム0.1M,EDTA 10mMの溶液を用いた。
【0086】
大腸菌が含まれていないことを確認済みの環境試料を超音波バスで分散した後、No.5Aろ紙を用いて吸引ろ過した。
得られたろ液を最初に孔径3.0μmのメンブレンフィルターに通液した。次に、フィルターに、50mLの0.02vol%のTriton X−100を含む溶液を通水することによってフィルター洗浄を行った。ろ液と洗液とを合わせて、次に孔径0.8μmのメンブレンフィルターに通液した。次に、フィルターに50mLの0.02vol%のTriton X−100を含む溶液を通水することによってフィルター洗浄を行った。以下、同じ手順で、孔径0.45μm及び0.2μmのメンブレンフィルターによる濾過を行った。
【0087】
各孔径のフィルターの捕集物を、β−グルクロニダーゼ酵素活性試験にかけてβ−グルクロニダーゼ酵素活性値を調べた。
酵素の抽出溶液としてBSAを0.1wt%含むリン酸ナトリウム0.1M溶液にTriton X−100を0.2vol%加えた溶液を用い、上述の0.02vol%Triton X−100溶液による洗浄を行った後の各孔径のフィルターをこの抽出溶液中に浸漬し、37℃で30分間溶菌処理を行った。
【0088】
β−グルクロニダーゼに対する反応基質溶液として、グルクロン(登録商標)1vol%、リン酸ナトリウム0.1M、EDTA 10mMを含む溶液を用い、この反応基質溶液180μLと、上述の溶菌処理で得られた酵素抽出液100μLを混合した。恒温振とう機を用いて37℃で5〜30分間振とうした。振とうを5分間、10分間、15分間及び20分間行った時点でそれぞれ試料を採取し、発光促進剤(トロピクス(Tropix)社:商品名アクセラレーター2(Accelerator II))300μLを添加して、2秒後の発光量を測定した。発光量の測定は、ルミノメータ(ベルトールド社製、LB−9507を用いて行った。
【0089】
各試料における振とう時間(酵素基質反応時間)に対する相対発光量(RLU: Relative Light Unit)をグラフ上にプロットし、求めた直線の傾き(RLU/min)から酵素活性値(β−グルクロニダーゼ活性値)を求めた。
【0090】
本実施例で用いた被検試料は、大腸菌が含まれていないことを確認済みの試料であるので、各試験において測定された酵素活性値は全て酵素活性試験に悪影響を与える夾雑物質によるバックグラウンドであると考えることができる。
【0091】
各種メンブレンフィルター別に、各孔径のフィルターによる捕集物に対して測定されたβ−グルクロニダーゼ酵素活性値(相対バックグラウンド)を図13に示す。濾過前の試料に対して同様の酵素活性試験を行うことによって測定された酵素活性値(バックグラウンド)を100%として、これに対する酵素活性値の相対値を相対バックグラウンドとして示した。
【0092】
いずれのメンブレンフィルターでも、孔径0.4〜0.45μmのフィルターでの試験で50%以上のバックグラウンドが検出された。図13より、孔径0.6μmを下回るメンブレンフィルターでの濾過によって、酵素活性試験に対して悪影響を与える夾雑物質が濾過膜上に捕集されてしまい、バックグラウンドが高くなることが分かる。
【0093】
図13の結果から、夾雑物の影響を排除するには、孔径が0.6μm以上である必要があることが分かった。また図12の結果から、大腸菌を十分な効率で捕集するには、孔径が5.0μm以下、特に3.0μm以下である必要があることが分かった。これらの結果を総合すると、孔径が0.6〜5.0μm、より好ましくは0.8〜3.0μmの濾過膜を用いて試料液の濾過を行って濾過膜上に細菌を捕集し、捕集された細菌に対して酵素活性試験を行うことによって、バックグラウンドの悪影響を排除し且つ実用的な範囲の精度で、試料中の細菌の検出・定量を行うことができることが示される。
【0094】
また、膜厚が10μm以下と薄く、且つ吸着性が低いポリカーボネートでは、大腸菌を高収率で捕集するのに必要な孔径が0.8μm以下であり、且つバックグラウンドが検出される孔径が0.4〜0.45μmであることから、最適な洗浄効果が得られる孔径の範囲が、より厚みのあるニトロセルロースメンブレンフィルターやセルロースアセテートメンブレンフィルターと比較して狭い。これより、大腸菌捕集に用いるフィルターは、10μmを超える厚みがあるものが好ましいことが分かった。
【0095】
[実施例2]:大腸菌の迅速・高感度測定
始めに、β−グルクロニダーゼ活性値を測定するための酵素反応基質として、グルクロン(登録商標)を用いることにより、標準試料を用いた場合の大腸菌測定が迅速・高感度化されることを示す。
【0096】
下水処理場から採取した初沈越流水中の大腸菌数を、培養法(コロニー計数法)で求めた。培地としては、3M社製ペトリフィルム「E−coli・大腸菌群数測定用ECプレート」を用いた。試料を37℃で20時間培養した後、β−グルクロニダーゼに対する特定酵素基質であるX−gluと反応して青色コロニーを形成して且つガス産生の有るものを大腸菌として計数した。この初沈越流水を滅菌希釈水に適宜添加して、1×101〜1×104個/mLの範囲で7検体の標準試料を作成した。初沈越流水中には1×106個/mLの大腸菌が含まれており、これを1×101〜1×104個/mLの範囲になるよう滅菌希釈水で希釈することにより、試料中に共存している夾雑物質の量は1/100以下になり、測定のバックグラウンドに与える影響を排除できる。
【0097】
これらの標準試料を、超音波バスで分散させた後、No.5A濾紙を用いて吸引濾過した。試料に添加・混合した後の濃度が、BSA濃度が0.1wt%、リン酸ナトリウム溶液濃度が0.1M、Triton X−100濃度が0.2vol%となるように調整した濃縮溶菌液を試料に添加して、37℃で30分間溶菌処理を行った。上澄液100μLを採取し、β−グルクロニダーゼに対する酵素反応基質溶液として、グルクロン 1vol%,リン酸ナトリウム0.1M、EDTA 10mMからなる溶液180μLと混合した。恒温振とう機を用いて37℃で振とうした。振とうを5分間、10分間、15分間及び20分間行った時点でそれぞれ試料を採取し、発光促進剤(トロピクス(Tropix)社:商品名アクセラレーター2(Accelerator II))300μLを添加して、2秒後の発光量を測定した。発光量の測定は、ルミノメータ(ベルトールド社製、LB−9507)を用いて行った。各試料における振とう時間(酵素基質反応時間)に対する相対発光量(RLU: Relative Light Unit)をグラフ上にプロットし、求めた直線の傾きを酵素活性値(β−グルクロニダーゼ活性値)とした。図14には、上記のようにして作成した振とう時間(酵素基質反応時間)に対する相対発光量(RLU: Relative Light Unit)のグラフの一例を示す。図14のグラフでは、酵素活性値(直線の傾き)は141.9RLU/minであった。
【0098】
以上の手法によって求められた大腸菌数(コロニー計数値)とβ−グルクロニダーゼ活性値との相関関係を図15に示す。
図15に示したとおり、大腸菌数で2.5×101CFU/mL〜2.5×103CFU/mLの範囲で非常に良好な直線関係が得られた。大腸菌の定量下限値が従来方法(非特許文献3に開示の方法)の1.0×103CFU/mLから40倍向上した。
【0099】
次に、メンブレンフィルターを用いることにより、測定のバックグラウンドに影響を与える夾雑物質が含まれている実試料を用いた場合でも、前述の標準試料と同様の高感度が得られることを示す。
【0100】
下水処理場から採取した初沈越流水,二次処理水,好気性ろ床出口水を、超音波バスで分散した後、No.5Aろ紙を用いて吸引ろ過した。得られたろ液を適宜混合して、大腸菌数=101〜104CFU/mLの範囲で7検体の試料を調製し、試料を二つに分けた。試料の一つは、孔径0.8μmのニトロセルロース製メンブレンフィルターに通液してメンブレン上に大腸菌を捕捉し、メンブレンを実施例1で用いたものと同じ50mLの0.02vol%Triton X−100を含む溶液で洗浄した後、BSAを0.1%含むリン酸ナトリウム0.1M溶液にTriton X−100を0.2vol%加えた溶液中に浸漬して大腸菌を溶菌させた。もう一つの試料液は、メンブレンフィルターへの通液を行わず、BSAを0.1wt%含むリン酸ナトリウム0.1M溶液にTriton X−100を0.2vol%加えた溶液と容積比1:1で混合して、大腸菌を溶菌させて酵素抽出液を得た(従来方法)。それぞれの酵素抽出液に対して、実施例1と同様のβ−グルクロニダーゼ酵素活性試験を行って酵素活性値(RLU/min)を求めると共に、コロニー試験による実際の大腸菌の検出・定量試験を行って、大腸菌数と酵素活性値との相関関係を調べた。結果を図16に示す。
【0101】
従来方法では試料溶液中の大腸菌を直接溶菌していたため、反応溶液に溶解性夾雑物が混入し、バックグランドノイズにより分析精度が低下して検出下限値が高くなった。これに対して、本発明方法によれば、大腸菌をメンブレンフィルター上に捕集し、界面活性剤による洗浄を行った後に、酵素活性試験を行うことにより、夾雑物が排除されて、図16に示すように検出下限値が1桁以上向上した。
【0102】
[実施例3]:界面活性剤洗浄による感度向上
本実施例では、細菌を捕集した濾過膜を界面活性剤で洗浄した後に酵素活性測定を行うことの有利性及びその場合の最適条件を検討する。
【0103】
はじめに、細菌を捕集した界面活性剤を用いて洗浄することによるバックグラウンドの低減効果を確認した。大腸菌が含まれていないことを前述のペトリフィルムを用いた測定であらかじめ確認してある環境水を超音波バスで分散させた後、No.5Aろ紙を用いて吸引ろ過した。ろ液を、孔径0.8μmのニトロセルロースメンブレンフィルターに通液した。同様の方法で、6検体試料を調製した。通液後のメンブレンフィルターに、Triton X−100を各々0vol%、0.005vol%、0.01vol%、0.02vol%、0.05vol%、0.1vol%含む溶液(洗浄液)を通液してフィルターを洗浄した後、フィルターの残留物に対して実施例1と同様の手順によってβ−グルクロニダーゼ酵素活性値(バックグランド)を求めた。結果を図17に示す。
【0104】
次に、界面活性剤を用いて洗浄することによる大腸菌の損失を調べた。下水処理場の初沈越流水から高濃度大腸菌を含む試料を採取し、滅菌希釈水で希釈することにより、大腸菌標準試料を作成した。この試料を超音波バスで分散させた後、No.5Aろ紙を用いて吸引ろ過した。ろ液を孔径0.8μmニトロセルロースメンブレンフィルターに通液して大腸菌を捕集した。同様の方法で、5検体試料を調製した。大腸菌が捕集されたメンブレンを、Triton X−100を各々0vol%、0.02vol%、0.05vol%、0.1vol%、0.2vol%含む溶液に含浸させ、含浸させた状態で5分間放置した後、実施例1と同様の手順によってこの浸漬液のβ−グルクロニダーゼ酵素活性値(大腸菌酵素活性値)を求めた。この酵素活性値を、洗浄によって損失する可能性のある大腸菌の量として評価した。結果を同様に図17に示す。
【0105】
図18より、十分なバックグラウンド低減効果を得るには、Triton X−100濃度を0.01vol%以上にする必要があった。一方、Triton X−100濃度が0.1vol%以上になると、損失する可能性のある大腸菌が増加した。したがって最適洗浄条件が得られる洗浄液のTriton X−100濃度は、0.01〜0.1vol%であることが分かる。
【0106】
[実施例4]:超音波を用いた溶菌処理
本発明において、大腸菌からβ−グルクロニダーゼを抽出する操作(溶菌処理)は、界面活性剤を用いても良いし、超音波を用いても良い。超音波を用いる場合でも、感度向上のため、反応液に界面活性剤を添加することが好ましい。
【0107】
下水処理場から採取した二次処理水を、超音波バスで分散させた後、No.5Aろ紙を用いて吸引ろ過した。ろ液を0.8μmメンブレンに通液し、大腸菌を捕集した。大腸菌が捕集されたメンブレンを、AMP=100watt、Pulse=1sec、Timer=1minの条件で超音波破砕し、β−グルクロニダーゼを抽出した(溶菌処理)。上澄液100μLを採取し、界面活性剤であるTriton X−100が最終濃度で各々0vol%、0.025vol%、0.5vol%、0.1vol%、0.3vol%、および0.5vol%となるように添加した後、実施例1と同じ酵素反応基質溶液180μLと混合した。実施例2と同様の手法により、恒温振とう機を用いて37℃で所定時間振とうさせた後に発光促進剤300μLを添加して発光を起こさせ発光量を測定して酵素活性値を求めた。界面活性剤濃度と酵素活性値の関係を図18に示した。
【0108】
超音波破砕によって溶菌処理を行い、酵素活性値を求める場合には、超音波処理後の試料に界面活性剤を添加することにより、添加しないときと比較して、最大で60%感度を向上させることができることが示される。また、この目的で界面活性剤を加える場合には、添加量としては、液中の界面活性剤濃度が0.01〜0.1vol%となるような量を加えることが好ましいことが分かる。
【0109】
[実施例5]:界面活性剤を用いて溶菌する際の最適条件:溶菌時間
界面活性剤を用いてグルクロニダーゼを抽出する(溶菌処理)場合は、一定の溶菌時間が必要である。
【0110】
下水処理場から採取した二次処理水を、超音波バスで分散させた後、No.5Aろ紙を用いて吸引ろ過した。ろ液を0.8μmメンブレンに通液し、大腸菌を捕集した。酵素の抽出溶液として、BSAを0.1wt%含むリン酸ナトリウム0.1M溶液にTriton X−100を0.1vol%加えた溶液を用い、大腸菌が捕集されたメンブレンをこの抽出溶液に浸漬して、37℃で0.5分間、5分間、10分間、15分間および30分間溶菌処理を行った。上澄液100μLを採取し、上述の酵素反応基質溶液180μLと混合した。実施例2と同様の手法により、恒温振とう機を用いて37℃で所定時間振とうさせた後に発光促進剤300μLを添加して発光を起こさせ発光量を測定して酵素活性値を求めた。溶菌時間と酵素活性値の関係を図19に示した。
【0111】
特許文献1で開示されている従来法では、界面活性剤と酵素反応基質を被検試料に同時に添加していた。この方法では、溶菌反応が十分に進まない状態で酵素反応を開始するため、抽出された酵素量と基質濃度のばらつきが大きくなり、十分な分析精度が得られなかった。本発明方法においては、大腸菌を十分に溶菌させた後に酵素反応基質を添加することで反応条件が一定になり、分析精度が大幅に向上した。
【0112】
[実施例6]:界面活性剤を用いて溶菌する際の最適条件:界面活性剤濃度
界面活性剤によって溶菌してグルクロニダーゼを抽出する場合は、Triton X−100の濃度を高くすることが好ましい。本実施例では、界面活性剤による溶菌効率と酵素反応阻害との関係を調べた。
【0113】
下水処理場から採取した二次処理水を、超音波バスで分散させた後、No.5Aろ紙を用いて吸引ろ過した。ろ液を0.8μmメンブレンに通液し、大腸菌を捕集した。酵素の抽出溶液として、BSAを0.1wt%含むリン酸ナトリウム0.1M溶液にTriton X−100を各々0vol%、0.025vol%、0.5vol%、0.1vol%、0.3vol%および0.5vol%加えた溶液を用い、大腸菌が捕集されたメンブレンをこの抽出溶液に浸漬し、37℃で30分間溶菌処理を行った。上澄液100μLを採取し、上述の酵素反応基質溶液180μLと混合した。実施例2と同様の手法により、恒温振とう機を用いて37℃で所定時間振とうさせた後に発光促進剤300μLを添加して発光を起こさせ発光量を測定して酵素活性値を求めた。Triton X−100濃度と酵素活性値の関係を図20に示す。溶菌効率と酵素反応阻害の関係から、最も高い酵素活性値が得られる最適Triton X−100の濃度は、0.2vol%前後であることが分かった。特許文献1に開示されている従来法では、界面活性剤としてTriton X−100を用いる場合は、濃度0.1vol%とされている。図20の結果から、Triton X−100の濃度を0.2vol%にしたことにより、感度が約2倍に向上したことが分かる。また、図20より好ましい溶菌剤としての界面活性剤濃度は0.15〜0.5vol%であることが分かる。
【0114】
[実施例7]
本実施例では、酵素反応基質と一緒に添加する場合の溶菌剤としての界面活性剤濃度の影響を調べた。
純水で10倍稀釈した下水10mLを、超音波バスで分散させた後、No.5Aろ紙を用いて吸引ろ過した。ろ液を0.8μmメンブレンに通液し、大腸菌を捕集した。そして、0.04vol%のTriton X-100を含む滅菌希釈水(栄研化学)10mLで2回を吸引濾過することにより、フィルターを洗浄した。さらに洗浄後のフィルターを試験管に挿入し、2mLの酵素基質液(0.1wt%牛血清アルブミン(BSA)、10mM EDTA、さらに1vol%グルクロン基質液を含むリン酸緩衝生理食塩水(日水製薬))に浸漬し、37℃で撹拌しながら反応を行った。この際、Triton X-100濃度を0.1〜0.8vol%に設定した。反応10分後と30分後に0.2mLの反応液を分取し、等量の発光促進剤(トロピクス(Tropix)社:商品名アクセラレーター2(Accelerator II))を添加して、2秒後の発光量を測定した。発光量の測定は、ルミノメータ(ベルトールド社製、LB-9507)を用いて行った。結果を図21に示す。酵素活性値とTriton X-100濃度の関係から、高い酵素活性値を得るためのTriton X-100の濃度は高い方が好ましく、好ましい界面活性剤濃度は0.1〜0.8vol%の間であった。
【0115】
[実施例8]:大腸菌の迅速・高感度測定
本発明によるβ−グルクロニダーゼ活性測定法において、メンブレンフィルターによる濃縮と膜の洗浄を組み合わせることにより、大腸菌測定を迅速化、高感度化できることを示す。
試料には、下水処理場の最初沈殿池越流水と二次処理水を採取し、直ちに測定に供した。培養法(コロニー計数法)による大腸菌数は、3M社製ペトリフィルム「E−coli・大腸菌群数測定用ECプレート」を用い、試料を37℃で20時間培養した後、β−グルクロニダーゼに対する特定酵素基質であるX−gluと反応して青色コロニーを形成して且つガス産生の有るものを大腸菌として計数した。その結果、最初沈殿池越流水中の大腸菌数は、9.1×104CFU/mL、二次処理水中の大腸菌数は、2.3×102CFU/mLであった。
【0116】
まず初めに、この二次処理水の酵素活性値を測定した。二次処理水100mLは、No.5A濾紙を用いて吸引濾過し、そのろ液を孔径1.0μmの混合セルロースエステル製メンブレンフィルター(直径25mm)により濾過することで、細菌をフィルター上に捕集した。そして、0.04vol%のTriton X−100を含む滅菌希釈水(栄研化学)10mLで2回を吸引濾過することにより、フィルターを洗浄した。そして、洗浄後のフィルターを直径30mmの透明ガラス製バイアル内に濾過面が下になるように置き、そこに1mLの酵素基質液(0.1wt%牛血清アルブミン(BSA)、0.1vol%Triton X−100、10m MEDTA、さらに1vol%グルクロン基質液を含むリン酸緩衝生理食塩水(日水製薬))に浸漬し、37℃で攪拌しながら反応を行った。酵素反応10分後、20分後、30分後に、各反応液300μLを採取し、発光促進剤(トロピクス(Tropix)社:商品名アクセラレーター2(Accelerator II))300μLを添加して、2秒後の発光量を測定した。発光量の測定は、ルミノメータ(ベルトールド社製、LB−9507)を用いて行った。各試料における振とう時間(酵素基質反応時間)に対する相対発光量(RLU: Relative Light Unit)をグラフ上にプロットし、求めた直線の傾きを酵素活性値(β−グルクロニダーゼ活性値)とした。
【0117】
図22には、上記のようにして作成した振とう時間(酵素基質反応時間)に対する相対発光量(RLU: Relative Light Unit)のグラフの一例を示す。図22のグラフでは、酵素活性値(直線の傾き)は996RLU/minであった。溶菌処理と酵素反応を同時に行う場合でも、反応時間に応じて発光量が増加した。
【0118】
次に大腸菌を含まない下水処理場の高度処理水に先の最初沈殿池越流水を0.0001〜1vol%添加することにより、所定濃度の大腸菌を含む試料を調製し、先に示した方法(図22と同様の方法)で10分から30分まで間における発光量の変化をβ−グルクロニダーゼ活性値として測定した。
【0119】
同じ試料について、培養法(コロニー計数法)により大腸菌数を測定し、この酵素活性値との相関関係を図23のように示した。
図23に示したとおり、酵素活性値は培養法による大腸菌数0.09CFU/mL〜91CFU/mLの範囲で非常に良好な直線関係が得られた。また、大腸菌の定量下限値が従来方法(非特許文献3に開示の方法)の1.0×103CFU/mLから10000倍以上向上した。次に同様の手法によって、実際の下水処理場の最終沈殿池越流水2検体、消毒処理水1検体について酵素活性値を測定し、この検量線を用いて大腸菌濃度を算出した。その結果を表3に示す。
【表3】

本発明の方法で測定した大腸菌濃度は、培養法で測定した大腸菌数と一致した。さらに、図23の検量線に用いた試料の溶菌酵素反応10分後、20分後、および30分後の発光量と培養法による大腸菌数の関係を図24に示した。溶菌酵素反応10〜30分後の発光量も酵素活性値と同様に大腸菌濃度と高い相関関係を示すことから、10分後の発光量をもって大腸菌数を測定できることが分かった。
【0120】
[実施例9]
次に、より簡易に大腸菌数を測定するため、酵素反応を行う容器内においてフィルターを浸漬した状態で発光量を測定する手法を検討した。
実施例8と同様に細菌を捕集したフィルターを浸漬し、30分間酵素反応を行ったバイアルに直接、発光促進剤(トロピクス(Tropix)社:商品名アクセラレーター2(Accelerator II))1mLを添加して、2秒後の発光量を測定した。このとき、発光量の測定は、直径30mmのバイアルを直接測定できるルミノメータ(マイクロテックニチオン社製、ルミカウンター2500A)を用いて、バイアルの下方よりフィルター全面を測光することにより行った。また、30分間酵素反応後の同反応液300μLを試験管に分取して、300μLの発酵促進剤を加えた系についても、同様に発光量を測定した。
【0121】
結果を図25に示すが、フィルターを含む反応液でも、培養法による大腸菌数と高い相関性を示した。さらに、前試料を発光測定に供する上、フィルター面による光の反射効果により、高濃度側の発光量がさらに増幅され、バックグラウンドも低下するために、より高精度で測定できることが見出された。これまでの蛍光法による酵素活性測定では、励起光の透過を妨害するフィルターを浸漬した試料を測定することは困難であったが、本発光測定法を用いることにより、フィルターを浸漬した状態の反応液の発光量を直接測定することが可能となり、より簡便、かつ高精度に測定することが可能になった。
【0122】
[実施例10]:下水処理場処理水を用いた実証試験
下水処理場から採取した二次処理水および好気性ろ床出口水を、超音波バスで分散させた後、No.5Aろ紙を用いて吸引ろ過した。ろ液を0.8μmメンブレンに通液し、大腸菌を捕集した。酵素の抽出溶液として、BSAを0.1wt%含むリン酸ナトリウム0.1M溶液にTriton X−100を0.2vol%加えた溶液を用い、この溶液に大腸菌が捕集されたメンブレンを浸漬し、37℃で30分間溶菌処理を行った。上澄液100μLを採取し、上述の酵素反応基質溶液180μLと混合した。実施例2と同様の手法により、恒温振とう機を用いて37℃で所定時間振とうさせた後に発光促進剤300μLを添加して発光を起こさせ発光量を測定して酵素活性値を求めた。これとは別に、同じ試料中の真の大腸菌数を培養法(コロニー計数法)で求めた。培地としては、3M社製ペトリフィルム「E−coli・大腸菌群数測定用ECプレート」を用いた。試料を37℃で20時間培養した後、β−グルクロニダーゼに対する特定酵素基質であるX−gluと反応して青色コロニーを形成して且つガス産生の有るものを大腸菌として計数した。
【0123】
以上の手法によって求められた大腸菌数(コロニー計数値)とβ−グルクロニダーゼ活性値との相関関係を図26に示す。
図26の結果を統計学的に解析した結果、95%信頼区間が実用的な範囲に収束した。本発明によれば、簡便且つ迅速且つ高感度なことに加え、測定精度も向上した結果、低濃度の大腸菌から高濃度の大腸菌まで精確に菌数を算出することが可能になった。
【0124】
[実施例11]:β−グルクロニダーゼ活性に基づく大腸菌群数の測定
下水処理場の二次処理水および好気性ろ床出口水に対して、本発明による方法を適用した。被検試料水を超音波バスで分散させた後、No.5Aろ紙を用いて吸引ろ過した。ろ液を0.8μmのメンブレンに通液して、大腸菌を捕集した。大腸菌が捕集されたメンブレンを、Triton X−100を0.2vol%含む抽出溶液に含浸させ、37℃で30分間溶菌した。上澄液100μLを採取し、グルクロン(登録商標)1vol%,リン酸ナトリウム0.1M、EDTA10mMからなる基質溶液180μLと混合した。実施例2と同様の手法により、恒温振とう機を用いて37℃で所定時間振とうさせた後に発光促進剤300μLを添加して発光を起こさせ発光量を測定して酵素活性値を求めた。
【0125】
これとは別に真の大腸菌群数を培養法(コロニー計数法)で求めた。培地としては、3M社製ペトリフィルム「E−coli・大腸菌群数測定用ECプレート」を用いた。試料を37℃で20時間培養した後、β−ガラクトシダーゼに対する特定酵素基質であるX−galと反応して赤色コロニーを形成して且つガス産生の有るものを大腸菌群として計数した。
【0126】
以上の手法によって求められた大腸菌群数(コロニー計数値)と酵素活性値(β−グルクロニダーゼ活性値)との相関を、図27に示した。
図27より、β−グルクロニダーゼ活性値と大腸菌群数とは直線的な相関関係があることが分かる。この結果から、β−グルクロニダーゼ活性値を測定すれば、大腸菌群を算出可能なことが実証された。
【0127】
[実施例12]:海水を用いた実証試験
本発明の好ましい態様では、濾過膜で捕集した細菌を界面活性剤で洗浄しているため、酵素反応が溶液の組成による阻害を受けない。したがって、本発明の好ましい態様によれば、例えば海水のような高濃度塩分を含む試料でも迅速・高感度測定が可能なことを本実施例で示す。
【0128】
雨天時合流式下水道越流水の影響で大腸菌濃度が高くなった海水を用いて、本発明による方法を適用した。被検試料水100mLを超音波バスで分散させた後、No.5Aろ紙を用いて吸引ろ過した。ろ液を1.0μmのメンブレンフィルターに通液して、大腸菌を捕集した。大腸菌が捕集されたメンブレンに10mLの0.02vol%のTritonX−100を含む溶液を2回通水することによってフィルター洗浄を行った。
【0129】
次に、メンブレンをTriton X−100を0.2vol%含む抽出溶液に含浸させ、37℃で30分間溶菌した。上澄液100μLを採取し、グルクロン(登録商標)1%,リン酸ナトリウム0.1M、EDTA10mMからなる基質溶液180μLと混合した。実施例2と同様の手法により、恒温振とう機を用いて37℃で所定時間振とうさせた後に発光促進剤300μLを添加して発光を起こさせ発光量を測定して酵素活性値を求めた。
【0130】
これとは別に真の大腸菌数を培養法(コロニー計数法)で求めた。培地としては、3M社製ペトリフィルム「E−coli・大腸菌群数測定用ECプレート」を用いた。試料を37℃で20時間培養した後、β−グルクロニダーゼに対する特定酵素基質であるX−gluと反応して青色コロニーを形成して且つガス産生の有るものを大腸菌として計数した。
【0131】
以上の手法によって求められた大腸菌群数(コロニー計数値)と酵素活性値(β−グルクロニダーゼ活性値)との相関を、図28に示した。
図28より、β−グルクロニダーゼ活性値に基づく大腸菌数の測定が、海水に影響されず、低濃度まで直線的な相関関係があることが分かる。この結果から、本発明の好ましい態様にかかる方法によれば、濾過膜で捕集した細菌を界面活性剤で洗浄しているため、酵素反応が溶液の組成による阻害を受けないことが実証された。
【0132】
[実施例13]:海水を用いた実証試験
雨天時合流式下水道越流水の影響で大腸菌濃度が高くなった海水を用いて、本発明による方法を適用した。被検試料水100mLを超音波バスで分散させた後、No.5Aろ紙を用いて吸引ろ過した。ろ液を1.0μmのニトロセルロース製メンブレンフィルターに通液して、大腸菌を捕集した。大腸菌が捕集されたメンブレンに10mLの0.02vol%のTriton X−100を含む溶液を2回通水することによってフィルター洗浄を行った。次に、メンブレンを2mlの溶菌酵素基質液(0.1wt%牛血清アルブミン(BSA)、0.1vol%Triton X−100、10m MEDTA、さらに1vol%グルクロン基質液(アプライドバイオシステムズ社)を含むリン酸緩衝生理食塩水(日水製薬))抽出溶液に含浸させ、37℃で30分間酵素反応を行った。酵素反応10分後、20分後、30分後に、各反応液300μLを採取し、発光促進剤300μLを添加して発光を起こさせ、2秒後の発光量を測定して酵素活性値を求めた。
【0133】
これとは別に真の糞便性大腸菌数を培養法(コロニー計数法)で求めた。100mLの試料を滅菌したHAフィルター(Millipore)でろ過し、ろ過したフィルターをm−FC倍地(Millipore m-FC Broth)を浸み込ませたパットを含むプラスチックシャーレに入れて、44.5℃で22時間培養した。そして、形成したコロニーをふん便性大腸菌群数として計数した。
【0134】
以上の手法によって求められた糞便性大腸菌群数(コロニー計数値)と酵素活性値(β−グルクロニダーゼ活性値)との相関を、図29に示す。
図29より、β−グルクロニダーゼ活性値に基づく糞便性大腸菌数の測定が、海水に影響されず、低濃度まで直線的な相関関係があることが分かる。本発明によれば、簡便且つ迅速且つ高感度なことに加え、測定精度も向上した結果、低濃度の大腸菌から高濃度の大腸菌まで精確に菌数を算出することが可能になった。
この結果から、本発明の好ましい態様にかかる方法によれば、濾過膜で捕集した細菌を界面活性剤で洗浄しているため、酵素反応が溶液の組成による阻害を受けないことが実証された。
【産業上の利用可能性】
【0135】
大腸菌は、衛生学的指標として重要であり、さまざまな迅速測定法が提唱されてきた。
しかし、いずれも測定法に問題があり、実用に適さなかった。同等の迅速性(測定時間約1時間)を持つ従来技術(非特許文献3)と比較すると、本発明の方法は感度が40倍〜1000倍以上向上した。また、同等の感度(1CFU/mL)を有する従来技術(特許文献2)と比較すると、測定時間が1/6.5〜1/38に短縮された。本発明は、放流基準値の判定に適する、衛生学的指標の算出方法として実用可能な初めての測定方法である。従来のコロニー計数による菌数測定では、測定に24時間を要していた。そのため、実際には菌数が放流基準値以内であっても、安全のために塩素添加、UV照射、オゾン処理等で殺菌処理を行ってきた。また、従来の迅速測定法では、測定精度が低いため、測定結果を衛生学的指標として用いることが出来ず、安全性が判定できなかった。そのため、これらの殺菌処理を省略することができなかった。しかし、塩素処理やオゾン処理に伴う副生成物が環境に悪いことが近年指摘されている。また、UV照射およびオゾン処理は処理に大きなエネルギーが必要となる。本発明を用いて大腸菌・大腸菌群を迅速に測定すれば、必要な場合だけ殺菌処理を行えば良いことになり、環境保護および省エネルギーに対する効果が大きい。
【0136】
また、本発明は、下水の性状分析のみならず、飲料水等の上水の性状分析(水中の大腸菌数、大腸菌群数などの測定)にも利用することができる。
【図面の簡単な説明】
【0137】
【図1】図1は、本発明方法を実施するための装置の一例の構成を示す図である。
【図2】図2は、本発明方法を実施するための装置の他の形態の構成を示す図である。
【図3】図3は、本発明方法を実施するための装置の他の形態の構成を示す図である。
【図4】図4は、本発明方法を実施するための装置の構成を示す図である。
【図5】図5は、本発明方法を実施するための装置の構成を示す図である。
【図6】図6は、本発明方法を実施するための装置の構成を示す図である。
【図7】図7は、本発明方法を実施するための装置の構成を示す図である。
【図8】図8は、本発明方法を実施するための装置の構成を示す図である。
【図9】図9は、捕集反応装置の一具体例を示す。
【図10】図10は、本発明方法を実施するための装置の構成を示す図である。
【図11】図11は、本発明の測定キットの具体例を示す。
【図12】図12は、実施例1において測定された各種メンブレンフィルターの孔径と細菌捕集効率との関係を示すグラフである。
【図13】図13は、実施例1において測定された各種メンブレンフィルターの孔径と酵素活性値の相対バックグラウンドとの関係を示すグラフである。濾過前の試料に対して同様の酵素活性試験を行うことによって測定された酵素活性値(バックグラウンド)を100%として、これに対する酵素活性値の相対値を相対バックグラウンドとして示した。
【図14】図14は、実施例2で測定された、酵素基質反応時間に対する相対発光量(RLU: Relative Light Unit)のグラフの一つである。反応時間を横軸に、相対発光量を縦軸にプロットし、直線の傾きから酵素活性値を求める。
【図15】図15は、実施例2で測定された、被検試料中の大腸菌数(コロニー計数値)と、本発明方法によって測定されたβ−グルクロニダーゼ活性値との関係を示すグラフである。
【図16】図16は、メンブレン捕集による検出限界値の向上を示すグラフである。
【図17】図17は、実施例3において測定された本発明方法における界面活性剤による濾過膜捕集物の洗浄条件の最適条件を示すグラフである。
【図18】図18は、実施例4で測定された、超音波による溶菌処理を行った酵素活性試験における界面活性剤添加量と酵素活性感度との関係を示すグラフである。
【図19】図19は、実施例5で測定された、界面活性剤による溶菌処理を行った酵素活性試験における溶菌時間と酵素活性感度との関係を示すグラフである。
【図20】図20は、実施例6で測定された、界面活性剤による溶菌処理を行った酵素活性試験における界面活性剤添加量と酵素活性感度との関係を示すグラフである。
【図21】図21は、実施例7で測定された、酵素反応基質と溶菌剤(界面活性剤)とを一緒に添加した場合の界面活性剤添加量と酵素活性感度との関係を示すグラフである。
【図22】図22は、実施例8で測定された、振とう時間(酵素基質反応時間)に対する相対発光量(RLU: Relative Light Unit)のグラフの一例を示す。
【図23】図23は、実施例8で測定された、被検試料中の大腸菌数(コロニー計数値)と、本発明方法によって測定されたβ−グルクロニダーゼ活性値との関係を示すグラフである。
【図24】図24は、一定時間後の発光量と大腸菌濃度との関係を示すグラフである。
【図25】図25は、直接測光と分取測光による発光量と大腸菌数との関係を示すグラフである。
【図26】図26は、実施例10で測定された、被検試料中の大腸菌群数とβ−グルクロニダーゼ活性値(相対発光量)との相関関係を示すグラフである。
【図27】図27は、実施例11で測定された、被検試料中の大腸菌群数と、本発明方法によって測定されたβ−グルクロニダーゼ活性値との関係を示すグラフである。
【図28】図28は、実施例12で測定された、海水試料中の大腸菌数と、本発明方法によって測定されたβ−グルクロニダーゼ活性値との関係を示すグラフである。
【図29】図29は、実施例13で測定された、海水試料中の糞便性大腸菌群数と、本発明方法によって測定されたβ−グルクロニダーゼ活性値との関係を示すグラフである。
【符号の説明】
【0138】
1:被検試料
2:捕集容器
3:溶菌剤
4:反応容器
5:酵素反応基質液
6:促進剤
7:測定装置
11:濾過膜
12:パージ用流体供給機構
13:試料液供給機構
14:酵素反応基質液供給機構
15:洗浄剤供給機構
17:捕集容器
18:恒温槽
32:促進剤供給機構
33:酵素活性値測定装置(ルミノメータ)
37:反応容器
41:目皿
50:循環ライン
【技術分野】
【0001】
本発明は、試料中の細菌を検出・定量する方法及び装置に関する。特に、本発明は、試料水中の大腸菌や大腸菌群などを迅速且つ簡便且つ高感度に検出・定量する方法として有用である。
【背景技術】
【0002】
大腸菌は、糞便性汚染の指標として重要である。また大腸菌群は、糞便性汚染の衛生学的指標として重要であると同時に、消毒効果確認の指標としても用いられている。
大腸菌群(Coliforms)は、グラム陰性、無芽胞の桿菌であり、乳糖ブイヨン−ブリリアントグリーン乳糖胆汁ブイヨン培地法(LB−BGLB法)によって乳糖を分解して酸とガスを生じるか、或いは特定酵素基質培地法によって指定の酵素基質を分解して発色物質を生じる好気性又は嫌気性の細菌と定義されるものであり、Escherichia属、Citrobacter属、Enterobacter属、Klebsiella属から主として構成される。大腸菌群は、病原細菌が存在すると存在する;水界で顕著に増減しない;病原細菌よりも多数存在する;病原細菌よりも消毒剤に対して抵抗性がある;簡単な培地で容易に増殖し、判定が明確にできる;検査すべき試料中にランダムに分布している;培地接種時に他の細菌によって増殖抑制されない;などの特徴を有しているので、古くから糞便性病原細菌(消化器系病原細菌)の汚染指標として広く利用されてきた。しかしながら、大腸菌群は、糞便性病原細菌の他に土壌等の自然由来の細菌も含むため、大腸菌群の検出によっては、温血動物の糞便由来の細菌のみを判別してはいない。
【0003】
大腸菌(Escherichia coli)は、特定酵素基質培地法によってβ−グルクロニダーゼ活性を有すると判定された細菌と定義される。大腸菌は、ヒトや温血動物の腸管内に常在し、糞便由来でない大腸菌群と比べて、糞便汚染の指標として信頼できる。また、単独の菌種であるばかりでなく、他の糞便性指標細菌と比較して、自然界では生存期間が短いため、糞便性汚染のより特異的な指標として用いることができる。
【0004】
また、糞便性大腸菌群(Faecal coliforms)は、大腸菌群にあって、44.5℃で24時間培養したときに、M−FC培地に青色の集落を形成するか、EC培地にガスを生じる細菌と定義されるものであり、Escherichia属、並びに、一部のCitrobacter属、Enterobacter属及びKlebsiella属から主として構成される。糞便汚染のない環境中では、大腸菌群が存在しても糞便性大腸菌群が存在することは少ない。したがって、糞便性大腸菌群は、糞便汚染の指標としては大腸菌よりも信頼性は薄いが、大部分の環境下では、糞便性大腸菌群の濃度が大腸菌の濃度に密接に関連する。このため、糞便性大腸菌群は、糞便汚染の指標として大腸菌群よりも優れていると考えられている。
【0005】
厚生労働省は上水中微生物の基準として大腸菌を採用しており、国土交通省は下水処理場の放流基準値として大腸菌群を採用している。各々の測定対象に応じて検査が義務付けられており、試験方法も定められている。したがって、被検試料の種類に応じて定められた基準に基づいて、試料中の大腸菌数或いは大腸菌群数を測定する必要がある。
【0006】
上記のような試料中の大腸菌或いは大腸菌群の検査において定められている試験方法とは、試料中の細菌を液体培地中あるいは寒天培地上で培養してコロニー数を計数するという検出法である。しかしながらこれらの検出法では、大腸菌数あるいは大腸菌群数の判定に24時間以上を要していた。また、多数の発酵管あるいは培地を調製する必要があり、作業効率が悪かった。
【0007】
試料中の細菌数を判定する方法として、時間の短縮および作業効率の向上を目的としてさまざまな方法が提唱されている。たとえば、大腸菌に特徴的な遺伝子をポリメラーゼ連鎖反応で増幅させた後に検出することによって試料中の大腸菌数を算出する方法(PCR法)や、大腸菌と抗体とを結合させて目印の酵素量を蛍光又は化学発光反応によって測定することによって試料中の大腸菌数を計数する方法(酵素免疫抗体法)などが提案されている。しかしながら、これらの方法は、死菌を生菌と同レベルで扱うため生死の区別が出来ず、したがって測定結果を衛生学的指標として用いることが難しい。また、試料中の細菌を液体培地中あるいは寒天培地上で簡易培養してミクロコロニーを形成して、形成したミクロコロニーを化学発光や蛍光を利用して計数するという方法も提案されている。しかしながらこの方法は、検出可能な大きさまでミクロコロニーを形成させるために4時間以上、前培養する必要がある。更に、デソキシコレート培地のような大腸菌群以外の細菌の生育を抑制する培地の入った密閉容器中に試料を入れて、大腸菌群の呼吸に基づく容器内の酸素又は二酸化炭素の変化を測定することによって大腸菌群の有無を測定する方法(呼吸活性法)も提案されているが、この方法は、菌数に反比例して測定感度が低下するため、低濃度試料の迅速な検出が不可能である。
【0008】
これらの問題を解決する手段として、Fiksdalらにより、試料中の大腸菌数の測定方法として、大腸菌が固有に持つ酵素であるβ−グルクロニダーゼの活性を測定することによって迅速に大腸菌数を算出する方法が提案された(非特許文献1)。この方法は、測定対象の試料に、まず必要に応じて濃縮処理を行い、次に溶菌処理を行って試料中の大腸菌から酵素(β−グルクロニダーゼ)を抽出し、次にこのβ−グルクロニダーゼに対する酵素反応基質を加えることで蛍光などを起こさせてこれを測定することにより試料中の大腸菌数を定量するというものである。このFiksdalらにより提案された方法(酵素活性法)は現在に至るまで様々な改良がなされている(非特許文献2,3)。Rompreらは、PCR法や免疫抗体法等の大腸菌・大腸菌群迅速測定法と比較して、Fiksdalらにより提唱された酵素活性法を「従来法の代替手段として適している」と評価した(非特許文献4)。
【0009】
Fiksdalらによって提唱された酵素活性法を実用化するにあたっての最大の問題点は、検出感度の向上であった。大腸菌群の下水放流基準値は3×103CFU/mLである。一般に、分析方法は、基準値の1/10の測定感度が求められている。また、下水放流水中の大腸菌数は、大腸菌群数の約1/10である。したがって、大腸菌に対しては、3×101CFU/mLの検出感度が求められている。しかし、従来の酵素活性法による大腸菌測定法では、十分な感度が得られなかった。大腸菌のグルクロニダーゼ活性測定用の酵素反応基質として最も広く用いられているのは、蛍光性反応基質である、4−メチルウンベリフェリル−β−D−グルクロニド(MUGlu)である。しかし、MUGluを用いた手法(非特許文献3)では、検出下限値が1×103CFU/mLであり、社会的に求められている検出感度が得られていない。一般的に、蛍光測定よりも発光測定の方が高感度が得られるとされている。そこで、感度を改善するために新規のβ−グルクロニダーゼ向けの発光性酵素反応基質が提案された(特許文献1)。しかし特許文献1で提案された測定法でも、検出下限値が2×105CFU/mLと極めて高く、実用に適さない。更に、ミクロコロニー法における検出下限値をより改善するため、3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−グルクロニド(グルクロン(Glucuron):登録商標(トロピックス社(Tropix,Inc.)))(以下グルクロン(登録商標)と記す)を用いた手法が提案された(特許文献2)。しかしこの手法は、6.5時間の前培養をして菌数を増やす(ミクロコロニーを形成する)必要があり、迅速性に問題があった。
【0010】
また、大腸菌や大腸菌群のような細菌を検出・定量する際に、細菌を含む試料液を濾過膜に通水して細菌を濾過膜上に捕集することにより試料の濃縮を行い、この捕集(濃縮)された細菌に対して分析を行うことによって、分析感度を向上させる試みが行われている。この目的で用いる濾過膜としては、従来は0.2〜0.45μm程度の孔径の濾過膜を用いるのが通常であった(特許文献2、特許文献3)。これは、大腸菌の大きさが通常1〜2μm×0.2〜0.4μm程度であり、上述の範囲の孔径の濾過膜でなければ細菌を高収率で捕集することができないと考えられていたためである。
【0011】
しかしながら、上述の範囲の孔径の濾過膜によって試料水中の細菌を捕集して分析を行った場合、分析結果のバックグラウンド値が高く、検出下限値が高かった。これは、上述の範囲の孔径の濾過膜では、分析対象の細菌に加えて、試料中に含まれている分析に悪影響を与える物質、即ち酵素反応基質と反応して試料の酵素活性測定値に影響を与える夾雑物質(バックグラウンド)も濾過膜上に捕集してしまうためであると考えられる。このため、特に低濃度の大腸菌を含む試料に対しては、この分析手法によって大腸菌の検出・定量を行うことは難しかった。
【0012】
【特許文献1】特開2000−270894
【特許文献2】特表平11−505405
【特許文献3】特開平5−273217
【非特許文献1】Fiksdal, L., Pommepuy, M., Caprais, M.-P., and Midttun, I., Monitoring of fecal pollution in coastal waters by use of rapid enzymatic techniques, Appl. Environ. Microbiol., 60, 1581-1584 (1994)
【非特許文献2】Van Poucke, S.O., and Nelis, H.J., Rapid detection of fluorescent and chemiluminescent total coliforms and Escherichia coli on membrane filters, J. Appl. Microbiol., 42, 233-244 (2000)
【非特許文献3】George, I., Crop, P., and Servais, P., Use of β-D-galactosidase and β-D-gulucuronidase activities for quantitative detection of total and fecal coliforms in wastewater, Can. J. Microbiol., 47, 670-675 (2001)
【非特許文献4】Rompre, A., Servais, P., Baudart, J., de-Roubin, M.-R., and Laurent, P., Detection and enumeration of coliforms in drinking water: current methods and emerging approaches, J. Microbiol. Meth., 49, 31-54 (2002)
【非特許文献5】Bronstein, I., Fortin, J.J., Voyta, J.C., Juo, R.-R., Edwards, B., Olesen, C.E.M., Lijam, N., and Kricka, L.J., Chemiluminescent reporter gene assay: sensitive detection of the GUS and SEAP gene products, BioTechniques, 17, 172-177 (1994)
【発明の開示】
【発明が解決しようとする課題】
【0013】
本発明は、上述の従来技術の問題点を解消し、迅速且つ簡便な方法により高感度で試料中の細菌、特に大腸菌、大腸菌群などを検出及び定量することのできる方法並びに装置を提供することを目的とする。
【課題を解決するための手段】
【0014】
本発明者らは、大腸菌及び大腸菌群などの細菌を濾過膜によって捕集して酵素活性法によって分析(検出・定量)する技術における濾過膜の孔径と検出性能との関係に注目して鋭意研究を行った結果、特定の孔径の濾過膜を用いることで、夾雑物の存在による分析のバックグラウンド値を大幅に小さくすることができ、高感度に細菌の検出及び定量が可能になることを見出し、本発明を完成するに至った。具体的には、本発明者らは、大腸菌などの捕集には、濾過膜の孔径だけではなく濾過膜の吸着性も影響することを見出し、これまでの常識(大腸菌などの捕集には0.2〜0.45μm程度の孔径の濾過膜が最適と考えられていた)に反する孔径0.6〜5.0μm、好ましくは孔径0.8〜3.0μmの吸着性を有する濾過膜が夾雑物を除去し大腸菌だけを選択的に捕集するために最適であることを知見し、本発明を完成するに至ったものである。
【0015】
したがって、本発明によれば、孔径0.6〜5.0μmの濾過膜及び/又はASTM F317-72で測定した場合の蒸留水通水流量が50〜500mL/min・cm2である濾過膜に試料液を通水することによって試料液中の細菌を濾過膜上に捕集し、細菌を捕集した濾過膜を溶菌剤及び酵素反応基質に接触させ、ターゲット細菌中酵素の酵素反応基質に対する酵素活性値を求めことによってる試料液中の細菌数を定量することを特徴とする細菌の検出方法が提供される。酵素活性値は、ターゲット細菌中酵素と酵素反応基質との反応生成物の発光量、蛍光量、発色量などに基づいて求めることができる。濾過膜と溶菌剤及び酵素反応基質との接触は、濾過膜と溶菌剤と酵素反応基質とを同時に接触させても、濾過膜をまず溶菌剤と接触させ、その後、酵素反応基質と接触させてもよい。
【0016】
更に、本発明者らは、上述の特定の濾過膜を用いて細菌を捕集して酵素活性法によって検出・定量を行う際に、細菌を捕集した濾過膜を界面活性剤で通水洗浄することによって分析感度を更に向上させることができることを見出した。
【0017】
即ち、本発明の他の態様は、細菌を捕集した濾過膜に界面活性剤を通水することによって濾過膜を洗浄した後に、濾過膜上に捕集された細菌の酵素活性値を測定することを更なる特徴とする上記記載の試料液中の細菌を検出する方法に関する。
【0018】
更に本発明者らは、酵素反応基質として3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−グルクロニドまたはその誘導体(例えばグルクロン(登録商標)など)を用いてβ−グルクロニダーゼ活性を測定し、測定されたβ−グルクロニダーゼ活性から試料中の大腸菌数及び/又は大腸菌群数及び/又は糞便性大腸菌群数を算出することにより、高感度で大腸菌数及び/又は大腸菌群数及び/又は糞便性大腸菌群数を検出することができることを見出した。本発明方法によるβ−グルクロニダーゼ活性の測定時間は約10分間〜約1時間で、特許文献2で開示されている従来方法での測定時間(6.5時間)を大幅に短縮することができた。また、測定感度(検出下限値)は、大腸菌数で0.1CFU/mL〜2.5×101CFU/mLと非常に高く、特許文献2で開示された方法の検出下限値(1,000CFU/mL)よりも大幅に向上した。
【0019】
即ち、本発明の他の態様は、酵素反応基質として3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−グルクロニドまたはその誘導体(例えばグルクロン(登録商標)など)を用いてβ−グルクロニダーゼ活性を測定することを更なる特徴とする上記記載の試料液中の細菌、特に大腸菌などを検出する方法に関する。
【0020】
更に本発明者らは、β−ガラクトシダーゼに特異的な酵素反応基質、例えば化学発光性酵素反応基質である3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−ガラクトピラノシドまたはその誘導体、特にクロロ誘導体(例えばガラクトン(Galacton):登録商標(トロピックス社(Tropix, Inc.))など)、を用いてβ−ガラクトシダーゼ活性を測定し、測定されたβ−ガラクトシダーゼ活性から試料中の大腸菌群数を算出することにより、高感度で大腸菌群数を検出することができることを見出した。
【0021】
本発明の方法においては、まず被検対象の水試料を、孔径0.6〜5.0μmの濾過膜及び/又はASTM F317-72で測定した場合の蒸留水通水流量が50〜500mL/min・cm2である濾過膜に通水することによって試料液中の細菌、特に大腸菌、大腸菌群及び/又は糞便性大腸菌群を濾過膜上に捕集する。次に、所望の場合には細菌、特に大腸菌、大腸菌群及び/又は糞便性大腸菌群を捕集した濾過膜を界面活性剤で洗浄する。次に、この濾過膜に、溶菌剤と一緒に又は溶菌剤を予め添加した後、測定対象の細菌に特異な酵素(例えば、大腸菌の場合にはβ−グルクロニダーゼ、大腸菌群の場合にはβ−ガラクトシダーゼなど)に対する酵素反応基質を接触させる。これにより、酵素基質反応が起こり、発光性、蛍光性、発色性などの定量測定可能な特性を有する化合物が産生される。そして、発光などを促進させる促進剤を加えて発光などの量を測定することによって、試料の酵素活性値を測定する。一方、被検対象の系において、試料中の測定対象の細菌数(大腸菌、大腸菌群及び/又は糞便性大腸菌群など)と酵素活性値との相関関係を予め求めて検量線を作成しておく。そして、この予め求めておいた細菌数と酵素活性値との相関関係(検量線)に基づいて、測定された酵素活性の測定値から試料中の細菌数を算出する。
【0022】
本発明の方法においては、水試料をそのまま用いても良いが、No.5Aろ紙(有効孔径7μm相当)あるいはこれに相当するフィルターで粗濾過して大きな粒子をあらかじめ除去することが望ましい。フィルターを通す場合は、事前に超音波等の手段を用いて試料を分散させることが望ましく、また通液後に吸引・空洗等の操作で回収率を向上させることが望ましい。
【0023】
必要により粗濾過を行った濾液(水試料)を、孔径0.6〜5.0μmの濾過膜に通水することによって試料液中の細菌を濾過膜上に捕集する。本発明者らの研究により、大腸菌などの細菌を捕集する目的で従来は用いられていなかった孔径(平均孔径)0.6〜5.0μmの濾過膜を用いて大腸菌などを高収率で捕集できることが見出された。本発明においては0.8〜3.0μmの孔径(平均孔径)の濾過膜をこの目的で用いることがより好ましい。なお、濾過膜の孔径(平均孔径)は、製造メーカーから±30%程度の許容範囲で公称値が示されている。濾過膜の材質としては、ニトロセルロース(セルロースナイトレートとセルロースアセテートとの混合物:セルロース混合エステル)製のメンブレンフィルター、セルロースアセテート製のメンブレンフィルター、セラミックフィルター、金属メッシュフィルター、ファブリックフィルターなどを使用することができるが、吸着力の優れているニトロセルロースが最も好ましい。
【0024】
メンブレンフィルターの孔径は、蒸留水通水流量と相関があることが知られており、計測方法も規定されている。本発明では、メンブレンフィルターの製品規格に用いられている試験方法であるASTM F317−72"Standard Test Method for Liquid Flow Rate of Membrane Filters"(孔径が0.10μmのメンブレンフィルターで濾過して粒子を除去した25℃の蒸留水を−0.069MPaの減圧下で濾過し、その流量を1cm2あたり毎分のmL数で表す)で測定した場合に蒸留水通水流量が50〜500mL/min・cm2である濾過膜が適していることを見出した。
【0025】
本発明者らが研究した結果、本発明に従って大腸菌などを高収率で捕集するのに用いることができる濾過膜としては、前述の方法を用いた通水試験ASTM F317-72における蒸留水通水水量が50〜500mL/min・cm2、好ましくは120〜300mL/min・cm2の通水流量を有するものが好適であることが見出された。
【0026】
なお、孔径の大きなメンブレンフィルター(通水流量200mL/min・cm2を超えるもの)を用いる場合には、フィルターを複数枚重ねて使用することによって細菌の捕集効率を向上させることができ、かかる形態も本発明の範囲内に含まれる。
【0027】
なお、厚さの薄いフィルター(厚さ50μm以下、特に10μm以下のもの)を用いる場合には、細菌の回収率が低下するため、孔径の小さなメンブレンフィルターを用いることが好ましい(孔径の大きなメンブレンフィルター(通水流量150mL/min・cm2を超えるもの)は用いないことが好ましい)。
【0028】
次いで、濾過膜を溶菌剤及び酵素反応基質と接触させて、濾過膜上に捕集された細菌(大腸菌及び/又は大腸菌群)から抽出した酵素の活性を測定する。濾過膜と溶菌剤及び酵素反応基質との接触は、濾過膜と溶菌剤と酵素反応基質とを一緒に接触させても、先ず濾過膜に溶菌剤を接触させて酵素を抽出した後に酵素反応基質と接触させてもよい。
本発明においては、濾過膜を溶菌剤及び酵素反応基質と接触させる前に、菌体が溶菌しない濃度の界面活性剤で洗浄することが好ましい。本発明者らの研究により、細菌を捕集した濾過膜を界面活性剤で洗浄することにより、酵素活性法による分析におけるバックグラウンドをより低減させることができ、分析感度を大幅に向上することができることが見出された。この目的で用いることのできる界面活性剤としては、例えば、Triton−X100のような非イオン界面活性剤、ドデシル硫酸ナトリウム(SDS)のような陰イオン界面活性剤などがあり、これらを単独または混合して使用することが好ましい。界面活性剤の濃度は、例えばTriton−X100の場合には、0.01〜0.1vol%であることが好ましい。
【0029】
濾過膜と溶菌剤及び酵素反応基質とを接触させることにより、分析対象の細菌数と相関のある酵素を抽出して特有の酵素反応を起こさせ、酵素反応生成物を指標として酵素活性値を測定することによって細菌を検出・定量することができる。細菌数と相関のある酵素としては、例えば、分析対象の細菌が大腸菌の場合にはβ−グルクロニダーゼ、大腸菌群及び/又は糞便性大腸菌群の場合にはβ−ガラクトシダーゼ及び/又はβ−グルクロニダーゼを用いることができる。
【0030】
溶菌剤としては、菌体を溶菌することができる濃度のTriton−X100のような非イオン界面活性剤やドデシル硫酸ナトリウム(SDS)のような陰イオン界面活性剤を単独または混合して用いることが望ましい。菌体を溶菌することができる界面活性剤の濃度としては、例えば大腸菌及び大腸菌群の場合には0.05〜0.5vol%の範囲を好ましく挙げることができる。溶菌剤として界面活性剤を添加して溶菌する場合には、室温でも良いが、20〜45℃の間の一定温度で溶菌させるのが望ましい。上述のように濾過膜上に細菌を捕捉して、捕捉した細菌に対して酵素活性試験を行う場合、界面活性剤による溶菌処理は、細菌を捕捉した濾過膜を界面活性剤中に浸漬した状態で5〜60分間、好ましくは10〜30分間保持することによって行うことが好ましい。酵素反応基質は、溶菌処理中に溶菌剤と一緒に添加しても、溶菌処理後に別に添加してもよい。
【0031】
また、溶菌剤及び酵素反応基質を添加する前に、超音波破砕を行うこともできる。超音波によって溶菌処理を行う場合には、超音波処理した液に更に界面活性剤を加えた後に酵素反応基質を加えて酵素基質反応を行わせると、菌体残渣が可溶化し、抽出された酵素の分散が進むことでより感度が向上するので好ましい。この場合、超音波処理した液に、酵素を分散でき且つ酵素反応を阻害しない0.01〜0.1%の濃度となるような量の界面活性剤を加えることが好ましい。
【0032】
酵素基質反応(酵素と酵素反応基質との反応)は、緩衝液中で行うことが好ましい。この目的で用いることのできる緩衝液としては、pH6.0〜8.5に調整したリン酸緩衝液あるいはPBS(リン酸緩衝生理食塩水)などを用いることができ、必要に応じて10〜200mMのEDTAと0.02〜2%のBSA(ウシ血清アルブミン)を添加したものも用いることができる。酵素を抽出した試料に、酵素反応基質を混合し、一定温度で5〜60分間反応させることが好ましい。反応温度は20℃〜45℃の間であればいずれも良いが、30℃〜40℃が望ましい。
【0033】
酵素反応基質としては、例えば、分析対象の細菌と相関性のある酵素がβ−グルクロニダーゼである場合、蛍光性酵素反応基質として、4−メチルウンベリフェリル−β−D−グルクロニド、5−ブロモ−4−クロロ−3−インドリル−β−D−グルクロニド、4−トリフロウンベリフェリル−β−D−グルクロニド、化学発光性酵素反応基質として、3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−グルクロニド、グルクロン(登録商標)、D−ルシフェリン−O−β−D−グルクロニド;発色性酵素反応基質として、p−ニトロフェニルグルクロニドなどを用いることができる。また、分析対象の細菌数と相関性のある酵素がβ−ガラクトシダーゼである場合、蛍光性酵素反応基質として、4−メチルウンベリフェリル−β−D−ガラクトピラノシド、4−トリフルオロメチルウンベリフェリル−β−D−ガラクトピラノシド、化学発光性酵素反応基質として3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−ガラクトピラノシドまたはその誘導体、特にクロロ誘導体(ガラクトン(Galacton):登録商標(トロピックス社(Tropix, Inc.)))(以下ガラクトン(登録商標)と記す)、D−ルシフェリン−O−β−D−ガラクトシド;などを用いることができる。
【0034】
濾過膜は酵素反応基質を含む緩衝液(以下、「酵素反応基質液」ともいう)に浸漬させ、一定温度で5〜60分間反応させるが、この際、添加する酵素反応基質液の量は0.1〜5mlが好ましい。この場合、濾過膜よりもわずかに大きな底面積を有する反応容器を用い、容器内に濾過膜を水平に置くことにより、より少量の酵素反応基質液で濾過膜を浸漬させることができるので好ましい。この時、反応温度は20℃〜45℃の間であればいずれでも良いが、30℃〜40℃が望ましく、適度な撹拌を加えることが好ましい。
【0035】
酵素と酵素反応基質との反応によって、発光性、蛍光性或いは発色性の化合物が産生する。反応後、必要に応じて促進剤(発光促進剤、蛍光促進剤、発色促進剤)を加えて、発光などを起こさせてその量を測定する。化学発光を測定する場合、促進剤との混合時間は10秒以内、望ましくは1秒以内とすることが好ましい。促進剤添加から化学発光量などを測定するまでの待ち時間は、1秒〜1分間、望ましくは2秒〜10秒とすることが好ましい。化学発光量などの測定時間は、1秒〜1分間、望ましくは2秒〜10秒間とすることが好ましい。混合時間、待ち時間および測定時間は、サンプル間で常に一定とする。
【0036】
化学発光量の測定は光電子増倍管を用いるフォトンカウンターを用い、酵素反応後の反応液の一部、または全量を発光促進剤と混合して測定することが可能である。この際、酵素反応後の反応液の一部を分取し、発光促進剤を添加してから発光強度を測定することも可能であるが、酵素反応基質液に浸漬した濾過膜に直接発光促進剤を添加し、濾過膜からの発光量を測定することがより望ましい。このとき、測光方向は限定されないが、濾過膜に対向する方向からの測光が望ましい。蛍光や比色強度を利用した方法では、試料液に励起光や透過光を照射する必要があり、反応液中に濾過膜のような光の透過を妨害する固形物を共存させることが出来ないが、化学発光を測定する場合は励起光などを照射する必要がなく、さらに発生する光が濾過膜に反射するため、より効率的に、安定して測定できる。なお、濾過膜は白色のものが好ましいが、非特異的な発光(バックグラウンド)が認められる場合には、黒色の膜を使用することが好ましい。
【0037】
また、本発明者らは、被検試料中のβ−グルクロニダーゼ活性測定値と大腸菌数との相関性に基づいて大腸菌数を測定する酵素活性法において、β−グルクロニダーゼ活性値を測定するための酵素反応基質として、3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−グルクロニド及びその誘導体、例えば、グルクロン(登録商標)などを用いてこれをβ−グルクロニダーゼと反応させて発光性化合物を産生し、産生された発光性化合物を、陽イオン性ポリマーおよびアルカリを含む促進剤を用いて発光させて発光量を定量してβ−グルクロニダーゼ活性を測定し、測定されたβ−グルクロニダーゼ活性から試料中の大腸菌数を算出することにより、高感度で大腸菌数を定量することができることを見出した。なお、大腸菌は大腸菌群やふん便性大腸菌群の中に含まれ、大腸菌群やふん便性大腸菌群中の大腸菌の存在割合は試料の種類によってほぼ一定であることから、大腸菌濃度を測定することで大腸菌群やふん便性大腸菌群数を推定できる。
【0038】
また、本発明者らは、被検試料中のβ−ガラクトシダーゼ活性測定値と大腸菌群数及び/又は糞便性大腸菌群数との相関性に基づいて大腸菌群数及び/又は糞便性大腸菌群数を推定する酵素活性法において、β−ガラクトシダーゼ活性値を測定するための酵素反応基質として、3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−ガラクトピラノシド及びその誘導体、例えばガラクトン(登録商標)などを用いてβ−ガラクトシダーゼと反応させて発光性化合物を産生し、産生された発光性化合物を、陽イオン性ポリマーおよびアルカリを含む発光促進剤、例えばアクセラレータII(商標)を用いて発光させて発光量を定量してβ−ガラクトシダーゼ活性を測定し、測定されたβ−ガラクトシダーゼ活性から高感度で大腸菌群数及び/又は糞便性大腸菌群数を推定することができることを見出した。
【0039】
以上のような3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−グルクロニド及びその誘導体、例えばグルクロン(登録商標)を酵素反応基質として用いてβ−グルクロニダーゼ活性を測定する態様、及び3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−ガラクトピラノシド及びその誘導体、例えばガラクトン(登録商標)を酵素反応基質として用いてβ−ガラクトシダーゼ活性を測定する態様も本発明の範囲内に包含される。即ち、本発明の更に好ましい態様は、上記に説明した酵素活性法による試料中の細菌の検出方法において、
測定対象の細菌が大腸菌であり、大腸菌から抽出されるβ−グルクロニダーゼに対する酵素反応基質として3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−グルクロニド及びその誘導体を用いることを更に特徴とする方法、及び測定対象の細菌が大腸菌群及び/又は糞便性大腸菌群であり、これらから抽出されるβ−ガラクトシダーゼに対する酵素反応基質として3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−ガラクトピラノシド及びその誘導体、例えばガラクトン(登録商標)を用いることを更に特徴とする方法に関する。
【0040】
酵素反応基質として3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−グルクロニド及びその誘導体を用いてβ−グルクロニダーゼ活性を測定する態様又は3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−ガラクトピラノシド及びその誘導体、例えばガラクトン(登録商標)を酵素反応基質として用いてβ−ガラクトシダーゼ活性を測定する態様においては、酵素基質反応の後、発光促進剤を添加して、発光性化合物の化学発光を起こさせ、発光量を測定することが好ましい。かかる態様において用いることのできる発光促進剤としては、陽イオン性ポリマーとアルカリから構成される薬剤ポリ(ビニルベンジルベンジルジメチル)アンモニウムクロライド含有アルカリ溶液を使用することができ、例えばトロピクス(Tropix)社からアクセラレーター2(Accelerator II)として市販されているものを使用することができる。尚、β−ガラクトシダーゼに対する酵素反応基質として3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−ガラクトピラノシドのクロロ誘導体、たとえばガラクトン−スター(登録商標:トロピックス社(Tropix, Inc.))などを用いる場合は、発光促進剤を使用せずに発光量を測定することが可能である。
【0041】
測定された発光量、蛍光量、発色量などから酵素活性値を算出する方法は、当該技術において公知の手法を採用することができる。なお、一般に酵素活性値は、単位時間当たりに生成・増加する反応生成物の量を単位として表す。しかし酵素反応基質として3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−グルクロニド及びその誘導体、例えばグルクロン(登録商標)を用いた場合、反応生成物を直接定量することが困難であることから、単位時間当たりの生成物量で酵素活性値を表すのが極めて難しい。そこで本発明では、反応生成物の量を光量で置き換え、単位時間当たりに増加する光の量で酵素活性値を表す。具体的には、RLU/min(1分間当たりに増加した相対的光量;Relative Light Unit)で表す。以下、単位時間当たりに増加した光量(RLU/min)を、酵素活性値とする。また、同一測定条件下においては、一定時間反応後の発光強度をもって、酵素活性値とすることも可能である。
【0042】
検量線の作成は、測定対象の被検試料と同じ系において、予め種々の所定濃度の細菌試料を用いて、同じ酵素活性測定法により求めたβ−グルクロニダーゼ活性の測定値と、試料中の細菌を液体培地中あるいは寒天培地上で培養してコロニー数を計数することによって求めた菌数との関係をプロットすることによって行うことができる。そして、この検量線に基づいて、上述の酵素活性測定法による未知試料に関する酵素活性の測定値から測定対象の細菌数を定量することができる。
【0043】
以上のように、本発明によれば、孔径0.6〜5.0μmの濾過膜及び/又は蒸留水通水流量が50〜500mL/min・cm2である濾過膜に試料液を通水することによって試料液中の細菌を濾過膜上に捕集し、細菌を捕集した濾過膜を溶菌剤及び酵素反応基質に接触させ、細菌の酵素反応による酵素活性値を測定することによって、夾雑物の存在による分析のバックグラウンド値を大幅に小さくすることができ、試料中の細菌、例えば、大腸菌や大腸菌群を迅速、簡便、且つ高感度で検出・定量することができる。
また、本発明は、上記に説明した試料中の細菌を検出する方法を実施するための装置にも関する。
【0044】
本発明によれば、孔径0.6〜5.0μmの濾過膜及び/又はASTM F317-72で測定した場合の蒸留水通水流量が50〜500mL/min・cm2である濾過膜を収容する捕集容器と、該濾過膜の一次側に試料液を供給する試料液供給機構と、酵素反応基質を供給する酵素反応基質供給機構と、酵素活性値を測定する酵素活性値測定装置と、を含む細菌(好ましくは大腸菌及び/又は大腸菌群)の検出装置が提供される。本発明の細菌の検出装置は、洗浄剤供給機構、溶菌剤供給機構及び/又は促進剤供給機構をさらに具備していてもよい。試料液供給機構及び酵素反応基質供給機構、並びに洗浄剤供給機構、溶菌剤供給機構及び/又は促進剤供給機構は、捕集容器に各流体を必要に応じて供給できるように、好ましくは定量供給できるように、バルブなどを有する配管によって接続されていることが好ましい。また、本発明の細菌の検出装置は、捕集容器とは別に酵素反応を進行させる反応容器を具備していてもよい。あるいは、捕集容器中で酵素反応を進行させてもよい。酵素反応を進行させるには、30℃〜40℃に維持することが必要であるから、恒温槽中に捕集容器及び/又は反応容器を設置することが好ましい。
【0045】
また、本発明によれば、孔径0.6〜5.0μmの濾過膜及び/又はASTM F317-72で測定した場合の蒸留水通水流量が50〜500mL/min・cm2である濾過膜を収容する濾過装置を具備する捕集ユニットと、捕集ユニットから供給される液を受容して酵素基質反応を行う反応ユニットとから構成され、捕集ユニットは、濾過膜の一次側に試料液を供給する試料供給装置、濾過膜の一次側に洗浄液を供給する洗浄液供給装置、細菌を捕集した濾過膜から細菌中の酵素を抽出する手段、抽出処理によって得られる酵素抽出液を反応ユニットに送る手段を具備し、反応ユニットは、捕集ユニットから供給される酵素抽出液に酵素反応基質を供給する酵素反応基質添加装置、酵素反応基質が添加された反応液に促進剤を加える促進剤添加装置、促進剤が加えられた反応液の発光又は蛍光又は発色の量を測定する測定装置を具備する、試料液中の細菌を検出するための装置が提供される。
【0046】
さらに本発明によれば、孔径0.6〜5.0μmの濾過膜及び/又はASTM F317-72で測定した場合の蒸留水通水流量が50〜500mL/min・cm2である濾過膜を収容する濾過装置、濾過膜の一次側に試料液を供給する試料供給装置、濾過膜の一次側に洗浄液を供給する洗浄液供給装置、溶菌酵素反応基質を供給する溶菌酵素反応基質添加装置、濾過膜を浸漬した状態で溶菌酵素反応基質液を一定温度に保持する恒温装置により構成される濾過反応ユニットと、酵素反応後の反応液を測定装置に送る手段を具備し、測定装置に供給する酵素反応後の反応液に促進剤を加える促進剤添加装置、促進剤が加えられた反応液の発光又は蛍光又は発色の量を測定する測定ユニットを具備する、試料液中の細菌(好ましくは大腸菌及び/又は大腸菌群)を検出するための装置が提供される。
【0047】
またさらに、本発明によれば、供給口及び排出口を具備するケーシング内に、孔径0.6〜5.0μmの濾過膜及び/又はASTM F317-72で測定した場合の蒸留水通水流量が50〜500mL/min・cm2である濾過膜を収容する捕集容器と、酵素反応基質液供給ユニットと、酵素活性値を測定する酵素活性値測定装置を含む細菌(好ましくは大腸菌及び/又は大腸菌群)簡易測定キットが提供される。本キットは、洗浄剤供給ユニット、溶菌剤供給ユニット及び/又は促進剤供給ユニットをさらに具備していてもよい。
【好ましい実施形態の説明】
【0048】
以下、本発明の好ましい実施形態を説明する。
本発明の一実施態様は、孔径0.6〜5.0μm及び/又は前述条件下における蒸留水の通水流量50〜500mL/min・cm2の濾過膜を収容し、試料液供給管が濾過膜の一次側に接続されている濾過装置;濾過装置の濾過膜上の捕集物に対して溶菌処理を行う溶菌装置;溶菌処理によって得られる酵素抽出液を受容し、特定の酵素に対する酵素反応基質を酵素抽出液に加えて酵素基質反応を行わせる手段を具備する酵素基質反応装置;酵素反応基質が加えられた反応液に促進剤を加える促進剤添加装置;促進剤が加えられた反応液の発光又は蛍光又は発色の量を測定する測定装置;を具備することを特徴とする試料液中の細菌を検出するための装置である。この実施態様にかかる装置の概念を図1に示す。図1において、試料液1はまず濾過装置2に受容される。濾過装置2は、内部に濾過膜を具備しており、試料液1は濾過膜の一次側に供給されて、濾過膜を通過することによって濾過される。次に、溶菌装置3によって濾過膜上に捕集された物質に溶菌処理が施される。溶菌装置3の具体例としては、濾過膜上の捕集物に超音波を照射する超音波照射装置や、試料液を濾過した濾過膜を界面活性剤中に浸漬して酵素を抽出する装置などを採用することができる。溶菌処理が施された試料は、次に酵素基質反応装置4において、特定の酵素に対する酵素反応基質5が添加され、次に促進剤添加装置6から、酵素基質反応によって産生する発光性、蛍光性又は発色性の化合物の発光、蛍光又は発色を促進する促進剤が添加される。これによって発光などが起こされ、発光などの量を測定装置7によって測定する。このようにして測定された発光量に基づいて、上記に説明した手法によって試料中の特定の細菌を検出・定量することができる。
【0049】
濾過装置2は、試料液を濾過した濾過装置の濾過膜の一次側に界面活性剤洗浄液を供給する濾過膜洗浄液供給装置を更に具備することが好ましい。更に、濾過膜の一次側に濾過膜を空気洗浄するための配管を更に具備することが好ましい。
【0050】
また、本発明方法を実施することのできる装置のより具体的な形態として、本発明の他の態様は、孔径0.6〜5.0μm及び/又は前述条件下における蒸留水の通水流量50〜500mL/min・cm2の濾過膜を収容する濾過装置を具備する捕集ユニットと、捕集ユニットから供給される液を受容して酵素基質反応を行う反応ユニットとから構成され、捕集ユニットは、濾過膜の一次側に試料液を供給する試料供給装置、濾過膜の一次側に洗浄液を供給する洗浄液供給装置、細菌を捕集した濾過膜から細菌中の酵素を抽出する手段、抽出処理によって得られる酵素抽出液を反応ユニットに送る手段を具備し、反応ユニットは、捕集ユニットから供給される酵素抽出液に酵素反応基質を供給する酵素反応基質添加装置、酵素反応基質が供給された反応液に促進剤を加える促進剤添加装置、促進剤が加えられた反応液の発光又は蛍光又は発色の量を測定する測定装置を具備する、試料液中の細菌を検出するための装置に関する。
【0051】
本発明のかかる形態に関する装置の一具体例を図2に示す。図2に示す試料中の細菌を検出するための装置は、試料中の細菌を捕集して溶菌処理を行う捕集ユニット(A)と、捕集ユニット(A)で溶菌処理がされた試料に対して酵素基質反応を行なって発光などの量の定量測定を行う反応ユニット(B)とから構成される。図2においては、反応ユニット(B)として、二種類のタイプが示されている。反応ユニット1では、1検体毎に反応を行うため、検体数が少ない場合に適している。また反応ユニット2では、連続して反応を行うため、連続測定に適している。測定の目的に適した反応ユニットを選択することが可能である。
【0052】
図2において、捕集ユニットAにおける濾過装置17は、内部に、孔径0.6〜5.0μm及び/又は前述条件下での蒸留水の通水流量50〜500mL/min・cm2の濾過膜11と濾過膜の通水量を一定にするための目皿41を収容している。濾過膜11の一次側には、供給配管20が接続され、切り替え弁16を介して、空気供給装置12、試料供給装置13、溶菌剤供給装置14、洗浄液供給装置15が接続されている。また、濾過膜11の下には目皿41、目皿41の二次側には排出管21が接続されている。濾過装置17は、恒温槽18内に配置され、例えば37℃で保持されることが好ましい。
【0053】
まず、試料供給装置13から測定対象の試料液が濾過膜11の一次側に一定流量で供給され、濾過膜を通過することにより濾過される。これにより、試料液中の細菌などは濾過膜11上に捕集される。濾過膜11を通過した液は排出管21を通って、バルブ19を介してドレインとして排出される。次に、切り替え弁16を切り替えて、洗浄液供給装置15から洗浄液を濾過膜11の一次側に供給して、通水洗浄を行うことができる。洗浄液としては、例えば、Triton−Xのような非イオン性界面活性剤が好ましい。濾過膜11を通過した洗浄液は排出管21を通って、バルブ19を介してドレインとして排出される。
【0054】
次に、切り替え弁16を切り替えて、空気供給装置12から空気を吹き込むことができる。これによって、まず、捕集ユニットをパージして、濾過膜上に残った洗浄液を排出管からドレインとして排出することができる。次に、切り替え弁19を切り替えて、空気を反応ユニットBに供給して反応ユニット内をパージすることができる。
【0055】
次に、切り替え弁16を切り替えて、溶菌剤供給装置14から溶菌剤(溶菌液)を濾過装置17に供給する。この際、切り替え弁19を閉止して、濾過装置内に溶菌液を保持して、濾過膜11を溶菌液によって湿潤させた状態で一定時間保持する。次に、切り替え弁19を切り替えて排出管21を反応ユニットBに接続すると共に、切り替え弁16を切り替えて空気供給装置12から空気を吹き込むことによって溶菌処理がされた試料液を反応ユニットBに流す。
【0056】
(b)に示す形態の反応ユニット1は、捕集ユニットAから供給される溶菌処理がされた試料液を受容する反応容器37と、反応容器に酵素反応基質を加える酵素反応基質添加装置31と、反応容器に促進剤を加える促進剤添加装置32、酵素基質反応によって産生する発光性又は蛍光性又は発色性化合物の発光などの量を測定する測定装置33を具備する。反応容器37は、恒温槽39内に配置され、例えば37℃で保持されることが好ましい。
【0057】
捕集ユニットAから供給される溶菌処理がされた試料液は、配管34を通って反応容器37に供給される。次に、酵素反応基質添加装置31から供給管35を通して反応容器37に酵素反応基質が添加される。これによって酵素と基質との反応が行われ、発光性などの特性を有する物質が産生される。図2(b)に示す装置においては、反応容器37には試料送り装置42が配置されており、例えば、一つ目の反応容器37へは酵素反応基質添加から10分後、二つ目の反応容器37へは酵素反応基質添加から15分後、三つ目の反応容器37へは酵素反応基質添加から20分後、というように時間差を付けて測定装置33に送られ、促進剤添加装置32から促進剤が配管36を通して各反応容器に供給される。促進剤を添加して所定時間(例えば2秒)経過後に、産生された物質の発光などの強度を測定装置33、例えばルミノメーターによって測定する。このようにして、幾つかの酵素基質反応時間に対する発光などの強度を測定し、上記に説明した手法によって試料の酵素活性値を算出することができる。
【0058】
(c)に示す形態の反応ユニット2は、捕集ユニットAから供給される溶菌処理がされた試料液を流す配管40と、配管40を流れる溶菌処理がされた試料液に酵素反応基質を加える酵素反応基質添加装置31と、酵素反応基質が加えられた試料液に促進剤を加える促進剤添加装置32と、酵素基質反応によって産生する発光性又は蛍光性又は発色性化合物の発光などの量を測定する測定装置33とを具備する。配管40は、恒温槽39内に配置され、例えば37℃で保持されることが好ましい。
【0059】
捕集ユニットAから供給される溶菌処理がされた試料液は、配管40内を流れ、酵素反応基質添加装置31から酵素反応基質が添加される。これによって酵素と基質との反応が行われ、発光性などの特性を有する物質が産生される。図2(c)に示す装置においては、酵素反応基質添加装置31は、配管の三箇所に接続されており、例えば、酵素反応基質添加装置の一つ目の接続部、二つ目の接続部、及び三つ目の接続部から促進剤添加装置の接続部まで試料液が流れる時間が、それぞれ20分、15分、10分となるように、各接続部の位置及び配管内の試料液の流速を調整する。また、促進剤添加装置32の接続部から測定装置33まで試料液が流れる時間が、例えば2秒となるように、それぞれの位置及び配管内の試料液の流速を調整する。試料液が三つの酵素反応基質添加装置接続部の全てに達した後に、酵素反応基質を三つの接続部に同時に供給する。そして、酵素反応基質の添加後、10分経過後、15分経過後、20分経過後に、促進剤添加装置32から促進剤を添加し、その2秒後に測定装置33によって発光などの強度を測定することによって、酵素基質反応時間が10分、15分、20分の場合の発光などの強度を測定することができ、得られた測定値に基づいて上記に説明した手法によって試料の酵素活性値を算出することができる。
【0060】
また、本発明は、孔径0.6〜5.0μmの濾過膜及び/又はASTM F317-72で測定した場合の蒸留水通水流量が50〜500mL/min・cm2である濾過膜を収容する捕集容器と、該濾過膜の一次側に試料液を供給する試料液供給機構と、酵素反応基質を供給する酵素反応基質供給機構と、酵素活性値を測定する酵素活性値測定装置と、を含む細菌(好ましくは大腸菌及び/又は大腸菌群)の検出装置に係る。この実施態様の概略を図3〜図8に示す。
【0061】
図3において、検出装置は、孔径0.6〜5.0μmの濾過膜及び/又は蒸留水通水流量が50〜500mL/min・cm2である濾過膜11及び濾過膜11の通水量を一定にするための目皿41を収容する捕集容器17と、酵素活性値を測定する酵素活性値測定装置33と、を含む。捕集容器17は、恒温槽18内に配置されており、30℃〜45℃、好ましくは37℃に維持され得る。また、捕集容器17は、捕集された細菌(大腸菌など)と酵素反応基質液及び溶菌剤とを充分に接触させるために撹拌装置又は振動装置(図示せず)などを具備することが好ましい。捕集容器17の濾過膜11の一次側には、捕集容器17の内部をパージするためのパージ用流体(空気、純水など)を供給するパージ用流体供給機構12と、濾過膜11の一次側に被検液を供給する試料液供給機構13と、酵素反応基質及び場合によっては溶菌剤を供給する酵素反応基質供給機構14と、洗浄剤を供給する洗浄剤供給機構15と、が切替弁16を有する配管を介して接続されており、所望量の各液を所望時に供給できるように構成されている。捕集容器17の濾過膜11の二次側には、三方バルブ19を有する配管21が接続されており、濾液や過剰の洗浄剤や溶菌剤などをドレインとして排出し、酵素反応生成物(ジオキセタン誘導体)を含む酵素活性値測定用試料液は酵素活性値測定装置33へ送るように構成されている。配管21には、促進剤供給機構32が接続されており、酵素活性値測定用試料に発光促進剤などを添加してから酵素活性値測定装置33に送ることもできる。酵素活性値測定装置33は、光電子増倍管やフォトダイオードを有するルミノメータやCCDカメラなど公知の発光測定装置でよい。
【0062】
次に、図3に示す検出装置を用いて細菌の検出を行う方法を説明する。まず、被検液を試料液供給機構13から濾過膜11の一次側に一定流量で供給する。被検液は、濾過膜11により濾過され、測定対象の細菌(大腸菌など)は濾過膜11上に捕集され、濾液は、配管21を通ってバルブ19を介してドレインとして排出される。次に、切り替え弁16を切り替えて、洗浄液(例えば、Triton−Xのような非イオン性界面活性剤を含む溶液)を洗浄液供給機構15から濾過膜11の一次側に供給して、通水洗浄を行う。濾過膜11を通過した洗浄液は配管21を通って、バルブ19を介してドレインとして排出される。次に、切り替え弁16を切り替えて、パージ用流体供給機構12からパージ用流体(例えば、空気又は純水)を吹き込み、捕集容器17内部をパージして、濾過膜11上に残った洗浄液を配管21を通してドレインとして排出させる。次に、切替弁16を切り替えて、酵素反応基質供給機構14から酵素反応基質液を捕集容器17に供給する。このとき、酵素反応基質液は、酵素反応基質(例えば、3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−グルクロニドまたはその誘導体)と溶菌剤(例えば、Triton X100などの非イオン系界面活性剤やドデシル硫酸ナトリウムなどの陰イオン界面活性剤)の混合物であることが好ましい。濾過膜11上に捕集された細菌の細胞壁は溶菌剤によって溶かされて酵素が露出する。酵素は酵素反応基質と反応して、発光性などの特性を有する酵素反応生成物(例えば、ジオキセタン誘導体)を産生する。次に、この酵素反応液に、促進剤供給機構32から発光を促進する発光促進剤(例えば、Accelerator II(Tropix社、商標))などを供給して、所定時間(例えば10秒以内)接触させた後、酵素活性値測定用試料液をフォトダイオードや光電子増倍管などを有するルミノメータやCCDカメラなどの酵素活性値測定装置33に送り、ここで発光量などが測定される。発光量などの測定値から、予め作成しておいた検量線を用いて酵素活性値を算出することができる。
【0063】
さて、図4〜図8に本発明の測定装置の数種の変形態様を示す。図4〜図8に示す装置は、基本的に図3に示す装置と同じ構成であり、同じ構成要素には同じ参照符号を付して説明を割愛し、異なる構成について説明する。
【0064】
図4に示す実施態様では、捕集容器17の下流側に反応容器37を設けている。反応容器37は恒温槽(図示せず)内部に設けられており、反応容器37内の温度を30℃〜45℃、好ましくは37℃、に維持することが望ましい。この場合、捕集容器17では酵素反応が十分に進行する必要はないので、捕集容器17を恒温槽18内に位置づけても位置づけなくてもどちらでもよい。反応容器37は、ループ状に形成した配管を恒温槽内に設置したもの用いることができる。反応容器37は、酵素と酵素反応基質との接触を良好にして反応を促進させるために、撹拌装置又は振動装置を具備することが好ましい。パージ用流体供給機構12からパージ用流体(空気が好ましい)を送り、反応容器37から測定対象物質を含む試料流体を測定装置33に送り出してもよい。図4に示す実施態様では、捕集容器17とは別に反応容器37を具備することで、捕集容器17では主として溶菌作用による酵素の抽出を行い、反応容器37では主として酵素と酵素反応基質との反応を進行させることができる。さらに細菌(酵素)と酵素反応基質との接触時間が長くなり反応が進行するため、測定感度がさらに向上するという利点がある。
【0065】
図5に示す実施態様では、反応容器37の下流に、循環ライン50と循環ポンプ51とを位置づけて、測定対象試料となる物質、酵素、酵素反応基質などを含む試料流体を捕集容器17に返送する。試料流体を捕集容器17に再循環させることによって、試料流体の撹拌が行なわれ、濾過膜11上に残留している細菌の溶菌が促進され、酵素、酵素反応基質などを試料流体中に洗い出すことができ、酵素と酵素反応基質との接触時間が長くなり反応が更に進行するので酵素反応生成物の濃度が上昇し、測定感度を向上させることができると共に、添加する酵素反応基質の総量が少量で済むという利点がある。
【0066】
図6に示す実施態様は、捕集容器17を透明樹脂又は透明ガラス製などの光透過性物質で構成し、捕集容器17をそのまま測定セルとして利用する態様である。促進剤供給機構32は、促進剤を濾過膜11の一次側に供給するように捕集容器17の上流に配置されている。また、酵素活性値測定装置33は、捕集容器17の濾過膜11の一次側から発光量を測定するように配置されている。この態様では、濾過膜11の一次側に被検液、溶菌剤及び酵素反応基質を供給して、酵素反応を進行させ、測定対象物質を産生させた後、発光性促進剤などを供給して発光を促進させ、濾過膜11の一次側濾過面を酵素活性値測定装置33で測定する。本実施態様では、捕集容器17において、酵素反応及び酵素活性値測定を行うことができるので、装置構成上及び測定作業上の両面において著しく簡易化できる。
【0067】
図7に示す実施態様は、図6とほぼ同じであるが、捕集容器17の濾過膜11の二次側濾過面を測定するように酵素活性値測定装置33を配置する。酵素反応の際に反応液の循環を行わないタイプの測定装置においては、図9のようにろ過ユニットの一次側に一定の空間を設け、そこに反応基質液を供給して反応ユニットを攪拌しながら溶菌酵素反応を進行させることが好ましい。この場合、反応液や膜と測定装置33との距離が長くなり、発光強度が低くなる。また、酵素反応中に反応液が二次側に漏洩する場合には、一次側の反応液量がばらつき、誤差を生じやすくなる。一方、二次側から測光すると、試料までの距離が短い上、過膜表面を直接測光するため、光が白色のろ紙に反射して高い発光強度が得られる。
【0068】
図8に示す実施態様は、濾過膜11の一次側に被検液及び洗浄液を供給し、二次側に酵素反応基質液及び促進剤を供給(圧入)し、二次側濾過面を測定する態様である。試料液供給機構13及び洗浄液供給機構15を濾過膜11の一次側で捕集容器17に配管20を介して接続し、酵素反応基質液供給機構14及び促進剤供給機構32を濾過膜11の二次側で捕集容器17に配管21(20)を介して接続し、捕集容器17下部に酵素活性値測定装置33を配置する。この実施態様では、配管21は、捕集容器17から被検液及び洗浄液を排出する排出ラインとして作用すると共に、捕集容器17に酵素反応基質液及び促進剤を供給する供給ラインとしても作用する。濾過膜11上には測定対象となる細菌が捕集され、濾過膜11の二次側から供給(圧入)された酵素反応基質液及び促進剤は濾過膜11に浸透し、濾過膜11の一次側まで移動して、濾過膜11上に捕集されている細菌と接触する。
【0069】
図9に、捕集容器17の一具体例を示す。捕集容器17は、恒温槽18内に位置づけられており、捕集容器17を振とうさせる振とう装置22が取り付けられている。捕集容器17内には、濾過膜11及び目皿41が取り付けられている。捕集容器17には、反応液を保持した状態で反応液を混合できるように、一次側に一定の空間を有している。捕集容器17には、液の供給及び排出のための配管が濾過膜11の一次側及び二次側に取り付けられている。図示した具体例では、二次側の配管にバルブ25を取り付け、液の流出を防止している。しかし、図2〜5に示したように、配管に三方バルブなどを取り付ける場合には、バルブ25はなくてもよい。
【0070】
図10に、濾過膜11が脱着可能に取り付けられている捕集容器17を用いる捕集ユニット及び反応・測定ユニットを具備する検査装置の一例を示す。捕集ユニットは、捕集容器17と、配管及び切替弁16を介して捕集容器17に接続されている試料液供給機構13、洗浄液供給機構15及びパージ用流体供給機構12を具備する。捕集容器17は適宜態様で開閉可能に構成されており、濾過膜11を脱着可能に取り付けることができる。反応・測定ユニットは、恒温槽18内に位置づけられている反応容器37と、反応容器37に配管20及び切替弁16を介して接続されている酵素反応基質液供給機構14及び促進剤供給機構32と、反応容器37の底部から測定するように位置づけられている酵素活性値測定装置33を具備する。被検液から細菌捕集後、濾過膜11を捕集容器17から取りだして、反応容器37に移し、酵素反応基質液及び促進剤を供給して、発光性物質の発光量などを酵素活性値測定装置33で測定する。
【0071】
図11に、測定キットの実施態様を示す。測定キットは、孔径0.6〜5.0μmの濾過膜及び/又は蒸留水通水流量が50〜500mL/min・cm2である濾過膜11及び濾過膜11の通水量を一定にするための目皿41を収容する捕集容器17と、酵素反応基質液供給容器15と、洗浄液供給容器14と、促進剤供給容器32を含む。各液の供給容器は、例えば、蓋部分をシリコンゴム性としてシリンジの針を突き刺して液を採取する態様、蓋部分にスポイトを取り付ける態様など液の計量採取に適する構成であることが好ましい。測定キットは、手作業での簡易測定に適している。
【0072】
本発明の実施態様は以下の通りである。
1.試料液を、孔径0.6〜5.0μm及び/又は蒸留水通水流量が50〜500mL/min・cm2である濾過膜に通水することによって試料液中の細菌を濾過膜上に捕集し、濾過膜上に捕集された細菌を溶菌処理にかけることによって酵素を抽出し、抽出液に所定の酵素反応基質を加えて酵素基質反応を行わせて酵素活性値を測定することによって試料液中の細菌数を定量することを特徴とする細菌の検出方法。
2.細菌を捕集した濾過膜に界面活性剤を通水することによって濾過膜を洗浄した後に、濾過膜上に捕集された細菌を溶菌処理にかける上記第1項に記載の方法。
3.試料液を、孔径0.6〜5.0μm及び/又はASTM F317-72で測定した場合の蒸留水通水流量が50〜500mL/min・cm2である濾過膜に通水することによって試料液中の細菌を濾過膜上に捕集し、細菌を捕集した濾過膜を溶菌剤と酵素反応基質を含む液に接触させ、酵素反応を行わせて酵素活性値を測定することによって所定の酵素反応基質を加えて酵素基質反応を行わせて酵素活性値を測定することによって試料液中の細菌数を定量することを特徴とする細菌の検出方法。
4.細菌を捕集した濾過膜に界面活性剤を通水することによって濾過膜を洗浄した後に、濾過膜上に捕集された細菌の酵素活性値を測定する上記第3項に記載の方法。
5.濾過膜に捕集した細菌由来の酵素活性値を発光強度によって測定する細菌の測定方法において、濾過膜を濾過面以上の底面積を有する反応室内で酵素基質液に浸漬して酵素反応を行い、その底面より濾過膜全面からの発光量を測定する上記請求項第3項又は第4項に記載の方法。 6.測定対象の細菌が大腸菌、大腸菌群及び/又は糞便性大腸菌群であり、大腸菌から抽出されるβ−グルクロニダーゼの酵素活性値に基づいて試料液中の大腸菌数を定量する上記第1項〜第5項のいずれかに記載の方法。
7.酵素反応基質として3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−グルクロニド(グルクロン(Glucuron):登録商標)またはその誘導体を用いる、上記第6項に記載の方法。
8.測定対象の細菌が大腸菌群及び/又は糞便性大腸菌群であり、大腸菌群から抽出されるβ−ガラクトシダーゼの酵素活性値に基づいて試料液中の大腸菌群数を定量する上記第1項〜第5項のいずれかに記載の方法。
9.酵素反応基質として3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−ガラクトピラノシド及びその誘導体を用いる、上記第8項に記載の方法。
10.孔径0.6〜5.0μmの濾過膜及び/又は蒸留水通水流量が50〜500mL/min・cm2である濾過膜を収容する濾過装置を具備する捕集ユニットと、捕集ユニットから供給される液を受容して酵素基質反応を行う反応ユニットとから構成され、捕集ユニットは、濾過膜の一次側に試料液を供給する試料供給装置、濾過膜の一次側に洗浄液を供給する洗浄液供給装置、細菌を捕集した濾過膜から細菌中の酵素を抽出する手段、抽出処理によって得られる酵素抽出液を反応ユニットに送る手段を具備し、反応ユニットは、捕集ユニットから供給される酵素抽出液に酵素反応基質を供給する酵素反応基質添加装置、酵素反応基質が添加された反応液に促進剤を加える促進剤添加装置、促進剤が加えられた反応液の発光又は蛍光又は発色の量を測定する測定装置を具備する、試料液中の細菌を検出するための装置。
11.孔径0.6〜5.0μmの濾過膜及び/又は蒸留水通水流量が50〜500mL/min・cm2である濾過膜を収容する濾過装置、濾過膜の一次側に試料液を供給する試料供給装置、濾過膜の一次側に洗浄液を供給する洗浄液供給装置、酵素反応基質を供給する酵素反応基質添加装置、濾過膜を浸漬した状態で酵素反応基質液を一定温度に保持する恒温装置により構成される濾過反応ユニットと、酵素反応後の反応液を測定装置に送る手段を具備し、測定装置に供給する酵素反応後の反応液に促進剤を加える促進剤添加装置、促進剤が加えられた反応液の発光又は蛍光又は発色の量を測定する測定ユニットを具備する、試料液中の細菌を検出するための装置。
【実施例】
【0073】
以下の実施例により本発明を更に具体的に説明する。本発明は以下の記載に限定されるものではない。
【0074】
[実施例1]:大腸菌捕集に用いるメンブレンフィルターの材質および孔径と、大腸菌およびバックグラウンドに影響する夾雑物の捕集効率との関係
本実施例では、市販されている種々の孔径(平均孔径)を有するメンブレンフィルター(ニトロセルロースメンブレンフィルター、セルロースアセテートメンブレンフィルター及びポリカーボネートメンブレンフィルター)を用いて、各種メンブレンフィルターにおける孔径と、細菌捕集効果、酵素活性試験におけるバックグラウンドとの関係を調べた。実験に使用した各種メンブレンフィルターの物性値(メーカーによる公表値)を表1に示す。表1から分かるとおり、メンブレンフィルターの規格は孔径で表しても良いし、蒸留水通水流量で表しても良い。実施例では便宜上、孔径で表すが、これらの数字は、表1を用いて蒸留水通水流量で換算しても良い。
【0075】
【表1】

【0076】
上記の各種メンブレンフィルターの細菌捕集効率を調べた。下水流入水を1/50に希釈して試料を調製し、φ47mmのメンブレンフィルターに通水した。通水量は、孔径0.2μmのフィルターで50mL,0.40〜0.45μmのフィルターで100mL,0.65μm以上のフィルターで200mLとした。ろ過前の試料及びろ液を、コロニー試験にかけ、試料及びろ液中のβ−ガラクトシダーゼ活性を有する細菌(GALase(+)),およびβ−グルクロニダーゼ活性を有する細菌(GLUase(+))を、3M社製ペトリフィルム(登録商標)を用いて計数した。具体的には、「E−coli・大腸菌群数測定用ECプレート」を用いて、試料及びろ液中の細菌を37℃で20時間培養した後、赤色コロニーを形成したものをGALase(+),青色コロニーを形成したものをGLUase(+)として、それぞれ計数した。
【0077】
ろ過前の試料中のGALase(+)は3,600CFU/mL,GLUase(+)は360CFU/mLであった。ろ液中のGALase(+)およびGLUase(+)の計数結果を表2および図12に示した。
【0078】
【表2】

【0079】
膜厚が100μm以上あり、且つ吸着性が低いセルロースアセテートでは、孔径が0.8μmから細菌のリークが始まり、孔径が大きくなるにしたがって細菌捕集効率が低下したが、網目状構造の中に大腸菌が入り込む形で捕集されるため、1μm以上の孔径を用いた場合でも捕集効率が高く、実用可能な範囲であった。
【0080】
膜厚が100μm以上あり、且つ吸着性が高いニトロセルロースでは、孔径が1.0μmから細菌のリークが始まったが、孔径が大きくなっても細菌捕集効率がほとんど低下しなかった。吸着性が高いため、同様の網目状構造を有するセルロースアセテートよりも捕集効率が高くなった。
【0081】
膜厚が10μm以下と薄く、且つ吸着性が低いポリカーボネートでは、孔径が0.8μmから細菌のリークが始まり、1μmになると細菌捕集効率が急激に低下した。これより、大腸菌捕集にポリカーボネートを用いる場合は、0.8μm以下の孔径を用いることが好ましいことが分かった。
【0082】
上記の結果から、孔径(平均孔径)が0.6〜5.0μm、より好ましくは0.8〜3.0μmのメンブレンフィルターを用いることによって、大腸菌などを実用的な範囲で高収率に捕集できることが見出された。
【0083】
また、膜厚が10μm以下のフィルターを用いる場合は、0.8μm以下の孔径であれば大腸菌などを実用的な範囲で高収率に捕集できることが見出された。
【0084】
次に、酵素活性試験のバックグラウンドを高くして定量下限値に悪影響を与える夾雑物を、前述のメンブレンフィルターを用いて排除する実験を行った。大腸菌が含まれていないことを前述のペトリフィルムを用いた測定であらかじめ確認してある環境水を用いて、孔径および材質の差による変化を調べた。上記で用いたニトロセルロースメンブレンフィルター、セルロースアセテートメンブレンフィルター及びポリカーボネートメンブレンフィルター)を用いて試験を行った。
【0085】
β−グルクロニダーゼに対する酵素反応基質溶液としては、グルクロン(登録商標)1vol%,リン酸ナトリウム0.1M,EDTA 10mMの溶液を用いた。
【0086】
大腸菌が含まれていないことを確認済みの環境試料を超音波バスで分散した後、No.5Aろ紙を用いて吸引ろ過した。
得られたろ液を最初に孔径3.0μmのメンブレンフィルターに通液した。次に、フィルターに、50mLの0.02vol%のTriton X−100を含む溶液を通水することによってフィルター洗浄を行った。ろ液と洗液とを合わせて、次に孔径0.8μmのメンブレンフィルターに通液した。次に、フィルターに50mLの0.02vol%のTriton X−100を含む溶液を通水することによってフィルター洗浄を行った。以下、同じ手順で、孔径0.45μm及び0.2μmのメンブレンフィルターによる濾過を行った。
【0087】
各孔径のフィルターの捕集物を、β−グルクロニダーゼ酵素活性試験にかけてβ−グルクロニダーゼ酵素活性値を調べた。
酵素の抽出溶液としてBSAを0.1wt%含むリン酸ナトリウム0.1M溶液にTriton X−100を0.2vol%加えた溶液を用い、上述の0.02vol%Triton X−100溶液による洗浄を行った後の各孔径のフィルターをこの抽出溶液中に浸漬し、37℃で30分間溶菌処理を行った。
【0088】
β−グルクロニダーゼに対する反応基質溶液として、グルクロン(登録商標)1vol%、リン酸ナトリウム0.1M、EDTA 10mMを含む溶液を用い、この反応基質溶液180μLと、上述の溶菌処理で得られた酵素抽出液100μLを混合した。恒温振とう機を用いて37℃で5〜30分間振とうした。振とうを5分間、10分間、15分間及び20分間行った時点でそれぞれ試料を採取し、発光促進剤(トロピクス(Tropix)社:商品名アクセラレーター2(Accelerator II))300μLを添加して、2秒後の発光量を測定した。発光量の測定は、ルミノメータ(ベルトールド社製、LB−9507を用いて行った。
【0089】
各試料における振とう時間(酵素基質反応時間)に対する相対発光量(RLU: Relative Light Unit)をグラフ上にプロットし、求めた直線の傾き(RLU/min)から酵素活性値(β−グルクロニダーゼ活性値)を求めた。
【0090】
本実施例で用いた被検試料は、大腸菌が含まれていないことを確認済みの試料であるので、各試験において測定された酵素活性値は全て酵素活性試験に悪影響を与える夾雑物質によるバックグラウンドであると考えることができる。
【0091】
各種メンブレンフィルター別に、各孔径のフィルターによる捕集物に対して測定されたβ−グルクロニダーゼ酵素活性値(相対バックグラウンド)を図13に示す。濾過前の試料に対して同様の酵素活性試験を行うことによって測定された酵素活性値(バックグラウンド)を100%として、これに対する酵素活性値の相対値を相対バックグラウンドとして示した。
【0092】
いずれのメンブレンフィルターでも、孔径0.4〜0.45μmのフィルターでの試験で50%以上のバックグラウンドが検出された。図13より、孔径0.6μmを下回るメンブレンフィルターでの濾過によって、酵素活性試験に対して悪影響を与える夾雑物質が濾過膜上に捕集されてしまい、バックグラウンドが高くなることが分かる。
【0093】
図13の結果から、夾雑物の影響を排除するには、孔径が0.6μm以上である必要があることが分かった。また図12の結果から、大腸菌を十分な効率で捕集するには、孔径が5.0μm以下、特に3.0μm以下である必要があることが分かった。これらの結果を総合すると、孔径が0.6〜5.0μm、より好ましくは0.8〜3.0μmの濾過膜を用いて試料液の濾過を行って濾過膜上に細菌を捕集し、捕集された細菌に対して酵素活性試験を行うことによって、バックグラウンドの悪影響を排除し且つ実用的な範囲の精度で、試料中の細菌の検出・定量を行うことができることが示される。
【0094】
また、膜厚が10μm以下と薄く、且つ吸着性が低いポリカーボネートでは、大腸菌を高収率で捕集するのに必要な孔径が0.8μm以下であり、且つバックグラウンドが検出される孔径が0.4〜0.45μmであることから、最適な洗浄効果が得られる孔径の範囲が、より厚みのあるニトロセルロースメンブレンフィルターやセルロースアセテートメンブレンフィルターと比較して狭い。これより、大腸菌捕集に用いるフィルターは、10μmを超える厚みがあるものが好ましいことが分かった。
【0095】
[実施例2]:大腸菌の迅速・高感度測定
始めに、β−グルクロニダーゼ活性値を測定するための酵素反応基質として、グルクロン(登録商標)を用いることにより、標準試料を用いた場合の大腸菌測定が迅速・高感度化されることを示す。
【0096】
下水処理場から採取した初沈越流水中の大腸菌数を、培養法(コロニー計数法)で求めた。培地としては、3M社製ペトリフィルム「E−coli・大腸菌群数測定用ECプレート」を用いた。試料を37℃で20時間培養した後、β−グルクロニダーゼに対する特定酵素基質であるX−gluと反応して青色コロニーを形成して且つガス産生の有るものを大腸菌として計数した。この初沈越流水を滅菌希釈水に適宜添加して、1×101〜1×104個/mLの範囲で7検体の標準試料を作成した。初沈越流水中には1×106個/mLの大腸菌が含まれており、これを1×101〜1×104個/mLの範囲になるよう滅菌希釈水で希釈することにより、試料中に共存している夾雑物質の量は1/100以下になり、測定のバックグラウンドに与える影響を排除できる。
【0097】
これらの標準試料を、超音波バスで分散させた後、No.5A濾紙を用いて吸引濾過した。試料に添加・混合した後の濃度が、BSA濃度が0.1wt%、リン酸ナトリウム溶液濃度が0.1M、Triton X−100濃度が0.2vol%となるように調整した濃縮溶菌液を試料に添加して、37℃で30分間溶菌処理を行った。上澄液100μLを採取し、β−グルクロニダーゼに対する酵素反応基質溶液として、グルクロン 1vol%,リン酸ナトリウム0.1M、EDTA 10mMからなる溶液180μLと混合した。恒温振とう機を用いて37℃で振とうした。振とうを5分間、10分間、15分間及び20分間行った時点でそれぞれ試料を採取し、発光促進剤(トロピクス(Tropix)社:商品名アクセラレーター2(Accelerator II))300μLを添加して、2秒後の発光量を測定した。発光量の測定は、ルミノメータ(ベルトールド社製、LB−9507)を用いて行った。各試料における振とう時間(酵素基質反応時間)に対する相対発光量(RLU: Relative Light Unit)をグラフ上にプロットし、求めた直線の傾きを酵素活性値(β−グルクロニダーゼ活性値)とした。図14には、上記のようにして作成した振とう時間(酵素基質反応時間)に対する相対発光量(RLU: Relative Light Unit)のグラフの一例を示す。図14のグラフでは、酵素活性値(直線の傾き)は141.9RLU/minであった。
【0098】
以上の手法によって求められた大腸菌数(コロニー計数値)とβ−グルクロニダーゼ活性値との相関関係を図15に示す。
図15に示したとおり、大腸菌数で2.5×101CFU/mL〜2.5×103CFU/mLの範囲で非常に良好な直線関係が得られた。大腸菌の定量下限値が従来方法(非特許文献3に開示の方法)の1.0×103CFU/mLから40倍向上した。
【0099】
次に、メンブレンフィルターを用いることにより、測定のバックグラウンドに影響を与える夾雑物質が含まれている実試料を用いた場合でも、前述の標準試料と同様の高感度が得られることを示す。
【0100】
下水処理場から採取した初沈越流水,二次処理水,好気性ろ床出口水を、超音波バスで分散した後、No.5Aろ紙を用いて吸引ろ過した。得られたろ液を適宜混合して、大腸菌数=101〜104CFU/mLの範囲で7検体の試料を調製し、試料を二つに分けた。試料の一つは、孔径0.8μmのニトロセルロース製メンブレンフィルターに通液してメンブレン上に大腸菌を捕捉し、メンブレンを実施例1で用いたものと同じ50mLの0.02vol%Triton X−100を含む溶液で洗浄した後、BSAを0.1%含むリン酸ナトリウム0.1M溶液にTriton X−100を0.2vol%加えた溶液中に浸漬して大腸菌を溶菌させた。もう一つの試料液は、メンブレンフィルターへの通液を行わず、BSAを0.1wt%含むリン酸ナトリウム0.1M溶液にTriton X−100を0.2vol%加えた溶液と容積比1:1で混合して、大腸菌を溶菌させて酵素抽出液を得た(従来方法)。それぞれの酵素抽出液に対して、実施例1と同様のβ−グルクロニダーゼ酵素活性試験を行って酵素活性値(RLU/min)を求めると共に、コロニー試験による実際の大腸菌の検出・定量試験を行って、大腸菌数と酵素活性値との相関関係を調べた。結果を図16に示す。
【0101】
従来方法では試料溶液中の大腸菌を直接溶菌していたため、反応溶液に溶解性夾雑物が混入し、バックグランドノイズにより分析精度が低下して検出下限値が高くなった。これに対して、本発明方法によれば、大腸菌をメンブレンフィルター上に捕集し、界面活性剤による洗浄を行った後に、酵素活性試験を行うことにより、夾雑物が排除されて、図16に示すように検出下限値が1桁以上向上した。
【0102】
[実施例3]:界面活性剤洗浄による感度向上
本実施例では、細菌を捕集した濾過膜を界面活性剤で洗浄した後に酵素活性測定を行うことの有利性及びその場合の最適条件を検討する。
【0103】
はじめに、細菌を捕集した界面活性剤を用いて洗浄することによるバックグラウンドの低減効果を確認した。大腸菌が含まれていないことを前述のペトリフィルムを用いた測定であらかじめ確認してある環境水を超音波バスで分散させた後、No.5Aろ紙を用いて吸引ろ過した。ろ液を、孔径0.8μmのニトロセルロースメンブレンフィルターに通液した。同様の方法で、6検体試料を調製した。通液後のメンブレンフィルターに、Triton X−100を各々0vol%、0.005vol%、0.01vol%、0.02vol%、0.05vol%、0.1vol%含む溶液(洗浄液)を通液してフィルターを洗浄した後、フィルターの残留物に対して実施例1と同様の手順によってβ−グルクロニダーゼ酵素活性値(バックグランド)を求めた。結果を図17に示す。
【0104】
次に、界面活性剤を用いて洗浄することによる大腸菌の損失を調べた。下水処理場の初沈越流水から高濃度大腸菌を含む試料を採取し、滅菌希釈水で希釈することにより、大腸菌標準試料を作成した。この試料を超音波バスで分散させた後、No.5Aろ紙を用いて吸引ろ過した。ろ液を孔径0.8μmニトロセルロースメンブレンフィルターに通液して大腸菌を捕集した。同様の方法で、5検体試料を調製した。大腸菌が捕集されたメンブレンを、Triton X−100を各々0vol%、0.02vol%、0.05vol%、0.1vol%、0.2vol%含む溶液に含浸させ、含浸させた状態で5分間放置した後、実施例1と同様の手順によってこの浸漬液のβ−グルクロニダーゼ酵素活性値(大腸菌酵素活性値)を求めた。この酵素活性値を、洗浄によって損失する可能性のある大腸菌の量として評価した。結果を同様に図17に示す。
【0105】
図18より、十分なバックグラウンド低減効果を得るには、Triton X−100濃度を0.01vol%以上にする必要があった。一方、Triton X−100濃度が0.1vol%以上になると、損失する可能性のある大腸菌が増加した。したがって最適洗浄条件が得られる洗浄液のTriton X−100濃度は、0.01〜0.1vol%であることが分かる。
【0106】
[実施例4]:超音波を用いた溶菌処理
本発明において、大腸菌からβ−グルクロニダーゼを抽出する操作(溶菌処理)は、界面活性剤を用いても良いし、超音波を用いても良い。超音波を用いる場合でも、感度向上のため、反応液に界面活性剤を添加することが好ましい。
【0107】
下水処理場から採取した二次処理水を、超音波バスで分散させた後、No.5Aろ紙を用いて吸引ろ過した。ろ液を0.8μmメンブレンに通液し、大腸菌を捕集した。大腸菌が捕集されたメンブレンを、AMP=100watt、Pulse=1sec、Timer=1minの条件で超音波破砕し、β−グルクロニダーゼを抽出した(溶菌処理)。上澄液100μLを採取し、界面活性剤であるTriton X−100が最終濃度で各々0vol%、0.025vol%、0.5vol%、0.1vol%、0.3vol%、および0.5vol%となるように添加した後、実施例1と同じ酵素反応基質溶液180μLと混合した。実施例2と同様の手法により、恒温振とう機を用いて37℃で所定時間振とうさせた後に発光促進剤300μLを添加して発光を起こさせ発光量を測定して酵素活性値を求めた。界面活性剤濃度と酵素活性値の関係を図18に示した。
【0108】
超音波破砕によって溶菌処理を行い、酵素活性値を求める場合には、超音波処理後の試料に界面活性剤を添加することにより、添加しないときと比較して、最大で60%感度を向上させることができることが示される。また、この目的で界面活性剤を加える場合には、添加量としては、液中の界面活性剤濃度が0.01〜0.1vol%となるような量を加えることが好ましいことが分かる。
【0109】
[実施例5]:界面活性剤を用いて溶菌する際の最適条件:溶菌時間
界面活性剤を用いてグルクロニダーゼを抽出する(溶菌処理)場合は、一定の溶菌時間が必要である。
【0110】
下水処理場から採取した二次処理水を、超音波バスで分散させた後、No.5Aろ紙を用いて吸引ろ過した。ろ液を0.8μmメンブレンに通液し、大腸菌を捕集した。酵素の抽出溶液として、BSAを0.1wt%含むリン酸ナトリウム0.1M溶液にTriton X−100を0.1vol%加えた溶液を用い、大腸菌が捕集されたメンブレンをこの抽出溶液に浸漬して、37℃で0.5分間、5分間、10分間、15分間および30分間溶菌処理を行った。上澄液100μLを採取し、上述の酵素反応基質溶液180μLと混合した。実施例2と同様の手法により、恒温振とう機を用いて37℃で所定時間振とうさせた後に発光促進剤300μLを添加して発光を起こさせ発光量を測定して酵素活性値を求めた。溶菌時間と酵素活性値の関係を図19に示した。
【0111】
特許文献1で開示されている従来法では、界面活性剤と酵素反応基質を被検試料に同時に添加していた。この方法では、溶菌反応が十分に進まない状態で酵素反応を開始するため、抽出された酵素量と基質濃度のばらつきが大きくなり、十分な分析精度が得られなかった。本発明方法においては、大腸菌を十分に溶菌させた後に酵素反応基質を添加することで反応条件が一定になり、分析精度が大幅に向上した。
【0112】
[実施例6]:界面活性剤を用いて溶菌する際の最適条件:界面活性剤濃度
界面活性剤によって溶菌してグルクロニダーゼを抽出する場合は、Triton X−100の濃度を高くすることが好ましい。本実施例では、界面活性剤による溶菌効率と酵素反応阻害との関係を調べた。
【0113】
下水処理場から採取した二次処理水を、超音波バスで分散させた後、No.5Aろ紙を用いて吸引ろ過した。ろ液を0.8μmメンブレンに通液し、大腸菌を捕集した。酵素の抽出溶液として、BSAを0.1wt%含むリン酸ナトリウム0.1M溶液にTriton X−100を各々0vol%、0.025vol%、0.5vol%、0.1vol%、0.3vol%および0.5vol%加えた溶液を用い、大腸菌が捕集されたメンブレンをこの抽出溶液に浸漬し、37℃で30分間溶菌処理を行った。上澄液100μLを採取し、上述の酵素反応基質溶液180μLと混合した。実施例2と同様の手法により、恒温振とう機を用いて37℃で所定時間振とうさせた後に発光促進剤300μLを添加して発光を起こさせ発光量を測定して酵素活性値を求めた。Triton X−100濃度と酵素活性値の関係を図20に示す。溶菌効率と酵素反応阻害の関係から、最も高い酵素活性値が得られる最適Triton X−100の濃度は、0.2vol%前後であることが分かった。特許文献1に開示されている従来法では、界面活性剤としてTriton X−100を用いる場合は、濃度0.1vol%とされている。図20の結果から、Triton X−100の濃度を0.2vol%にしたことにより、感度が約2倍に向上したことが分かる。また、図20より好ましい溶菌剤としての界面活性剤濃度は0.15〜0.5vol%であることが分かる。
【0114】
[実施例7]
本実施例では、酵素反応基質と一緒に添加する場合の溶菌剤としての界面活性剤濃度の影響を調べた。
純水で10倍稀釈した下水10mLを、超音波バスで分散させた後、No.5Aろ紙を用いて吸引ろ過した。ろ液を0.8μmメンブレンに通液し、大腸菌を捕集した。そして、0.04vol%のTriton X-100を含む滅菌希釈水(栄研化学)10mLで2回を吸引濾過することにより、フィルターを洗浄した。さらに洗浄後のフィルターを試験管に挿入し、2mLの酵素基質液(0.1wt%牛血清アルブミン(BSA)、10mM EDTA、さらに1vol%グルクロン基質液を含むリン酸緩衝生理食塩水(日水製薬))に浸漬し、37℃で撹拌しながら反応を行った。この際、Triton X-100濃度を0.1〜0.8vol%に設定した。反応10分後と30分後に0.2mLの反応液を分取し、等量の発光促進剤(トロピクス(Tropix)社:商品名アクセラレーター2(Accelerator II))を添加して、2秒後の発光量を測定した。発光量の測定は、ルミノメータ(ベルトールド社製、LB-9507)を用いて行った。結果を図21に示す。酵素活性値とTriton X-100濃度の関係から、高い酵素活性値を得るためのTriton X-100の濃度は高い方が好ましく、好ましい界面活性剤濃度は0.1〜0.8vol%の間であった。
【0115】
[実施例8]:大腸菌の迅速・高感度測定
本発明によるβ−グルクロニダーゼ活性測定法において、メンブレンフィルターによる濃縮と膜の洗浄を組み合わせることにより、大腸菌測定を迅速化、高感度化できることを示す。
試料には、下水処理場の最初沈殿池越流水と二次処理水を採取し、直ちに測定に供した。培養法(コロニー計数法)による大腸菌数は、3M社製ペトリフィルム「E−coli・大腸菌群数測定用ECプレート」を用い、試料を37℃で20時間培養した後、β−グルクロニダーゼに対する特定酵素基質であるX−gluと反応して青色コロニーを形成して且つガス産生の有るものを大腸菌として計数した。その結果、最初沈殿池越流水中の大腸菌数は、9.1×104CFU/mL、二次処理水中の大腸菌数は、2.3×102CFU/mLであった。
【0116】
まず初めに、この二次処理水の酵素活性値を測定した。二次処理水100mLは、No.5A濾紙を用いて吸引濾過し、そのろ液を孔径1.0μmの混合セルロースエステル製メンブレンフィルター(直径25mm)により濾過することで、細菌をフィルター上に捕集した。そして、0.04vol%のTriton X−100を含む滅菌希釈水(栄研化学)10mLで2回を吸引濾過することにより、フィルターを洗浄した。そして、洗浄後のフィルターを直径30mmの透明ガラス製バイアル内に濾過面が下になるように置き、そこに1mLの酵素基質液(0.1wt%牛血清アルブミン(BSA)、0.1vol%Triton X−100、10m MEDTA、さらに1vol%グルクロン基質液を含むリン酸緩衝生理食塩水(日水製薬))に浸漬し、37℃で攪拌しながら反応を行った。酵素反応10分後、20分後、30分後に、各反応液300μLを採取し、発光促進剤(トロピクス(Tropix)社:商品名アクセラレーター2(Accelerator II))300μLを添加して、2秒後の発光量を測定した。発光量の測定は、ルミノメータ(ベルトールド社製、LB−9507)を用いて行った。各試料における振とう時間(酵素基質反応時間)に対する相対発光量(RLU: Relative Light Unit)をグラフ上にプロットし、求めた直線の傾きを酵素活性値(β−グルクロニダーゼ活性値)とした。
【0117】
図22には、上記のようにして作成した振とう時間(酵素基質反応時間)に対する相対発光量(RLU: Relative Light Unit)のグラフの一例を示す。図22のグラフでは、酵素活性値(直線の傾き)は996RLU/minであった。溶菌処理と酵素反応を同時に行う場合でも、反応時間に応じて発光量が増加した。
【0118】
次に大腸菌を含まない下水処理場の高度処理水に先の最初沈殿池越流水を0.0001〜1vol%添加することにより、所定濃度の大腸菌を含む試料を調製し、先に示した方法(図22と同様の方法)で10分から30分まで間における発光量の変化をβ−グルクロニダーゼ活性値として測定した。
【0119】
同じ試料について、培養法(コロニー計数法)により大腸菌数を測定し、この酵素活性値との相関関係を図23のように示した。
図23に示したとおり、酵素活性値は培養法による大腸菌数0.09CFU/mL〜91CFU/mLの範囲で非常に良好な直線関係が得られた。また、大腸菌の定量下限値が従来方法(非特許文献3に開示の方法)の1.0×103CFU/mLから10000倍以上向上した。次に同様の手法によって、実際の下水処理場の最終沈殿池越流水2検体、消毒処理水1検体について酵素活性値を測定し、この検量線を用いて大腸菌濃度を算出した。その結果を表3に示す。
【表3】

本発明の方法で測定した大腸菌濃度は、培養法で測定した大腸菌数と一致した。さらに、図23の検量線に用いた試料の溶菌酵素反応10分後、20分後、および30分後の発光量と培養法による大腸菌数の関係を図24に示した。溶菌酵素反応10〜30分後の発光量も酵素活性値と同様に大腸菌濃度と高い相関関係を示すことから、10分後の発光量をもって大腸菌数を測定できることが分かった。
【0120】
[実施例9]
次に、より簡易に大腸菌数を測定するため、酵素反応を行う容器内においてフィルターを浸漬した状態で発光量を測定する手法を検討した。
実施例8と同様に細菌を捕集したフィルターを浸漬し、30分間酵素反応を行ったバイアルに直接、発光促進剤(トロピクス(Tropix)社:商品名アクセラレーター2(Accelerator II))1mLを添加して、2秒後の発光量を測定した。このとき、発光量の測定は、直径30mmのバイアルを直接測定できるルミノメータ(マイクロテックニチオン社製、ルミカウンター2500A)を用いて、バイアルの下方よりフィルター全面を測光することにより行った。また、30分間酵素反応後の同反応液300μLを試験管に分取して、300μLの発酵促進剤を加えた系についても、同様に発光量を測定した。
【0121】
結果を図25に示すが、フィルターを含む反応液でも、培養法による大腸菌数と高い相関性を示した。さらに、前試料を発光測定に供する上、フィルター面による光の反射効果により、高濃度側の発光量がさらに増幅され、バックグラウンドも低下するために、より高精度で測定できることが見出された。これまでの蛍光法による酵素活性測定では、励起光の透過を妨害するフィルターを浸漬した試料を測定することは困難であったが、本発光測定法を用いることにより、フィルターを浸漬した状態の反応液の発光量を直接測定することが可能となり、より簡便、かつ高精度に測定することが可能になった。
【0122】
[実施例10]:下水処理場処理水を用いた実証試験
下水処理場から採取した二次処理水および好気性ろ床出口水を、超音波バスで分散させた後、No.5Aろ紙を用いて吸引ろ過した。ろ液を0.8μmメンブレンに通液し、大腸菌を捕集した。酵素の抽出溶液として、BSAを0.1wt%含むリン酸ナトリウム0.1M溶液にTriton X−100を0.2vol%加えた溶液を用い、この溶液に大腸菌が捕集されたメンブレンを浸漬し、37℃で30分間溶菌処理を行った。上澄液100μLを採取し、上述の酵素反応基質溶液180μLと混合した。実施例2と同様の手法により、恒温振とう機を用いて37℃で所定時間振とうさせた後に発光促進剤300μLを添加して発光を起こさせ発光量を測定して酵素活性値を求めた。これとは別に、同じ試料中の真の大腸菌数を培養法(コロニー計数法)で求めた。培地としては、3M社製ペトリフィルム「E−coli・大腸菌群数測定用ECプレート」を用いた。試料を37℃で20時間培養した後、β−グルクロニダーゼに対する特定酵素基質であるX−gluと反応して青色コロニーを形成して且つガス産生の有るものを大腸菌として計数した。
【0123】
以上の手法によって求められた大腸菌数(コロニー計数値)とβ−グルクロニダーゼ活性値との相関関係を図26に示す。
図26の結果を統計学的に解析した結果、95%信頼区間が実用的な範囲に収束した。本発明によれば、簡便且つ迅速且つ高感度なことに加え、測定精度も向上した結果、低濃度の大腸菌から高濃度の大腸菌まで精確に菌数を算出することが可能になった。
【0124】
[実施例11]:β−グルクロニダーゼ活性に基づく大腸菌群数の測定
下水処理場の二次処理水および好気性ろ床出口水に対して、本発明による方法を適用した。被検試料水を超音波バスで分散させた後、No.5Aろ紙を用いて吸引ろ過した。ろ液を0.8μmのメンブレンに通液して、大腸菌を捕集した。大腸菌が捕集されたメンブレンを、Triton X−100を0.2vol%含む抽出溶液に含浸させ、37℃で30分間溶菌した。上澄液100μLを採取し、グルクロン(登録商標)1vol%,リン酸ナトリウム0.1M、EDTA10mMからなる基質溶液180μLと混合した。実施例2と同様の手法により、恒温振とう機を用いて37℃で所定時間振とうさせた後に発光促進剤300μLを添加して発光を起こさせ発光量を測定して酵素活性値を求めた。
【0125】
これとは別に真の大腸菌群数を培養法(コロニー計数法)で求めた。培地としては、3M社製ペトリフィルム「E−coli・大腸菌群数測定用ECプレート」を用いた。試料を37℃で20時間培養した後、β−ガラクトシダーゼに対する特定酵素基質であるX−galと反応して赤色コロニーを形成して且つガス産生の有るものを大腸菌群として計数した。
【0126】
以上の手法によって求められた大腸菌群数(コロニー計数値)と酵素活性値(β−グルクロニダーゼ活性値)との相関を、図27に示した。
図27より、β−グルクロニダーゼ活性値と大腸菌群数とは直線的な相関関係があることが分かる。この結果から、β−グルクロニダーゼ活性値を測定すれば、大腸菌群を算出可能なことが実証された。
【0127】
[実施例12]:海水を用いた実証試験
本発明の好ましい態様では、濾過膜で捕集した細菌を界面活性剤で洗浄しているため、酵素反応が溶液の組成による阻害を受けない。したがって、本発明の好ましい態様によれば、例えば海水のような高濃度塩分を含む試料でも迅速・高感度測定が可能なことを本実施例で示す。
【0128】
雨天時合流式下水道越流水の影響で大腸菌濃度が高くなった海水を用いて、本発明による方法を適用した。被検試料水100mLを超音波バスで分散させた後、No.5Aろ紙を用いて吸引ろ過した。ろ液を1.0μmのメンブレンフィルターに通液して、大腸菌を捕集した。大腸菌が捕集されたメンブレンに10mLの0.02vol%のTritonX−100を含む溶液を2回通水することによってフィルター洗浄を行った。
【0129】
次に、メンブレンをTriton X−100を0.2vol%含む抽出溶液に含浸させ、37℃で30分間溶菌した。上澄液100μLを採取し、グルクロン(登録商標)1%,リン酸ナトリウム0.1M、EDTA10mMからなる基質溶液180μLと混合した。実施例2と同様の手法により、恒温振とう機を用いて37℃で所定時間振とうさせた後に発光促進剤300μLを添加して発光を起こさせ発光量を測定して酵素活性値を求めた。
【0130】
これとは別に真の大腸菌数を培養法(コロニー計数法)で求めた。培地としては、3M社製ペトリフィルム「E−coli・大腸菌群数測定用ECプレート」を用いた。試料を37℃で20時間培養した後、β−グルクロニダーゼに対する特定酵素基質であるX−gluと反応して青色コロニーを形成して且つガス産生の有るものを大腸菌として計数した。
【0131】
以上の手法によって求められた大腸菌群数(コロニー計数値)と酵素活性値(β−グルクロニダーゼ活性値)との相関を、図28に示した。
図28より、β−グルクロニダーゼ活性値に基づく大腸菌数の測定が、海水に影響されず、低濃度まで直線的な相関関係があることが分かる。この結果から、本発明の好ましい態様にかかる方法によれば、濾過膜で捕集した細菌を界面活性剤で洗浄しているため、酵素反応が溶液の組成による阻害を受けないことが実証された。
【0132】
[実施例13]:海水を用いた実証試験
雨天時合流式下水道越流水の影響で大腸菌濃度が高くなった海水を用いて、本発明による方法を適用した。被検試料水100mLを超音波バスで分散させた後、No.5Aろ紙を用いて吸引ろ過した。ろ液を1.0μmのニトロセルロース製メンブレンフィルターに通液して、大腸菌を捕集した。大腸菌が捕集されたメンブレンに10mLの0.02vol%のTriton X−100を含む溶液を2回通水することによってフィルター洗浄を行った。次に、メンブレンを2mlの溶菌酵素基質液(0.1wt%牛血清アルブミン(BSA)、0.1vol%Triton X−100、10m MEDTA、さらに1vol%グルクロン基質液(アプライドバイオシステムズ社)を含むリン酸緩衝生理食塩水(日水製薬))抽出溶液に含浸させ、37℃で30分間酵素反応を行った。酵素反応10分後、20分後、30分後に、各反応液300μLを採取し、発光促進剤300μLを添加して発光を起こさせ、2秒後の発光量を測定して酵素活性値を求めた。
【0133】
これとは別に真の糞便性大腸菌数を培養法(コロニー計数法)で求めた。100mLの試料を滅菌したHAフィルター(Millipore)でろ過し、ろ過したフィルターをm−FC倍地(Millipore m-FC Broth)を浸み込ませたパットを含むプラスチックシャーレに入れて、44.5℃で22時間培養した。そして、形成したコロニーをふん便性大腸菌群数として計数した。
【0134】
以上の手法によって求められた糞便性大腸菌群数(コロニー計数値)と酵素活性値(β−グルクロニダーゼ活性値)との相関を、図29に示す。
図29より、β−グルクロニダーゼ活性値に基づく糞便性大腸菌数の測定が、海水に影響されず、低濃度まで直線的な相関関係があることが分かる。本発明によれば、簡便且つ迅速且つ高感度なことに加え、測定精度も向上した結果、低濃度の大腸菌から高濃度の大腸菌まで精確に菌数を算出することが可能になった。
この結果から、本発明の好ましい態様にかかる方法によれば、濾過膜で捕集した細菌を界面活性剤で洗浄しているため、酵素反応が溶液の組成による阻害を受けないことが実証された。
【産業上の利用可能性】
【0135】
大腸菌は、衛生学的指標として重要であり、さまざまな迅速測定法が提唱されてきた。
しかし、いずれも測定法に問題があり、実用に適さなかった。同等の迅速性(測定時間約1時間)を持つ従来技術(非特許文献3)と比較すると、本発明の方法は感度が40倍〜1000倍以上向上した。また、同等の感度(1CFU/mL)を有する従来技術(特許文献2)と比較すると、測定時間が1/6.5〜1/38に短縮された。本発明は、放流基準値の判定に適する、衛生学的指標の算出方法として実用可能な初めての測定方法である。従来のコロニー計数による菌数測定では、測定に24時間を要していた。そのため、実際には菌数が放流基準値以内であっても、安全のために塩素添加、UV照射、オゾン処理等で殺菌処理を行ってきた。また、従来の迅速測定法では、測定精度が低いため、測定結果を衛生学的指標として用いることが出来ず、安全性が判定できなかった。そのため、これらの殺菌処理を省略することができなかった。しかし、塩素処理やオゾン処理に伴う副生成物が環境に悪いことが近年指摘されている。また、UV照射およびオゾン処理は処理に大きなエネルギーが必要となる。本発明を用いて大腸菌・大腸菌群を迅速に測定すれば、必要な場合だけ殺菌処理を行えば良いことになり、環境保護および省エネルギーに対する効果が大きい。
【0136】
また、本発明は、下水の性状分析のみならず、飲料水等の上水の性状分析(水中の大腸菌数、大腸菌群数などの測定)にも利用することができる。
【図面の簡単な説明】
【0137】
【図1】図1は、本発明方法を実施するための装置の一例の構成を示す図である。
【図2】図2は、本発明方法を実施するための装置の他の形態の構成を示す図である。
【図3】図3は、本発明方法を実施するための装置の他の形態の構成を示す図である。
【図4】図4は、本発明方法を実施するための装置の構成を示す図である。
【図5】図5は、本発明方法を実施するための装置の構成を示す図である。
【図6】図6は、本発明方法を実施するための装置の構成を示す図である。
【図7】図7は、本発明方法を実施するための装置の構成を示す図である。
【図8】図8は、本発明方法を実施するための装置の構成を示す図である。
【図9】図9は、捕集反応装置の一具体例を示す。
【図10】図10は、本発明方法を実施するための装置の構成を示す図である。
【図11】図11は、本発明の測定キットの具体例を示す。
【図12】図12は、実施例1において測定された各種メンブレンフィルターの孔径と細菌捕集効率との関係を示すグラフである。
【図13】図13は、実施例1において測定された各種メンブレンフィルターの孔径と酵素活性値の相対バックグラウンドとの関係を示すグラフである。濾過前の試料に対して同様の酵素活性試験を行うことによって測定された酵素活性値(バックグラウンド)を100%として、これに対する酵素活性値の相対値を相対バックグラウンドとして示した。
【図14】図14は、実施例2で測定された、酵素基質反応時間に対する相対発光量(RLU: Relative Light Unit)のグラフの一つである。反応時間を横軸に、相対発光量を縦軸にプロットし、直線の傾きから酵素活性値を求める。
【図15】図15は、実施例2で測定された、被検試料中の大腸菌数(コロニー計数値)と、本発明方法によって測定されたβ−グルクロニダーゼ活性値との関係を示すグラフである。
【図16】図16は、メンブレン捕集による検出限界値の向上を示すグラフである。
【図17】図17は、実施例3において測定された本発明方法における界面活性剤による濾過膜捕集物の洗浄条件の最適条件を示すグラフである。
【図18】図18は、実施例4で測定された、超音波による溶菌処理を行った酵素活性試験における界面活性剤添加量と酵素活性感度との関係を示すグラフである。
【図19】図19は、実施例5で測定された、界面活性剤による溶菌処理を行った酵素活性試験における溶菌時間と酵素活性感度との関係を示すグラフである。
【図20】図20は、実施例6で測定された、界面活性剤による溶菌処理を行った酵素活性試験における界面活性剤添加量と酵素活性感度との関係を示すグラフである。
【図21】図21は、実施例7で測定された、酵素反応基質と溶菌剤(界面活性剤)とを一緒に添加した場合の界面活性剤添加量と酵素活性感度との関係を示すグラフである。
【図22】図22は、実施例8で測定された、振とう時間(酵素基質反応時間)に対する相対発光量(RLU: Relative Light Unit)のグラフの一例を示す。
【図23】図23は、実施例8で測定された、被検試料中の大腸菌数(コロニー計数値)と、本発明方法によって測定されたβ−グルクロニダーゼ活性値との関係を示すグラフである。
【図24】図24は、一定時間後の発光量と大腸菌濃度との関係を示すグラフである。
【図25】図25は、直接測光と分取測光による発光量と大腸菌数との関係を示すグラフである。
【図26】図26は、実施例10で測定された、被検試料中の大腸菌群数とβ−グルクロニダーゼ活性値(相対発光量)との相関関係を示すグラフである。
【図27】図27は、実施例11で測定された、被検試料中の大腸菌群数と、本発明方法によって測定されたβ−グルクロニダーゼ活性値との関係を示すグラフである。
【図28】図28は、実施例12で測定された、海水試料中の大腸菌数と、本発明方法によって測定されたβ−グルクロニダーゼ活性値との関係を示すグラフである。
【図29】図29は、実施例13で測定された、海水試料中の糞便性大腸菌群数と、本発明方法によって測定されたβ−グルクロニダーゼ活性値との関係を示すグラフである。
【符号の説明】
【0138】
1:被検試料
2:捕集容器
3:溶菌剤
4:反応容器
5:酵素反応基質液
6:促進剤
7:測定装置
11:濾過膜
12:パージ用流体供給機構
13:試料液供給機構
14:酵素反応基質液供給機構
15:洗浄剤供給機構
17:捕集容器
18:恒温槽
32:促進剤供給機構
33:酵素活性値測定装置(ルミノメータ)
37:反応容器
41:目皿
50:循環ライン
【特許請求の範囲】
【請求項1】
孔径0.6〜5.0μmの濾過膜及び/又はASTM F317-72で測定した場合の蒸留水通水流量が50〜500mL/min・cm2である濾過膜に試料液を通水することによって試料液中の細菌を濾過膜上に捕集し、該濾過膜を溶菌剤及び酵素反応基質に接触させ、ターゲット細菌中酵素の酵素反応基質に対する酵素活性値を求めることによって、試料液中の細菌数を定量することを特徴とする細菌の検出方法。
【請求項2】
前記濾過膜は、孔径0.8〜3.0μmのニトロセルロースメンブレンであることを特徴とする請求項1に記載の方法。
【請求項3】
前記濾過膜を溶菌剤及び酵素反応基質に接触させる前に、該濾過膜に界面活性剤を通水することによって該濾過膜を洗浄することを特徴とする請求項1又は2に記載の方法。
【請求項4】
前記濾過膜と溶菌剤及び酵素反応基質との接触は、溶菌剤と酵素反応基質を濾過膜に同時に接触させることを特徴とする請求項1〜3の何れか1項に記載の方法。
【請求項5】
前記濾過膜と溶菌剤及び酵素反応基質との接触は、まず濾過膜を溶菌剤に接触させて酵素を抽出し、次いで抽出された酵素を酵素反応基質と接触させることを特徴とする請求項1〜3の何れか1項に記載の方法。
【請求項6】
測定対象の細菌が大腸菌、大腸菌群及び/又は糞便性大腸菌群であり、大腸菌から抽出されるβ−グルクロニダーゼの酵素活性値に基づいて試料液中の大腸菌数を定量する請求項1〜5のいずれか1項に記載の方法。
【請求項7】
酵素反応基質として3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−グルクロニドまたはその誘導体を用いる、請求項6に記載の方法。
【請求項8】
さらに、発光促進剤を添加して、発光性化合物の化学発光量を測定することにより酵素活性値を決定することを特徴とする請求項1〜7の何れか1項に記載の方法。
【請求項9】
孔径0.6〜5.0μmの濾過膜及び/又はASTM F317-72で測定した場合の蒸留水通水流量が50〜500mL/min・cm2である濾過膜を収容する捕集容器と、
該濾過膜の一次側に試料液を供給する試料液供給機構と、
酵素反応基質を供給する酵素反応基質供給機構と、
酵素活性値を測定する酵素活性値測定装置と、
を含む細菌の検出装置
【請求項10】
発光促進剤を供給する発光促進剤供給装置を更に具備する、請求項9に記載の装置。
【請求項11】
前記濾過膜は、孔径0.8〜3.0μmのニトロセルロースメンブレンであることを特徴とする請求項9又は10に記載の装置。
【請求項12】
前記酵素反応基質供給装置は、溶菌剤も供給することを特徴とする請求項9〜11の何れか1項に記載の装置。
【請求項13】
前記捕集容器に溶菌剤を供給する溶菌剤供給装置をさらに具備することを特徴とする請求項9〜11の何れか1項に記載の装置。
【請求項14】
孔径0.6〜5.0μmの濾過膜及び/又はASTM F317-72で測定した場合の蒸留水通水流量が50〜500mL/min・cm2である濾過膜を収容する濾過装置を具備する捕集ユニットと、捕集ユニットから供給される液を受容して酵素基質反応を行う反応ユニットとから構成され、捕集ユニットは、濾過膜の一次側に試料液を供給する試料供給装置、濾過膜の一次側に洗浄液を供給する洗浄液供給装置、細菌を捕集した濾過膜から細菌中の酵素を抽出する手段、抽出処理によって得られる酵素抽出液を反応ユニットに送る手段を具備し、反応ユニットは、捕集ユニットから供給される酵素抽出液に酵素反応基質を供給する酵素反応基質添加装置、酵素反応基質が添加された反応液に促進剤を加える促進剤添加装置、促進剤が加えられた反応液の発光又は蛍光又は発色の量を測定する測定装置を具備する、試料液中の細菌を検出するための装置。
【請求項15】
前記濾過膜は、孔径0.8〜3.0μmのニトロセルロースメンブレンであることを特徴とする請求項14に記載の装置。
【請求項16】
孔径0.6〜5.0μmの濾過膜及び/又はASTM F317-72で測定した場合の蒸留水通水流量が50〜500mL/min・cm2である濾過膜を収容する濾過装置、濾過膜の一次側に試料液を供給する試料供給装置、濾過膜の一次側に洗浄液を供給する洗浄液供給装置、溶菌酵素反応基質を供給する溶菌酵素反応基質添加装置、濾過膜を浸漬した状態で溶菌酵素反応基質液を一定温度に保持する恒温装置により構成される濾過反応ユニットと、酵素反応後の反応液を測定装置に送る手段を具備し、測定装置に供給する酵素反応後の反応液に促進剤を加える促進剤添加装置、促進剤が加えられた反応液の発光又は蛍光又は発色の量を測定する測定ユニットを具備する、試料液中の細菌を検出するための装置。
【請求項17】
前記濾過膜は、孔径0.8〜3.0μmのニトロセルロースメンブレンであることを特徴とする請求項16に記載の装置。
【請求項18】
ターゲット細菌が大腸菌及び/又は大腸菌群である、請求項9〜17の何れか1項に記載の装置。
【請求項19】
供給口及び排出口を具備するケーシング内に、孔径0.6〜5.0μmの濾過膜及び/又はASTM F317-72で測定した場合の蒸留水通水流量が50〜500mL/min・cm2である濾過膜を収容する捕集容器と、
酵素反応基質液供給ユニットと、
酵素活性値を測定する酵素活性値測定装置と、
を含む細菌簡易測定キット
【請求項20】
洗浄液供給ユニット及び/又は発光促進剤供給ユニットをさらに具備する、請求項19に記載の細菌簡易測定キット。
【請求項21】
溶菌剤供給ユニットをさらに具備する、請求項19又は20に記載の細菌簡易測定キット。
【請求項22】
前記酵素反応基質液供給ユニットは、溶菌剤及び酵素反応基質液を含む、請求項19又は20に記載の細菌簡易測定キット。
【請求項23】
前記濾過膜は、孔径0.8〜3.0μmのニトロセルロースメンブレンであることを特徴とする請求項19〜22の何れか1項に記載の細菌簡易測定キット。
【請求項24】
ターゲット細菌が大腸菌及び/又は大腸菌群である請求項19〜23の何れか1項に記載の簡易測定キット。
【請求項1】
孔径0.6〜5.0μmの濾過膜及び/又はASTM F317-72で測定した場合の蒸留水通水流量が50〜500mL/min・cm2である濾過膜に試料液を通水することによって試料液中の細菌を濾過膜上に捕集し、該濾過膜を溶菌剤及び酵素反応基質に接触させ、ターゲット細菌中酵素の酵素反応基質に対する酵素活性値を求めることによって、試料液中の細菌数を定量することを特徴とする細菌の検出方法。
【請求項2】
前記濾過膜は、孔径0.8〜3.0μmのニトロセルロースメンブレンであることを特徴とする請求項1に記載の方法。
【請求項3】
前記濾過膜を溶菌剤及び酵素反応基質に接触させる前に、該濾過膜に界面活性剤を通水することによって該濾過膜を洗浄することを特徴とする請求項1又は2に記載の方法。
【請求項4】
前記濾過膜と溶菌剤及び酵素反応基質との接触は、溶菌剤と酵素反応基質を濾過膜に同時に接触させることを特徴とする請求項1〜3の何れか1項に記載の方法。
【請求項5】
前記濾過膜と溶菌剤及び酵素反応基質との接触は、まず濾過膜を溶菌剤に接触させて酵素を抽出し、次いで抽出された酵素を酵素反応基質と接触させることを特徴とする請求項1〜3の何れか1項に記載の方法。
【請求項6】
測定対象の細菌が大腸菌、大腸菌群及び/又は糞便性大腸菌群であり、大腸菌から抽出されるβ−グルクロニダーゼの酵素活性値に基づいて試料液中の大腸菌数を定量する請求項1〜5のいずれか1項に記載の方法。
【請求項7】
酵素反応基質として3−(4−メトキシスピロ{1,2−ジオキセタン−3,2’−(5’−クロロ)−トリシクロ−[3.3.1.13,7]デカン}−4−イル)フェニル−β−D−グルクロニドまたはその誘導体を用いる、請求項6に記載の方法。
【請求項8】
さらに、発光促進剤を添加して、発光性化合物の化学発光量を測定することにより酵素活性値を決定することを特徴とする請求項1〜7の何れか1項に記載の方法。
【請求項9】
孔径0.6〜5.0μmの濾過膜及び/又はASTM F317-72で測定した場合の蒸留水通水流量が50〜500mL/min・cm2である濾過膜を収容する捕集容器と、
該濾過膜の一次側に試料液を供給する試料液供給機構と、
酵素反応基質を供給する酵素反応基質供給機構と、
酵素活性値を測定する酵素活性値測定装置と、
を含む細菌の検出装置
【請求項10】
発光促進剤を供給する発光促進剤供給装置を更に具備する、請求項9に記載の装置。
【請求項11】
前記濾過膜は、孔径0.8〜3.0μmのニトロセルロースメンブレンであることを特徴とする請求項9又は10に記載の装置。
【請求項12】
前記酵素反応基質供給装置は、溶菌剤も供給することを特徴とする請求項9〜11の何れか1項に記載の装置。
【請求項13】
前記捕集容器に溶菌剤を供給する溶菌剤供給装置をさらに具備することを特徴とする請求項9〜11の何れか1項に記載の装置。
【請求項14】
孔径0.6〜5.0μmの濾過膜及び/又はASTM F317-72で測定した場合の蒸留水通水流量が50〜500mL/min・cm2である濾過膜を収容する濾過装置を具備する捕集ユニットと、捕集ユニットから供給される液を受容して酵素基質反応を行う反応ユニットとから構成され、捕集ユニットは、濾過膜の一次側に試料液を供給する試料供給装置、濾過膜の一次側に洗浄液を供給する洗浄液供給装置、細菌を捕集した濾過膜から細菌中の酵素を抽出する手段、抽出処理によって得られる酵素抽出液を反応ユニットに送る手段を具備し、反応ユニットは、捕集ユニットから供給される酵素抽出液に酵素反応基質を供給する酵素反応基質添加装置、酵素反応基質が添加された反応液に促進剤を加える促進剤添加装置、促進剤が加えられた反応液の発光又は蛍光又は発色の量を測定する測定装置を具備する、試料液中の細菌を検出するための装置。
【請求項15】
前記濾過膜は、孔径0.8〜3.0μmのニトロセルロースメンブレンであることを特徴とする請求項14に記載の装置。
【請求項16】
孔径0.6〜5.0μmの濾過膜及び/又はASTM F317-72で測定した場合の蒸留水通水流量が50〜500mL/min・cm2である濾過膜を収容する濾過装置、濾過膜の一次側に試料液を供給する試料供給装置、濾過膜の一次側に洗浄液を供給する洗浄液供給装置、溶菌酵素反応基質を供給する溶菌酵素反応基質添加装置、濾過膜を浸漬した状態で溶菌酵素反応基質液を一定温度に保持する恒温装置により構成される濾過反応ユニットと、酵素反応後の反応液を測定装置に送る手段を具備し、測定装置に供給する酵素反応後の反応液に促進剤を加える促進剤添加装置、促進剤が加えられた反応液の発光又は蛍光又は発色の量を測定する測定ユニットを具備する、試料液中の細菌を検出するための装置。
【請求項17】
前記濾過膜は、孔径0.8〜3.0μmのニトロセルロースメンブレンであることを特徴とする請求項16に記載の装置。
【請求項18】
ターゲット細菌が大腸菌及び/又は大腸菌群である、請求項9〜17の何れか1項に記載の装置。
【請求項19】
供給口及び排出口を具備するケーシング内に、孔径0.6〜5.0μmの濾過膜及び/又はASTM F317-72で測定した場合の蒸留水通水流量が50〜500mL/min・cm2である濾過膜を収容する捕集容器と、
酵素反応基質液供給ユニットと、
酵素活性値を測定する酵素活性値測定装置と、
を含む細菌簡易測定キット
【請求項20】
洗浄液供給ユニット及び/又は発光促進剤供給ユニットをさらに具備する、請求項19に記載の細菌簡易測定キット。
【請求項21】
溶菌剤供給ユニットをさらに具備する、請求項19又は20に記載の細菌簡易測定キット。
【請求項22】
前記酵素反応基質液供給ユニットは、溶菌剤及び酵素反応基質液を含む、請求項19又は20に記載の細菌簡易測定キット。
【請求項23】
前記濾過膜は、孔径0.8〜3.0μmのニトロセルロースメンブレンであることを特徴とする請求項19〜22の何れか1項に記載の細菌簡易測定キット。
【請求項24】
ターゲット細菌が大腸菌及び/又は大腸菌群である請求項19〜23の何れか1項に記載の簡易測定キット。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【図27】


【図28】


【図29】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【図27】


【図28】


【図29】


【公開番号】特開2007−37536(P2007−37536A)
【公開日】平成19年2月15日(2007.2.15)
【国際特許分類】
【出願番号】特願2006−168893(P2006−168893)
【出願日】平成18年6月19日(2006.6.19)
【出願人】(000000239)株式会社荏原製作所 (1,477)
【Fターム(参考)】
【公開日】平成19年2月15日(2007.2.15)
【国際特許分類】
【出願日】平成18年6月19日(2006.6.19)
【出願人】(000000239)株式会社荏原製作所 (1,477)
【Fターム(参考)】
[ Back to top ]

