酸可溶性亜鉛を高含有する野菜
【課題】野菜の葉又は果実等の可食物中に酸可溶性亜鉛を高濃度含有する野菜、及びその製造法を提供する。
【解決手段】亜鉛を含有する液をホウレンソウ、キャベツ、又はトマトの葉面に散布することにより、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するホウレンソウ、地上部に酸可溶性亜鉛を5mg/100g(乾燥重)以上含有するキャベツ、又は果実中に酸可溶性酸可溶性亜鉛を0.15mg/100g(新鮮重)以上含有するトマトを製造する。
【解決手段】亜鉛を含有する液をホウレンソウ、キャベツ、又はトマトの葉面に散布することにより、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するホウレンソウ、地上部に酸可溶性亜鉛を5mg/100g(乾燥重)以上含有するキャベツ、又は果実中に酸可溶性酸可溶性亜鉛を0.15mg/100g(新鮮重)以上含有するトマトを製造する。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、可食部中に酸可溶性亜鉛を高濃度含有し、ヒト、動物の食品または食品材料として有用な野菜、及びその製造法に関する。
【背景技術】
【0002】
近年、食生活の変化等により、種々の栄養素の不足が懸念されており、亜鉛(Zn)等の微量金属もその一つである。亜鉛は、人体内中で微量金属元素としては鉄についで多く含まれており、代謝系で重要な役割を担っていることが知られている(特許文献1)。亜鉛は、牡蠣中には13.2mg/100g、牛レバーには3.8mg/100g含有されていることが知られているが(非特許文献1)、これらのように亜鉛を多く含む食品は限られており、現在の食習慣で亜鉛を所要量摂取することは困難である。
【0003】
植物中の亜鉛含量を高める技術が種々提案されている。例えば、ライムギにおいてシロイヌナズナ由来の亜鉛トランスポーター遺伝子を過剰発現させる方法が開発されている(非特許文献2)。しかしながら、この遺伝子組換体の亜鉛吸収速度は高くはない。
【0004】
また、豆類(特許文献1)、イモ類(特許文献2)、イネ(特許文献3)、トウモロコシ(特許文献4)、ソバ(特許文献5)、コムギ(特許文献7)のような穀類、又は直根類(特許文献6)等の植物の葉面等に亜鉛含有液を散布することによって、植物の子実や根の亜鉛含量を高める方法が提案されている。また、これらの亜鉛含有液に海藻抽出物を含有させることによって、子実等への亜鉛移行率が向上することが報告されている(特許文献1〜7)。亜鉛の葉面散布自体は、土壌に亜鉛を大量に施肥した場合に生じるとされている、土壌中の鉄の吸収移動を阻害し、鉄欠乏症状を引き起こしてしまう(重金属誘導クロロシス)という問題(非特許文献3)が生じないため好ましい。しかしながら、前記方法では、植物の子実中の亜鉛含有量の上昇はわずかである。また、一般的に、ヒト等の動物が吸収可能な亜鉛は、食品等から酸で可溶化する亜鉛である(非特許文献4、5、6)が、穀物中の亜鉛はフィチン酸に強固に結合しているので、ヒトが栄養として吸収するのは困難である(非特許文献7、8、9)。
【0005】
一方、亜鉛を土壌に大量に施肥すると、土壌中の鉄の吸収移動を阻害し、鉄欠乏症状を引き起こしてしまう(重金属誘導クロロシス)という問題(熊沢・西沢1976.植物の養分吸収.東京大学出版会)がある。また、例えば日本においては、平成15年の環境基本法改正により河川や海水中の亜鉛濃度基準が10〜30μg/L以下と設定されているが、土壌に大量に亜鉛を施用すると、河川等への流亡も環境保全上問題となる。
【0006】
日本において日常的に摂取する食習慣を有する植物として、ホウレンソウ、コマツナ等の野菜がある。これらは冷凍食品等の加工食品中にも多く含まれ、ほぼ毎日無理なく摂取できる食材といえる。この点から野菜における亜鉛等の微量金属元素の含有量を高めることができれば有用と考えられるが、亜鉛等のミネラルは葉から転流される(非特許文献10、11)ため、欠乏症状が現れた栽培初期、中期(収穫の数週間以上前)に葉面散布を実施する従来の散布方法では、葉中に高濃度で蓄積させることは困難であった。
【先行技術文献】
【特許文献】
【0007】
【特許文献1】特開2008−161099
【特許文献2】特開2008−263891
【特許文献3】特開2008−263892
【特許文献4】特開2008−263893
【特許文献5】特開2008−263894
【特許文献6】特開2008−263895
【特許文献7】特開2008−263896
【非特許文献】
【0008】
【非特許文献1】「五訂増補日本食品標準成分表」文部科学省科学技術・学術審議会・資源調査分科会(http://www.mext.go.jp/b_menu/shingi/gijyutu/gijyutu3/toushin/05031802.htm)
【非特許文献2】Ramesh, et al. 2004 Plant Mol Biol 54:373−385
【非特許文献3】熊沢喜久雄ら、「植物の養分吸収」東京大学出版会、1976年
【非特許文献4】鈴木啓三ら、生物試料分析 31(2):139−146, 2008
【非特許文献5】吉田宗弘ら、微量栄養素研究、20:23−26, 2003
【非特許文献6】辻貴之ら、微量栄養素研究、17:153−157, 2000
【非特許文献7】日本栄養・食糧学会誌、50(4):273−278, 1997
【非特許文献8】日本栄養・食糧学会誌、58(5):267−272, 200.
【非特許文献9】Yano, H. et al., BIOMEDICAL RESEARCH ON TRACE ELEMENTS, 7(3):105−106, 1996
【非特許文献10】蔡徳龍ら、日本土壌肥料學雜誌、64(2):126−133, 19930405
【非特許文献11】小畑仁ら、日本土壌肥料學雜誌、53(3):235−240, 1982
【発明の概要】
【発明が解決しようとする課題】
【0009】
本発明は、野菜の可食部、すなわち葉等の地上部又は果実中に酸可溶性亜鉛を高濃度含有する野菜及びその製造法を提供することを課題とする。
【課題を解決するための手段】
【0010】
本発明者は、野菜の可食部中に酸可溶性亜鉛を高濃度で取り込ませるべく種々検討した結果、亜鉛含有液を葉面に散布することにより、高濃度に葉中に取り込まれ、葉又は果実中の亜鉛濃度が従来にない高濃度の野菜が得られること、更にこの亜鉛は、酸可溶性の亜鉛であり、ヒト、動物が摂取した場合に胃で可溶化され、吸収されやすい亜鉛であることを見出し、本発明を完成した。
すなわち、本発明は以下のとおりである。
【0011】
(1)地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するホウレンソウ。
(2)亜鉛含有量が200mg/100g以下である、前記ホウレンソウ。
(3)地上部に酸可溶性亜鉛を5mg/100g(乾燥重)以上含有するキャベツ。
(4)亜鉛含有量が100mg/100g(乾燥重)以下である、前記キャベツ。
(5)果実に酸可溶性亜鉛を0.15mg/100g(新鮮重)以上含有するトマト。
(6)亜鉛含有量が1mg/100g(新鮮重)以下である、前記トマト。
(7)地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するコマツナ。
(8)亜鉛含有量が500mg/100g(乾燥重)以下である、前記コマツナ。
(9)地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するレタス。
(10)亜鉛含有量が200mg/100g(乾燥重)以下である、前記レタス。
(11)地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するケール。
(12)亜鉛含有量が200mg/100g(乾燥重)以下である、前記ケール。
(13)亜鉛を0.001〜2重量%含有する液を、収穫日の0〜14日前にホウレンソウの葉面に散布することを特徴とする、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するホウレンソウの製造法。
(14)亜鉛を0.05〜2重量%含有する液を、収穫日の0〜14日前にキャベツの葉面に散布することを特徴とする、地上部に酸可溶性亜鉛を5mg/100g(乾燥重)以上含有するキャベツの製造法。
(15)亜鉛を0.05〜2重量%含有する液を、収穫日の0〜40日前にトマトの葉面に散布することを特徴とする、果実中に酸可溶性亜鉛を0.15mg/100g(新鮮重)以上含有するトマトの製造法。
(16)亜鉛を0.001〜2重量%含有する液を、収穫日の0〜14日前にコマツナの葉面に散布することを特徴とする、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するコマツナの製造法。
(17)亜鉛を0.001〜2重量%含有する液を、収穫日の0〜14日前にレタスの葉面に散布することを特徴とする、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するレタスの製造法。
(18)亜鉛を0.001〜2重量%含有する液を、収穫日の0〜14日前にケールの葉面に散布することを特徴とする、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するケールの製造法。
(19)亜鉛を含有する液が、さらに微生物又は微生物抽出物を含有する、前記方法。
(20)亜鉛を含有する液の散布量が、1ヘクタール当たり500リットル以上である、前記方法。
(21)ミネラルを含有する液を野菜の葉面に散布することにより、野菜の地上部又は果実中のミネラル含量を高める方法。
(22)酸可溶性亜鉛を高含有する野菜の製造に用いられる野菜製造用資材であって、亜鉛を0.001〜2重量%含有し、使用に際して葉面散布される、野菜製造用資材。
(23)さらに、微生物又は微生物抽出物を含有する、前記野菜製造用資材。
【発明の効果】
【0012】
本発明の野菜は高濃度の酸可溶性亜鉛を含有しており、栄養価の高い食品及び食品材料として有用である。
また、本発明の野菜の製造法は、葉面等への散布により亜鉛含有液を施用することから、重金属誘導クロロシスのような問題を生じず、河川への流亡等の環境保全上の問題もない。
【図面の簡単な説明】
【0013】
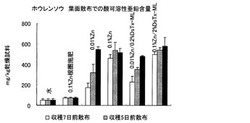
【図1】亜鉛を葉面散布したホウレンソウの地上部中の酸可溶性亜鉛含量を示す図。
【図2】亜鉛/鉄/銅/マグネシウム/カルシウムを葉面散布したキャベツの地上部中の亜鉛含量を示す図。
【図3】亜鉛/鉄/銅/マグネシウム/カルシウムを葉面散布したキャベツの地上部中の鉄含量を示す図。
【図4】発酵副生液の表面張力低下作用を示す図。「ap」は、アプローチBI(花王(株)。「アプローチ」は同社の登録商標である。)を示す。
【図5】亜鉛を葉面散布したトマトの果実中の酸可溶性亜鉛含量を示す図。
【図6】亜鉛を葉面散布したコマツナの地上部中の亜鉛含量を示す図。
【図7】亜鉛を葉面散布したレタスの地上部中の亜鉛含量を示す図。
【図8】亜鉛を葉面散布したケールの地上部中の亜鉛含量を示す図。
【発明を実施するための形態】
【0014】
以下、本発明を詳細に説明する。
本発明の野菜は、葉茎菜類又は果実類である。葉茎菜類としては、ホウレンソウ、キャベツ、コマツナ、レタス、ケール、フダンソウ、オカヒジキ、クレソン、ワサビ、コールラビ、ブロッコリー、カリフラワー、ハクサイ、メキャベツ、タカナ、ハクラン、ジュンサイ、アリタバ、ハマボウフウ、ミツバ、セルリー、セリ、パセリ、セージ、ハッカ、タイム、チョロギ、シソ、フキ、シュンギク、エンダイブ、食用ギク、ネギ、タケノコ、ニンニク、ワケギ、タマネギ、ラッキョウ、アサツキ、リーキ、ニラ、アスパラガス、ミョウガ、ショウガ、ウド等が挙げられる。果実類としては、トマト、オクラ、ナス、ピーマン、トウガラシ、キュウリ、メロン、ニガウリ、カボチャ、マクワウリ、ハヤトウリ、スイカ、イチゴ等が挙げられる。
【0015】
前記野菜の品種は特に制限されないが、例えば、ホウレンソウとしては、角種(つのだね)、赤根ほうれん草、日本ほうれん草、次郎丸ほうれん草、禹城(うじょう)、京ほうれん草、寒締めほうれん草、ピロフレー、黒葉ミンスターランド、リードほうれん草、豊葉ほうれん草、アトラスほうれん草、ミンスターほうれん草、スーパー日本ほうれん草、サラダほうれん草等が挙げられる。
【0016】
キャベツとしては、グリーンボール、レッドキャベツ、チリメンキャベツ(サボイキャベツ)、メキャベツ等が挙げられる。
【0017】
トマトとしては、桃太郎、ミニキャロル、ローマ、黄寿、ファーストトマト、赤色丸玉、イエローキャロル、パルチェ等が挙げられる。
【0018】
コマツナとしては、ハッケイ、風の娘、夏清水、安藤早生、よかった菜、すてきだ菜、ワカミ、キヨスミ、楽天、夏楽天、極楽天、笑天、オソメ、寒じめ、あやか小松菜、ナッチャン、菜々美等が挙げられる。
【0019】
レタスとしては、TE242、シグマ、LE−7MT、ファイングリーン、V、サンバレー、J、テンション、トリガー、ゲット、グリーンスパン、レッドコーラル、ブラックローズ、アーリースパン、レッドスパン、ラ・コスタ、レッドストーン、レッドロック、バシオ、コスレタス、レッドファルダ、グリーンウェーブ、リトルジェムロメイン、エムラップ231、ニガチシャ、エンダイブ、オンタリオ、キングクラウン、茎レタス、ケルン、コスタリカ4号、コスレタス、レッドウェーブ、サマーグリーン、サリナス88、シグマ、ファルコン、リバーグリーン、リーフレタスグリーン、リーフレタスレッド、グリーンオーク、フリンジーグリーン、フリンジーレッド、チマ・サンチュ、レッドオーク、ナンソウベニ、ニシナベニ、レッドウェーブ等が挙げられる。
【0020】
ケールとしては、キッチンケール、ツリーケール、ブッシュケール、マローケール、コラード、緑葉カンラン、ドリンクリーフ、ポルトガルケール等が挙げられる。
【0021】
本発明のホウレンソウは、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上、好ましくは20mg/100g(乾燥重)以上含有する。亜鉛濃度の上限は、特に制限されないが、通常200mg/100g(乾燥重)以下であり、他の形態では160mg/100g(乾燥重)以下である。通常、ホウレンソウ中の亜鉛濃度は0.7mg/100g(新鮮重)とされているが、本発明のホウレンソウはそれよりも高濃度の酸可溶性亜鉛を含有する。
尚、「地上部」には、葉及び/又は茎が含まれる。
【0022】
本発明のキャベツは、地上部に酸可溶性亜鉛を5mg/100g(乾燥重)以上、好ま
しくは10mg/100g(乾燥重)以上含有する。亜鉛濃度の上限は、特に制限されないが、通常100mg/100g(乾燥重)以下であり、他の形態では80mg/100g(乾燥重)以下である。通常、キャベツ中の酸可溶性亜鉛濃度は0.2mg/100g(乾燥重)とされているが、本発明のキャベツはそれよりも高濃度の酸可溶性亜鉛を含有する。
【0023】
本発明のトマトは、果実中に酸可溶性亜鉛を0.15mg/100g(新鮮重)以上、好ましくは0.16mg/100g以上(新鮮重)含有する。酸可溶性亜鉛濃度の上限は、特に制限されないが、通常1mg/100g(新鮮重)以下であり、他の形態では0.5mg/100g(新鮮重)以下である。通常、トマト果実中の酸可溶性亜鉛濃度は0.13mg/100gとされているが、本発明のトマトはそれよりも高濃度の酸可溶性亜鉛を果実中に含有する。
【0024】
本発明のコマツナは、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上、好ましくは20mg/100g(乾燥重)以上含有する。亜鉛濃度の上限は、特に制限されないが、通常500mg/100g(乾燥重)以下であり、他の形態では160mg/100g(乾燥重)以下である。通常、コマツナ中の亜鉛濃度は0.2mg/100g(新鮮重)とされているが、本発明のコマツナはそれよりも高濃度の酸可溶性亜鉛を含有する。
尚、「地上部」には、葉及び/又は茎が含まれる。
【0025】
本発明のレタスは、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上、好ましくは20mg/100g(乾燥重)以上含有する。亜鉛濃度の上限は、特に制限されないが、通常200mg/100g(乾燥重)以下であり、他の形態では160mg/100g(乾燥重)以下である。通常、コマツナ中の亜鉛濃度は0.2mg/100g(新鮮重)とされているが、本発明のコマツナはそれよりも高濃度の酸可溶性亜鉛を含有する。
尚、「地上部」には、葉及び/又は茎が含まれる。
【0026】
本発明のケールは、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上、好ましくは20mg/100g(乾燥重)以上含有する。亜鉛濃度の上限は、特に制限されないが、通常200mg/100g(乾燥重)以下であり、他の形態では160mg/100g(乾燥重)以下である。通常、コマツナ中の亜鉛濃度は0.3mg/100g(新鮮重)とされているが、本発明のコマツナはそれよりも高濃度の酸可溶性亜鉛を含有する。
尚、「地上部」には、葉及び/又は茎が含まれる。
【0027】
上記野菜中の亜鉛濃度は、例えば、原子吸光法、ICP発光分析法、ICP質量分析法、蛍光X線分析法等により測定することができる。酸可溶性亜鉛濃度は、野菜の葉部又は果実を酸溶液、例えば0.1N塩酸で抽出し、前記方法で亜鉛濃度を定量することによって、測定することができる。酸溶液での抽出に先立って、乾燥、粉砕等の前処理を行ってもよい。
【0028】
上記のような葉等の地上部、又は果実中に高濃度の酸可溶性亜鉛を含有する野菜は、亜鉛を0.001〜2重量%含有する液を、収穫前14日以内に野菜に葉面散布することにより製造できる。以下の記載において、野菜の製造方法、及び野菜製造用資材における野菜には、典型的にはホウレンソウ、キャベツ、トマトを含むが、これらには限定されない。
【0029】
本発明者等の検討によれば、野菜の葉等の地上部、又は果実中に酸可溶性亜鉛を高濃度で蓄積させるには、土壌散布でなく、葉面散布が好ましいことが判明した。従って、亜鉛を0.01〜2重量%含有する、野菜の葉面散布用液は、地上部又は果実中に酸可溶性亜
鉛を高含有する野菜製造用資材として有用である。
【0030】
本発明の野菜の製造方法の一形態は、亜鉛を0.001〜2重量%含有する液を、収穫日の0〜14日前、好ましくは0〜7日前、さらに好ましくは1〜7日前に、ホウレンソウの葉面に散布することを特徴とする、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するホウレンソウの製造法である。
【0031】
他の形態は、亜鉛を0.05〜2重量%含有する液を、収穫日の0〜14日前、好ましくは0〜7日前、さらに好ましくは1〜7日前に、にキャベツの葉面に散布することを特徴とする、地上部に酸可溶性亜鉛を5mg/100g(乾燥重)以上含有するキャベツの製造法である。
【0032】
さらに他の形態は、亜鉛を0.05〜2重量%含有する液を、収穫日の0〜40日前、好ましくは1〜30日前に、トマトの葉面に散布することを特徴とする、果実中に酸可溶性亜鉛を0.15mg/100g(新鮮重)以上含有するトマトの製造法である。
【0033】
さらに他の形態は、亜鉛を0.001〜2重量%含有する液を、収穫日の0〜14日前、好ましくは0〜7日前、さらに好ましくは1〜7日前に、コマツナの葉面に散布することを特徴とする、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するコマツナの製造法である。
【0034】
さらに他の形態は、亜鉛を0.001〜2重量%含有する液を、収穫日の0〜14日前、好ましくは0〜7日前、さらに好ましくは1〜7日前に、レタスの葉面に散布することを特徴とする、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するレタスの製造法である。
【0035】
さらに他の形態は、亜鉛を0.001〜2重量%含有する液を、収穫日の収穫日の0〜14日前、好ましくは0〜7日前、さらに好ましくは1〜7日前に、ケールの葉面に散布することを特徴とする、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するケールの製造法である。
【0036】
散布に用いる液(以下、「葉面散布資材」ということもある)は、亜鉛を0.001重量%以上、好ましくは0.005重量%以上、より好ましくは0.01重量%以上含有することが好ましい。亜鉛濃度の上限は、例えば2重量%以下、他の形態では1重量%以下である。また、葉面散布資材中の亜鉛濃度は、ホウレンソウ、コマツナ、レタス、ケール及びトマトでは0.005重量%以上が好ましく、キャベツでは0.05%以上が好ましい。
亜鉛含有液を調製するために用いる亜鉛としては水溶性があれば特に制限はなく、硫酸亜鉛、塩化亜鉛、硝酸亜鉛、蟻酸亜鉛、酢酸亜鉛等の亜鉛塩、又は、EDTA亜鉛のようなキレート体亜鉛などが挙げられる。このうち、葉への薬害軽減の点から硫酸亜鉛が特に好ましい。
【0037】
また、本発明で用いる葉面散布資材には、微生物又は微生物抽出物を含有させることにより、葉面への亜鉛の展着性が向上する。微生物としては特に制限されないが、細菌が好ましく、エシェリヒア(Escherichia)属、パントエア(Pantoea)属等の腸内細菌、又はコリネバクテリウム(Corynebacterium)属等のコリネ型細菌等が好ましい。これらの微生物又は微生物抽出物は水分を含んだままでもよいし、乾燥させてもよく、アミノ酸、核酸等の生産に用いた後の発酵副生液であってもよい。抽出物としては、熱水抽出物、酸性熱水抽出物、アルコール抽出物などが挙げられる。
【0038】
アミノ酸発酵副生液または核酸発酵副生液は、澱粉系及び糖蜜系を主原料とするグルタミン酸、リジン等の各種アミノ酸発酵副生液及びイノシン酸、グアニル酸、イノシン、グアノシン等の各種核酸発酵副生液である。具体的に、ここでいう副生液とは、リジン、グルタミンなどの塩基性または中性アミノ酸発酵液をpH調整した後、強酸性陽イオン樹脂に通じ、当該アミノ酸を吸着させた後の貫流液及びその濃縮液、並びに、グルタミン酸などの酸性アミノ酸発酵液を鉱酸でpHを等電点に調整し、析出した当該アミノ酸結晶を固液分離したときに得られる母液及びその濃縮液、核酸発酵液を、溶解度差を利用した冷却晶析及び濃縮晶析することで当該核酸を晶析し、析出した結晶を固液分離したときに得られる母液およびその濃縮液を例示することができる。これら発酵副生液には、固形分として、各種アミノ酸(濃縮液で5〜14重量%含有)、各種核酸の他、糖類、発酵菌体、有機態窒素、無機態窒素、ビタミン等の植物成長に必要な栄養分が多量に含まれており(固形分含量は30〜50重量%)、これらのなかにはフェニルアラニン発酵副生液である「PAL」(登録番号:生第74220号)、グルタミン発酵副生液である「グルタミン」(神奈川県第712号)のようにすでに液体副産窒素肥料として肥料登録され市販されているものもある。また、本発明の効果を阻害しない限り、これらアミノ酸発酵副生液に、所望により、窒素、リン酸、カリウム、ミネラル等の一般に考えられる肥料成分をさらに加えることも可能である。実施例で使用したDsTx−ML及びDSCLは、グルタミン酸発酵副生液であり、NAMLはイノシン酸、グアニル酸発酵副生液である。DsTx−MLはpH調整に塩酸を、DSCLはpH調整に硫酸を使用している。
【0039】
微生物又は微生物抽出物の葉面散布資材中の含有量は、微生物又は微生物抽出物、及び他の葉面散布資材成分(水分を含む)の合計量で、乾燥物換算で0.01〜20重量%、さらに0.1〜10重量%が好ましい。
【0040】
葉面散布資材には、葉面への付着性を高めるため、農業上通常用いられる展着剤、及び/または界面活性剤を添加してもよい。展着剤、界面活性剤は特に制限はないが、展着剤としては、例えばアプローチBI(花王(株)。「アプローチ」は同社の登録商標である。)、ミックスパワー(シンジェンタ ジャパン(株)。「ミックスパワー」は同社の登録商標である。)などが挙げられる。界面活性剤としては非イオン性、陰イオン性、陽イオン性及び両イオン性のいずれも使用することが出来る。例を挙げると、ポリオキシエチレンアルキルエーテル、ポリオキシエチレンアルキルアリールエーテル、ポリオキシエチレン脂肪酸エステル、ソルビタン脂肪酸エステル、ポリオキシエチレンソルビタン脂肪酸エステル、オキシエチレンポリマー、オキシプロピレンポリマー、ポリオキシエチレンアルキルリン酸エステル、脂肪酸塩、アルキル硫酸エステル塩、アルキルスルホン酸塩、アルキルアリールスルホン酸塩、アルキルリン酸塩、アルキルリン酸エステル塩、ポリオキシエチレンアルキル硫酸エステル、第四級アンモニウム塩、オキシアルキルアミン、レシチン、サポニン等である。また、必要に応じてゼラチン、カゼイン、デンプン、寒天、ポリビニルアルコール、アルギン酸ソーダなどを補助剤として用いることが出来る。
【0041】
葉面散布資材を散布する場合、農業上通常用いられる葉面散布用肥料と混合してもよい。この場合、肥料成分としては特に制限はないが、溶解後アルカリ性を示すものについては亜鉛が塩として沈殿を起こすため好ましくない場合がある。混合する場合に好ましい肥料成分を例示すれば、尿素、燐酸アンモニウム、塩酸アンモニウム、硫酸アンモニウム、燐酸、ピロ燐酸などが挙げられる。中でも尿素の混用は亜鉛の吸収量を高める場合があるため好ましい(Mortvedt, J.J. et al., 1993.”Zinc
fertilizers” in Robson, A.D. (Ed.) Zinc
in soils and plants (p.33−44), Kluweracademic publishers, Dordrecht, the Netherland)。
【0042】
本発明の野菜を栽培する場合の土壌に施用する基肥、追肥は、野菜の種類に応じてその地域で通常行われている施肥量・施肥方法に準拠すればよい。また、環境を損わない範囲で土壌を亜鉛処理してもよい。土壌の亜鉛処理によって、野菜中の亜鉛含量をさらに若干増加させることが出来る。
【0043】
本発明の野菜を栽培する場合の栽植密度は、野菜の種類に応じてその地域で推奨されている密度でよいが、畦間(条間)については葉面散布資材が下部の葉にも容易に到達できるよう、30cm以上とすることが好ましい。
【0044】
葉面散布資材の散布方法は特に制限されないが、野菜の地上部全体に葉面散布資材が展着するようにすることが望ましい。人手により散布する場合は、葉面散布資材の噴霧口が葉表面ないしは裏面部位に向くような操作が望まれる。また、ブームスプレーヤーを使用する場合は、散布液量を1ヘクタール当たり100リットル以上、好ましくは200〜3000リットル、より好ましくは300〜2000リットルとすることが望ましい。また、静電気を利用することにより噴霧液の植物体への付着を促進させるいわゆる静電噴霧機や静電噴霧ノズル口を用いてもよい。
【0045】
葉茎菜類の葉面散布資材の散布時期については、収穫日から14日以内、より好ましくは収穫日から7日以内の時期が好ましい。散布は、収穫同日でもよいが、少なくとも前日までに行うことが好ましい。散布回数は、適宜設定することができるが、1日1回から2週間に1回が好ましい。さらに1週間に1回散布することがより好ましい。また、作物生育期間中での合計散布回数は1〜3回が好ましい。
【0046】
果実類の葉面散布資材の散布時期については着蕾期から開花期を経て果実が成熟する時期までがよく、特に開花期〜成熟直前までの時期が好ましい。具体的には収穫日から40日以内、好ましくは収穫日から1〜30日前が好ましい。葉面散布資材の散布間隔については、適宜設定することができるが、1日1回から2週間に1回が好ましい。さらに1〜2週間に1回散布することがより好ましい。また、作物生育期間中での合計散布回数は2〜10回が好ましい。
【0047】
亜鉛以外のミネラル、例えば鉄、銅、カルシウム、マグネシウム、バナジウムなども、上記と同様にして、ミネラルを含有する液を野菜の葉面に散布することにより、野菜の地上部又は果実中の含量を高めることができる。
【実施例】
【0048】
次に実施例を示して本発明を更に詳細に説明するが、本発明は以下の実施例に限定されるものではない。
【0049】
〔実施例1〕
ホウレンソウは、楽秋ほうれん草(アタリヤ(株))を用いた。栽培には、5cm角のロックウール(日東紡社製、サイズV 50x50x50mm、ポリエチレンフィルムカバー無し)を用いた。肥料として、OptMS Zn(−)無機塩類培養液(表1)を栽培開始時および播種15日目に1回与え、水のみを週2回与えた。播種、栽培は、人工気象室(23℃)で実施した。光強度は100μmol m-2 s-1程度とし、14時間明期、10時間暗期のサイクルで、49日間栽培した。
植物への各試料液の散布は15時から17時の間に行なった。散布量は、およそ1ml/1個体で、収穫の7日前、5日前、2日前にそれぞれ散布した。亜鉛の根圏施肥を行なう場合は、1ml/1個体となるように収穫の22日前ないしは7日前に施肥した。各試料液は表2に示した。表2中、DsTx−MLは、L−グルタミン酸発酵副生液である。また、亜鉛濃度は亜鉛換算の%(w/v)濃度である(以下の記載においても同様である
。)。葉面散布にあたっては、SPRAY−WORK HG AIR COMPRESSOR REVO((株)タミヤ社製)を用い、すべての葉面に十分散布溶液が行き届くように散布した。試験は各処理n=3(3株)で行なった。また、実験に使用した亜鉛には、全て硫酸亜鉛を用いた。
【0050】
【表1】

【0051】
収穫は播種後49日目に行い、各個体の地上部を分離し、乾燥機内で80℃、3日間乾燥させた。乾燥後の地上部は乳鉢で粉砕した後、0.1gを秤量し、0.1N塩酸10mLを加え、37℃で3時間の抽出を行った。抽出液を更に0.1N塩酸で15倍(v/v)希釈し、その液中の亜鉛含量をICP発光分光分析装置ICPS−8100((株)島津製作所社製)によって測定した。測定値から、乾物重あたりの亜鉛含有量を算出した。
その結果は図1に示した。根圏に亜鉛を施用することでは、地上部中の酸可溶性亜鉛は僅かな上昇を示すものの、対照である水との差は小さかった。一方、等量の亜鉛(0.1%Zn)を根圏施肥した場合と葉面散布した場合を比較すると、葉面散布した場合の酸可溶性亜鉛の上昇は、根圏施肥した場合の7〜8倍となり、葉面散布処理が有効であることが明らかであった。また、1/10量の亜鉛を葉面散布した場合でも、酸可溶性亜鉛の上昇は、根圏散布に比べて2〜8倍高値を示し、葉面散布処理がヒト、動物に吸収されやすい酸可溶性亜鉛の上昇に有効であることを示している。
【0052】
【表2】

【0053】
〔実施例2〕
キャベツは、金系201号((株)サカタのタネ)を用いた。栽培には、パワーソイル(関東肥料工業(株))を内径6cmのポリプロピレン製ポット(日本ポリプロ(株))に0.1Lずつ充填したポットを用いた。肥料として、OptMS Zn(−)無機塩類培養液(表1)を播種18日目、33日目に2回与え、水のみを週2回与えた。播種、栽培は、人工気象室(23℃)で実施した。光強度は120μmol m-2 s-1程度とし、14時間明期、10時間暗期のサイクルで、39日間栽培した。
【0054】
栽培植物への各試料液の散布は15時から17時の間に行なった。散布量は、およそ0.25ml/1個体で、収穫の7日前、5日前、2日前に3回(計0.75ml/1個体)散布した。ミネラルの根圏施肥を行なう場合は、0.75ml/1個体となるように収穫の20日前に施肥した。各試料液は表3に示した。葉面散布にあたっては、SPRAY−WORK HG AIR COMPRESSOR REVO((株)タミヤ社製)を用い、すべての葉面に十分散布溶液が行き届くように散布した。試験は各処理n=3(3株)で行なった。また実験に使用した亜鉛には、全て硫酸亜鉛を用いた。同様に実験に使用した鉄、マグネシウム、カルシウム、銅には、それぞれ硫酸鉄、硫酸マグネシウム、硫酸カルシウム、硫酸銅を用いた。
【0055】
収穫は播種後39日目に行い、各個体の地上部を分離し、乾燥機内で80℃、3日間乾燥させた。乾燥後の地上部は乳鉢で粉砕した後、エネルギー分散型蛍光X線分析装置EDX−900HS((株)島津製作所社製)によって亜鉛含量を測定した。測定値から、乾物重あたりの亜鉛含有量を算出した。
【0056】
その結果は図2(亜鉛含量)、図3(鉄含量)に示した。根圏への亜鉛施用の有無に関わらず、地上部の亜鉛は検出限界以下であった。一方、葉面散布した場合は地上部の亜鉛の検出が可能となることから、葉面散布処理が有効であることが明らかとなった。また、この葉面散布処理は、L−グルタミン酸発酵副生液の存在下では、等量の亜鉛を葉面散布した場合と比較して5倍以上の高値を示し、亜鉛の上昇に有効であることを示している。また、同様に地上部の鉄量も特にL−グルタミン酸発酵副生液の存在下では、等量の鉄を
葉面散布した場合と比較して約2倍の高値を示し、鉄の上昇に有効であることを示している。これらの結果から、亜鉛のみでなく、鉄などのミネラル上昇にも葉面散布処理、特に発酵副生液を共存させた葉面散布処理が有効であることが示された。
【0057】
なお、「五訂増補日本食品標準成分表」による亜鉛高含有食品として知られているかき(生)中の平均的な亜鉛含量は132mg/kg、牛レバー(生)中の平均的な亜鉛含量は38mg/kgとされており、この点から考えると本実施例の亜鉛葉面散布によって牛レバーの2〜3倍、かきに匹敵する亜鉛含量をもつキャベツが得られたこととなる。また、L−グルタミン酸発酵副生液を亜鉛と併用した場合は、牛レバーの10〜20倍、かきの4〜5倍の亜鉛含量をもつキャベツが得られたこととなる。
【0058】
【表3】

【0059】
〔実施例3〕発酵副生液の展着性の評価
(表面張力値試験)
発酵副生液の展着剤としての効力の目安として、表面張力値をウイルヘルミイ(Wihelmy)法(J. Physiol. (1979), 295, 217−227)にて測定した。測定には、表面張力測定装置CBVP−A3(協和界面科学(株))を用いた。測定したサンプルは、市販の展着剤アプローチBI(花王(株))、グルタミン酸発酵副生液(DsTx−ML、DSCL)、核酸発酵副生液(NAML)のそれぞれ希釈溶液である。
【0060】
試験結果は図4に示すとおりである。この試験結果から明らかなように、発酵副生液は、0.2%〜2%という低濃度においても市販の展着剤に匹敵する表面張力の低下作用を有し、濡れ難い植物であるキャベツなどへの展着において有利である。
【0061】
〔実施例4〕
トマトはマイクロトムを用いた。栽培には、パワーソイル(関東肥料工業(株))を内径6cmのポリプロピレン製ポット(日本ポリプロ(株))に0.1Lずつ充填したポッ
トを用いた。肥料として、OptMS Zn(−)無機塩類培養液(表1)を播種20日目、47日目に2回与え、水のみを週2回与えた。播種、栽培は、人工気象室(23℃)で実施した。光強度は120μmol m-2 s-1程度とし、14時間明期、10時間暗期のサイクルで、78日間栽培した。約49日後に開花し、62日後に結実した。
【0062】
栽培植物への各試料液の散布は15時から17時の間に行なった。散布量は、およそ0.5ml/1個体で、表4に記載したタイミングでそれぞれ散布した。各試料液は表4に示した。葉面散布にあたっては、SPRAY−WORK HG AIR COMPRESSOR REVO((株)タミヤ社製)を用い、すべての葉面に十分散布溶液が行き届くように散布した。試験は各処理n=5(5株)で行なった。また実験に使用した亜鉛は全て硫酸亜鉛を用いた。
【0063】
収穫は播種後78日目に行い、各固体の果実を収穫し、ミキサーで粉砕した。粉砕試料1gを秤量し、0.1N塩酸9mLを加え、37℃で3時間の抽出を行った。抽出液中の亜鉛含量をICP発光分光分析装置ICPS−8100((株)島津製作所社製)によって測定した。測定値から、新鮮重あたりの亜鉛含有量を算出した。
【0064】
その結果は図4に示した。亜鉛(0.01%Zn)を葉面散布した場合、水を葉面散布した場合と比較して酸可溶性亜鉛が上昇し、果実への亜鉛の蓄積においても、葉面散布処理が有効であることが明らかとなり、葉面散布処理がヒト、動物に吸収されやすい酸可溶性亜鉛の上昇に有効であることを示している。亜鉛散布のタイミングとしては、生育初期からの散布でも有効であるが、開花後の散布でも同様に有効であった。
【0065】
【表4】

【0066】
〔実施例5〕
コマツナは、コマツナ(サカタのタネ)を用いた。栽培には、5cm角のロックウール(日東紡社製、サイズV 50x50x50mm、ポリエチレンフィルムカバー無し)を用いた。肥料として、OptMS Zn(−)無機塩類培養液(表1)を栽培開始時および播種10日目に1回与え、水のみを週2回与えた。播種、栽培は、人工気象室(23℃)で実施した。光強度は120μmol m-2 s-1程度とし、14時間明期、10時間暗期のサイクルで、24日間栽培した。
植物への各試料液の散布は15時から17時の間に行なった。散布量は、およそ1ml/1個体で、収穫の5日前、2日前にそれぞれ散布した。亜鉛の根圏施肥を行なう場合は、1ml/1個体となるように収穫の22日前ないしは7日前に施肥した。各試料液は表5に示した。表5中、DsTx−MLは、L−グルタミン酸発酵副生液である。また、亜鉛濃度は亜鉛換算の%(w/v)濃度である(以下の記載においても同様である。)。葉
面散布にあたっては、SPRAY−WORK HG AIR COMPRESSOR REVO((株)タミヤ社製)を用い、すべての葉面に十分散布溶液が行き届くように散布した。試験は各処理n=3(3株)で行なった。また、実験に使用した亜鉛には、全て硫酸亜鉛を用いた。
【0067】
収穫は播種後24日目に行い、各個体の地上部を分離し、乾燥機内で80℃、3日間乾燥させた。乾燥後の地上部は乳鉢で粉砕した後、0.1gを秤量し、0.1N塩酸10mLを加え、37℃で3時間の抽出を行った。抽出液を更に0.1N塩酸で15倍(v/v)希釈し、その液中の亜鉛含量をICP発光分光分析装置ICPS−8100((株)島津製作所社製)によって測定した。測定値から、乾物重あたりの亜鉛含有量を算出した。
その結果は図6に示した。根圏に亜鉛を施用することでは、地上部中の酸可溶性亜鉛は僅かな上昇を示すものの、対照である水との差は小さかった。一方、等量の亜鉛(0.1%Zn)を根圏施肥した場合と葉面散布した場合を比較すると、葉面散布した場合の酸可溶性亜鉛の上昇は、根圏施肥した場合の2〜3倍となり、葉面散布処理が有効であることが明らかであった。また、1/10量の亜鉛を葉面散布した場合でも、酸可溶性亜鉛の上昇は、根圏散布に比べて約3倍高値を示し、葉面散布処理がヒト、動物に吸収されやすい酸可溶性亜鉛の上昇に有効であることを示している。また、この葉面散布処理は、L−グルタミン酸発酵副生液の存在下では、等量の亜鉛を葉面散布した場合と比較して3〜5倍以上の高値を示し、亜鉛の上昇に有効であることを示している。
【0068】
【表5】

【0069】
〔実施例6〕
レタスは、カキチシャ チマ・サンチュ(サカタのタネ)を用いた。栽培には、5cm角のロックウール(日東紡社製、サイズV 50x50x50mm、ポリエチレンフィルムカバー無し)を用いた。肥料として、OptMS Zn(−)無機塩類培養液(表1)を栽培開始時および播種10日目に1回与え、水のみを週2回与えた。播種、栽培は、人工気象室(23℃)で実施した。光強度は120μmol m-2 s-1程度とし、14時間明期、10時間暗期のサイクルで、27日間栽培した。
植物への各試料液の散布は15時から17時の間に行なった。散布量は、およそ1ml/1個体で、収穫の7日前、5日前、2日前にそれぞれ散布した。亜鉛の根圏施肥を行なう場合は、1ml/1個体となるように収穫の24日前ないしは7日前に施肥した。各試料液は表6に示した。表6中、DsTx−MLは、L−グルタミン酸発酵副生液である。また、亜鉛濃度は亜鉛換算の%(w/v)濃度である(以下の記載においても同様である。)。葉面散布にあたっては、SPRAY−WORK HG AIR COMPRESS
OR REVO((株)タミヤ社製)を用い、すべての葉面に十分散布溶液が行き届くように散布した。試験は各処理n=3(3株)で行なった。また、実験に使用した亜鉛には、全て硫酸亜鉛を用いた。
【0070】
収穫は播種後24日目に行い、各個体の地上部を分離し、乾燥機内で80℃、3日間乾燥させた。乾燥後の地上部は乳鉢で粉砕した後、0.1gを秤量し、0.1N塩酸10mLを加え、37℃で3時間の抽出を行った。抽出液を更に0.1N塩酸で15倍(v/v)希釈し、その液中の亜鉛含量をICP発光分光分析装置ICPS−8100((株)島津製作所社製)によって測定した。測定値から、乾物重あたりの亜鉛含有量を算出した。
その結果は図7に示した。根圏に亜鉛を施用することでは、地上部中の酸可溶性亜鉛は僅かな上昇を示すものの、対照である水との差は小さかった。一方、等量の亜鉛(0.1%Zn)を根圏施肥した場合と葉面散布した場合を比較すると、葉面散布した場合の酸可溶性亜鉛の上昇は、根圏施肥した場合の6〜10倍となり、葉面散布処理が有効であることが明らかであった。また、1/10量の亜鉛を葉面散布した場合でも、酸可溶性亜鉛の上昇は、根圏散布に比べて2倍以上高値を示し、葉面散布処理がヒト、動物に吸収されやすい酸可溶性亜鉛の上昇に有効であることを示している。また、この葉面散布処理は、L−グルタミン酸発酵副生液の存在下では、等量の亜鉛を葉面散布した場合と比較して約1.5倍の高値を示し、亜鉛の上昇に有効であることを示している。
【0071】
【表6】

【0072】
〔実施例7〕
ケールは、ケール(サカタのタネ)を用いた。栽培には、5cm角のロックウール(日東紡社製、サイズV 50x50x50mm、ポリエチレンフィルムカバー無し)を用いた。肥料として、OptMS Zn(−)無機塩類培養液(表1)を栽培開始時および播種10日目に1回与え、水のみを週2回与えた。播種、栽培は、人工気象室(23℃)で実施した。光強度は120μmol m-2 s-1程度とし、14時間明期、10時間暗期のサイクルで、27日間栽培した。
植物への各試料液の散布は15時から17時の間に行なった。散布量は、およそ1ml/1個体で、収穫の7日前、5日前、2日前にそれぞれ散布した。亜鉛の根圏施肥を行なう場合は、1ml/1個体となるように収穫の24日前ないしは7日前に施肥した。各試
料液は表7に示した。表7中、DsTx−MLは、L−グルタミン酸発酵副生液である。また、亜鉛濃度は亜鉛換算の%(w/v)濃度である(以下の記載においても同様である。)。葉面散布にあたっては、SPRAY−WORK HG AIR COMPRESSOR REVO((株)タミヤ社製)を用い、すべての葉面に十分散布溶液が行き届くように散布した。試験は各処理n=3(3株)で行なった。また、実験に使用した亜鉛には、全て硫酸亜鉛を用いた。
【0073】
収穫は播種後24日目に行い、各個体の地上部を分離し、乾燥機内で80℃、3日間乾燥させた。乾燥後の地上部は乳鉢で粉砕した後、0.1gを秤量し、0.1N塩酸10mLを加え、37℃で3時間の抽出を行った。抽出液を更に0.1N塩酸で15倍(v/v)希釈し、その液中の亜鉛含量をICP発光分光分析装置ICPS−8100((株)島津製作所社製)によって測定した。測定値から、乾物重あたりの亜鉛含有量を算出した。
その結果は図8に示した。根圏に亜鉛を施用することでは、地上部中の酸可溶性亜鉛は僅かな上昇を示すものの、対照である水との差は小さかった。一方、等量の亜鉛(0.1%Zn)を根圏施肥した場合と葉面散布した場合を比較すると、葉面散布した場合の酸可溶性亜鉛の上昇は、根圏施肥した場合の3〜4倍となり、葉面散布処理が有効であることが明らかであった。これらの結果は、葉面散布処理がヒト、動物に吸収されやすい酸可溶性亜鉛の上昇に有効であることを示している。また、この葉面散布処理は、L−グルタミン酸発酵副生液の存在下では、等量の亜鉛を葉面散布した場合と比較して2〜6倍の高値を示し、亜鉛の上昇に有効であることを示している。
【0074】
【表7】

【技術分野】
【0001】
本発明は、可食部中に酸可溶性亜鉛を高濃度含有し、ヒト、動物の食品または食品材料として有用な野菜、及びその製造法に関する。
【背景技術】
【0002】
近年、食生活の変化等により、種々の栄養素の不足が懸念されており、亜鉛(Zn)等の微量金属もその一つである。亜鉛は、人体内中で微量金属元素としては鉄についで多く含まれており、代謝系で重要な役割を担っていることが知られている(特許文献1)。亜鉛は、牡蠣中には13.2mg/100g、牛レバーには3.8mg/100g含有されていることが知られているが(非特許文献1)、これらのように亜鉛を多く含む食品は限られており、現在の食習慣で亜鉛を所要量摂取することは困難である。
【0003】
植物中の亜鉛含量を高める技術が種々提案されている。例えば、ライムギにおいてシロイヌナズナ由来の亜鉛トランスポーター遺伝子を過剰発現させる方法が開発されている(非特許文献2)。しかしながら、この遺伝子組換体の亜鉛吸収速度は高くはない。
【0004】
また、豆類(特許文献1)、イモ類(特許文献2)、イネ(特許文献3)、トウモロコシ(特許文献4)、ソバ(特許文献5)、コムギ(特許文献7)のような穀類、又は直根類(特許文献6)等の植物の葉面等に亜鉛含有液を散布することによって、植物の子実や根の亜鉛含量を高める方法が提案されている。また、これらの亜鉛含有液に海藻抽出物を含有させることによって、子実等への亜鉛移行率が向上することが報告されている(特許文献1〜7)。亜鉛の葉面散布自体は、土壌に亜鉛を大量に施肥した場合に生じるとされている、土壌中の鉄の吸収移動を阻害し、鉄欠乏症状を引き起こしてしまう(重金属誘導クロロシス)という問題(非特許文献3)が生じないため好ましい。しかしながら、前記方法では、植物の子実中の亜鉛含有量の上昇はわずかである。また、一般的に、ヒト等の動物が吸収可能な亜鉛は、食品等から酸で可溶化する亜鉛である(非特許文献4、5、6)が、穀物中の亜鉛はフィチン酸に強固に結合しているので、ヒトが栄養として吸収するのは困難である(非特許文献7、8、9)。
【0005】
一方、亜鉛を土壌に大量に施肥すると、土壌中の鉄の吸収移動を阻害し、鉄欠乏症状を引き起こしてしまう(重金属誘導クロロシス)という問題(熊沢・西沢1976.植物の養分吸収.東京大学出版会)がある。また、例えば日本においては、平成15年の環境基本法改正により河川や海水中の亜鉛濃度基準が10〜30μg/L以下と設定されているが、土壌に大量に亜鉛を施用すると、河川等への流亡も環境保全上問題となる。
【0006】
日本において日常的に摂取する食習慣を有する植物として、ホウレンソウ、コマツナ等の野菜がある。これらは冷凍食品等の加工食品中にも多く含まれ、ほぼ毎日無理なく摂取できる食材といえる。この点から野菜における亜鉛等の微量金属元素の含有量を高めることができれば有用と考えられるが、亜鉛等のミネラルは葉から転流される(非特許文献10、11)ため、欠乏症状が現れた栽培初期、中期(収穫の数週間以上前)に葉面散布を実施する従来の散布方法では、葉中に高濃度で蓄積させることは困難であった。
【先行技術文献】
【特許文献】
【0007】
【特許文献1】特開2008−161099
【特許文献2】特開2008−263891
【特許文献3】特開2008−263892
【特許文献4】特開2008−263893
【特許文献5】特開2008−263894
【特許文献6】特開2008−263895
【特許文献7】特開2008−263896
【非特許文献】
【0008】
【非特許文献1】「五訂増補日本食品標準成分表」文部科学省科学技術・学術審議会・資源調査分科会(http://www.mext.go.jp/b_menu/shingi/gijyutu/gijyutu3/toushin/05031802.htm)
【非特許文献2】Ramesh, et al. 2004 Plant Mol Biol 54:373−385
【非特許文献3】熊沢喜久雄ら、「植物の養分吸収」東京大学出版会、1976年
【非特許文献4】鈴木啓三ら、生物試料分析 31(2):139−146, 2008
【非特許文献5】吉田宗弘ら、微量栄養素研究、20:23−26, 2003
【非特許文献6】辻貴之ら、微量栄養素研究、17:153−157, 2000
【非特許文献7】日本栄養・食糧学会誌、50(4):273−278, 1997
【非特許文献8】日本栄養・食糧学会誌、58(5):267−272, 200.
【非特許文献9】Yano, H. et al., BIOMEDICAL RESEARCH ON TRACE ELEMENTS, 7(3):105−106, 1996
【非特許文献10】蔡徳龍ら、日本土壌肥料學雜誌、64(2):126−133, 19930405
【非特許文献11】小畑仁ら、日本土壌肥料學雜誌、53(3):235−240, 1982
【発明の概要】
【発明が解決しようとする課題】
【0009】
本発明は、野菜の可食部、すなわち葉等の地上部又は果実中に酸可溶性亜鉛を高濃度含有する野菜及びその製造法を提供することを課題とする。
【課題を解決するための手段】
【0010】
本発明者は、野菜の可食部中に酸可溶性亜鉛を高濃度で取り込ませるべく種々検討した結果、亜鉛含有液を葉面に散布することにより、高濃度に葉中に取り込まれ、葉又は果実中の亜鉛濃度が従来にない高濃度の野菜が得られること、更にこの亜鉛は、酸可溶性の亜鉛であり、ヒト、動物が摂取した場合に胃で可溶化され、吸収されやすい亜鉛であることを見出し、本発明を完成した。
すなわち、本発明は以下のとおりである。
【0011】
(1)地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するホウレンソウ。
(2)亜鉛含有量が200mg/100g以下である、前記ホウレンソウ。
(3)地上部に酸可溶性亜鉛を5mg/100g(乾燥重)以上含有するキャベツ。
(4)亜鉛含有量が100mg/100g(乾燥重)以下である、前記キャベツ。
(5)果実に酸可溶性亜鉛を0.15mg/100g(新鮮重)以上含有するトマト。
(6)亜鉛含有量が1mg/100g(新鮮重)以下である、前記トマト。
(7)地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するコマツナ。
(8)亜鉛含有量が500mg/100g(乾燥重)以下である、前記コマツナ。
(9)地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するレタス。
(10)亜鉛含有量が200mg/100g(乾燥重)以下である、前記レタス。
(11)地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するケール。
(12)亜鉛含有量が200mg/100g(乾燥重)以下である、前記ケール。
(13)亜鉛を0.001〜2重量%含有する液を、収穫日の0〜14日前にホウレンソウの葉面に散布することを特徴とする、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するホウレンソウの製造法。
(14)亜鉛を0.05〜2重量%含有する液を、収穫日の0〜14日前にキャベツの葉面に散布することを特徴とする、地上部に酸可溶性亜鉛を5mg/100g(乾燥重)以上含有するキャベツの製造法。
(15)亜鉛を0.05〜2重量%含有する液を、収穫日の0〜40日前にトマトの葉面に散布することを特徴とする、果実中に酸可溶性亜鉛を0.15mg/100g(新鮮重)以上含有するトマトの製造法。
(16)亜鉛を0.001〜2重量%含有する液を、収穫日の0〜14日前にコマツナの葉面に散布することを特徴とする、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するコマツナの製造法。
(17)亜鉛を0.001〜2重量%含有する液を、収穫日の0〜14日前にレタスの葉面に散布することを特徴とする、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するレタスの製造法。
(18)亜鉛を0.001〜2重量%含有する液を、収穫日の0〜14日前にケールの葉面に散布することを特徴とする、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するケールの製造法。
(19)亜鉛を含有する液が、さらに微生物又は微生物抽出物を含有する、前記方法。
(20)亜鉛を含有する液の散布量が、1ヘクタール当たり500リットル以上である、前記方法。
(21)ミネラルを含有する液を野菜の葉面に散布することにより、野菜の地上部又は果実中のミネラル含量を高める方法。
(22)酸可溶性亜鉛を高含有する野菜の製造に用いられる野菜製造用資材であって、亜鉛を0.001〜2重量%含有し、使用に際して葉面散布される、野菜製造用資材。
(23)さらに、微生物又は微生物抽出物を含有する、前記野菜製造用資材。
【発明の効果】
【0012】
本発明の野菜は高濃度の酸可溶性亜鉛を含有しており、栄養価の高い食品及び食品材料として有用である。
また、本発明の野菜の製造法は、葉面等への散布により亜鉛含有液を施用することから、重金属誘導クロロシスのような問題を生じず、河川への流亡等の環境保全上の問題もない。
【図面の簡単な説明】
【0013】
【図1】亜鉛を葉面散布したホウレンソウの地上部中の酸可溶性亜鉛含量を示す図。
【図2】亜鉛/鉄/銅/マグネシウム/カルシウムを葉面散布したキャベツの地上部中の亜鉛含量を示す図。
【図3】亜鉛/鉄/銅/マグネシウム/カルシウムを葉面散布したキャベツの地上部中の鉄含量を示す図。
【図4】発酵副生液の表面張力低下作用を示す図。「ap」は、アプローチBI(花王(株)。「アプローチ」は同社の登録商標である。)を示す。
【図5】亜鉛を葉面散布したトマトの果実中の酸可溶性亜鉛含量を示す図。
【図6】亜鉛を葉面散布したコマツナの地上部中の亜鉛含量を示す図。
【図7】亜鉛を葉面散布したレタスの地上部中の亜鉛含量を示す図。
【図8】亜鉛を葉面散布したケールの地上部中の亜鉛含量を示す図。
【発明を実施するための形態】
【0014】
以下、本発明を詳細に説明する。
本発明の野菜は、葉茎菜類又は果実類である。葉茎菜類としては、ホウレンソウ、キャベツ、コマツナ、レタス、ケール、フダンソウ、オカヒジキ、クレソン、ワサビ、コールラビ、ブロッコリー、カリフラワー、ハクサイ、メキャベツ、タカナ、ハクラン、ジュンサイ、アリタバ、ハマボウフウ、ミツバ、セルリー、セリ、パセリ、セージ、ハッカ、タイム、チョロギ、シソ、フキ、シュンギク、エンダイブ、食用ギク、ネギ、タケノコ、ニンニク、ワケギ、タマネギ、ラッキョウ、アサツキ、リーキ、ニラ、アスパラガス、ミョウガ、ショウガ、ウド等が挙げられる。果実類としては、トマト、オクラ、ナス、ピーマン、トウガラシ、キュウリ、メロン、ニガウリ、カボチャ、マクワウリ、ハヤトウリ、スイカ、イチゴ等が挙げられる。
【0015】
前記野菜の品種は特に制限されないが、例えば、ホウレンソウとしては、角種(つのだね)、赤根ほうれん草、日本ほうれん草、次郎丸ほうれん草、禹城(うじょう)、京ほうれん草、寒締めほうれん草、ピロフレー、黒葉ミンスターランド、リードほうれん草、豊葉ほうれん草、アトラスほうれん草、ミンスターほうれん草、スーパー日本ほうれん草、サラダほうれん草等が挙げられる。
【0016】
キャベツとしては、グリーンボール、レッドキャベツ、チリメンキャベツ(サボイキャベツ)、メキャベツ等が挙げられる。
【0017】
トマトとしては、桃太郎、ミニキャロル、ローマ、黄寿、ファーストトマト、赤色丸玉、イエローキャロル、パルチェ等が挙げられる。
【0018】
コマツナとしては、ハッケイ、風の娘、夏清水、安藤早生、よかった菜、すてきだ菜、ワカミ、キヨスミ、楽天、夏楽天、極楽天、笑天、オソメ、寒じめ、あやか小松菜、ナッチャン、菜々美等が挙げられる。
【0019】
レタスとしては、TE242、シグマ、LE−7MT、ファイングリーン、V、サンバレー、J、テンション、トリガー、ゲット、グリーンスパン、レッドコーラル、ブラックローズ、アーリースパン、レッドスパン、ラ・コスタ、レッドストーン、レッドロック、バシオ、コスレタス、レッドファルダ、グリーンウェーブ、リトルジェムロメイン、エムラップ231、ニガチシャ、エンダイブ、オンタリオ、キングクラウン、茎レタス、ケルン、コスタリカ4号、コスレタス、レッドウェーブ、サマーグリーン、サリナス88、シグマ、ファルコン、リバーグリーン、リーフレタスグリーン、リーフレタスレッド、グリーンオーク、フリンジーグリーン、フリンジーレッド、チマ・サンチュ、レッドオーク、ナンソウベニ、ニシナベニ、レッドウェーブ等が挙げられる。
【0020】
ケールとしては、キッチンケール、ツリーケール、ブッシュケール、マローケール、コラード、緑葉カンラン、ドリンクリーフ、ポルトガルケール等が挙げられる。
【0021】
本発明のホウレンソウは、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上、好ましくは20mg/100g(乾燥重)以上含有する。亜鉛濃度の上限は、特に制限されないが、通常200mg/100g(乾燥重)以下であり、他の形態では160mg/100g(乾燥重)以下である。通常、ホウレンソウ中の亜鉛濃度は0.7mg/100g(新鮮重)とされているが、本発明のホウレンソウはそれよりも高濃度の酸可溶性亜鉛を含有する。
尚、「地上部」には、葉及び/又は茎が含まれる。
【0022】
本発明のキャベツは、地上部に酸可溶性亜鉛を5mg/100g(乾燥重)以上、好ま
しくは10mg/100g(乾燥重)以上含有する。亜鉛濃度の上限は、特に制限されないが、通常100mg/100g(乾燥重)以下であり、他の形態では80mg/100g(乾燥重)以下である。通常、キャベツ中の酸可溶性亜鉛濃度は0.2mg/100g(乾燥重)とされているが、本発明のキャベツはそれよりも高濃度の酸可溶性亜鉛を含有する。
【0023】
本発明のトマトは、果実中に酸可溶性亜鉛を0.15mg/100g(新鮮重)以上、好ましくは0.16mg/100g以上(新鮮重)含有する。酸可溶性亜鉛濃度の上限は、特に制限されないが、通常1mg/100g(新鮮重)以下であり、他の形態では0.5mg/100g(新鮮重)以下である。通常、トマト果実中の酸可溶性亜鉛濃度は0.13mg/100gとされているが、本発明のトマトはそれよりも高濃度の酸可溶性亜鉛を果実中に含有する。
【0024】
本発明のコマツナは、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上、好ましくは20mg/100g(乾燥重)以上含有する。亜鉛濃度の上限は、特に制限されないが、通常500mg/100g(乾燥重)以下であり、他の形態では160mg/100g(乾燥重)以下である。通常、コマツナ中の亜鉛濃度は0.2mg/100g(新鮮重)とされているが、本発明のコマツナはそれよりも高濃度の酸可溶性亜鉛を含有する。
尚、「地上部」には、葉及び/又は茎が含まれる。
【0025】
本発明のレタスは、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上、好ましくは20mg/100g(乾燥重)以上含有する。亜鉛濃度の上限は、特に制限されないが、通常200mg/100g(乾燥重)以下であり、他の形態では160mg/100g(乾燥重)以下である。通常、コマツナ中の亜鉛濃度は0.2mg/100g(新鮮重)とされているが、本発明のコマツナはそれよりも高濃度の酸可溶性亜鉛を含有する。
尚、「地上部」には、葉及び/又は茎が含まれる。
【0026】
本発明のケールは、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上、好ましくは20mg/100g(乾燥重)以上含有する。亜鉛濃度の上限は、特に制限されないが、通常200mg/100g(乾燥重)以下であり、他の形態では160mg/100g(乾燥重)以下である。通常、コマツナ中の亜鉛濃度は0.3mg/100g(新鮮重)とされているが、本発明のコマツナはそれよりも高濃度の酸可溶性亜鉛を含有する。
尚、「地上部」には、葉及び/又は茎が含まれる。
【0027】
上記野菜中の亜鉛濃度は、例えば、原子吸光法、ICP発光分析法、ICP質量分析法、蛍光X線分析法等により測定することができる。酸可溶性亜鉛濃度は、野菜の葉部又は果実を酸溶液、例えば0.1N塩酸で抽出し、前記方法で亜鉛濃度を定量することによって、測定することができる。酸溶液での抽出に先立って、乾燥、粉砕等の前処理を行ってもよい。
【0028】
上記のような葉等の地上部、又は果実中に高濃度の酸可溶性亜鉛を含有する野菜は、亜鉛を0.001〜2重量%含有する液を、収穫前14日以内に野菜に葉面散布することにより製造できる。以下の記載において、野菜の製造方法、及び野菜製造用資材における野菜には、典型的にはホウレンソウ、キャベツ、トマトを含むが、これらには限定されない。
【0029】
本発明者等の検討によれば、野菜の葉等の地上部、又は果実中に酸可溶性亜鉛を高濃度で蓄積させるには、土壌散布でなく、葉面散布が好ましいことが判明した。従って、亜鉛を0.01〜2重量%含有する、野菜の葉面散布用液は、地上部又は果実中に酸可溶性亜
鉛を高含有する野菜製造用資材として有用である。
【0030】
本発明の野菜の製造方法の一形態は、亜鉛を0.001〜2重量%含有する液を、収穫日の0〜14日前、好ましくは0〜7日前、さらに好ましくは1〜7日前に、ホウレンソウの葉面に散布することを特徴とする、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するホウレンソウの製造法である。
【0031】
他の形態は、亜鉛を0.05〜2重量%含有する液を、収穫日の0〜14日前、好ましくは0〜7日前、さらに好ましくは1〜7日前に、にキャベツの葉面に散布することを特徴とする、地上部に酸可溶性亜鉛を5mg/100g(乾燥重)以上含有するキャベツの製造法である。
【0032】
さらに他の形態は、亜鉛を0.05〜2重量%含有する液を、収穫日の0〜40日前、好ましくは1〜30日前に、トマトの葉面に散布することを特徴とする、果実中に酸可溶性亜鉛を0.15mg/100g(新鮮重)以上含有するトマトの製造法である。
【0033】
さらに他の形態は、亜鉛を0.001〜2重量%含有する液を、収穫日の0〜14日前、好ましくは0〜7日前、さらに好ましくは1〜7日前に、コマツナの葉面に散布することを特徴とする、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するコマツナの製造法である。
【0034】
さらに他の形態は、亜鉛を0.001〜2重量%含有する液を、収穫日の0〜14日前、好ましくは0〜7日前、さらに好ましくは1〜7日前に、レタスの葉面に散布することを特徴とする、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するレタスの製造法である。
【0035】
さらに他の形態は、亜鉛を0.001〜2重量%含有する液を、収穫日の収穫日の0〜14日前、好ましくは0〜7日前、さらに好ましくは1〜7日前に、ケールの葉面に散布することを特徴とする、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するケールの製造法である。
【0036】
散布に用いる液(以下、「葉面散布資材」ということもある)は、亜鉛を0.001重量%以上、好ましくは0.005重量%以上、より好ましくは0.01重量%以上含有することが好ましい。亜鉛濃度の上限は、例えば2重量%以下、他の形態では1重量%以下である。また、葉面散布資材中の亜鉛濃度は、ホウレンソウ、コマツナ、レタス、ケール及びトマトでは0.005重量%以上が好ましく、キャベツでは0.05%以上が好ましい。
亜鉛含有液を調製するために用いる亜鉛としては水溶性があれば特に制限はなく、硫酸亜鉛、塩化亜鉛、硝酸亜鉛、蟻酸亜鉛、酢酸亜鉛等の亜鉛塩、又は、EDTA亜鉛のようなキレート体亜鉛などが挙げられる。このうち、葉への薬害軽減の点から硫酸亜鉛が特に好ましい。
【0037】
また、本発明で用いる葉面散布資材には、微生物又は微生物抽出物を含有させることにより、葉面への亜鉛の展着性が向上する。微生物としては特に制限されないが、細菌が好ましく、エシェリヒア(Escherichia)属、パントエア(Pantoea)属等の腸内細菌、又はコリネバクテリウム(Corynebacterium)属等のコリネ型細菌等が好ましい。これらの微生物又は微生物抽出物は水分を含んだままでもよいし、乾燥させてもよく、アミノ酸、核酸等の生産に用いた後の発酵副生液であってもよい。抽出物としては、熱水抽出物、酸性熱水抽出物、アルコール抽出物などが挙げられる。
【0038】
アミノ酸発酵副生液または核酸発酵副生液は、澱粉系及び糖蜜系を主原料とするグルタミン酸、リジン等の各種アミノ酸発酵副生液及びイノシン酸、グアニル酸、イノシン、グアノシン等の各種核酸発酵副生液である。具体的に、ここでいう副生液とは、リジン、グルタミンなどの塩基性または中性アミノ酸発酵液をpH調整した後、強酸性陽イオン樹脂に通じ、当該アミノ酸を吸着させた後の貫流液及びその濃縮液、並びに、グルタミン酸などの酸性アミノ酸発酵液を鉱酸でpHを等電点に調整し、析出した当該アミノ酸結晶を固液分離したときに得られる母液及びその濃縮液、核酸発酵液を、溶解度差を利用した冷却晶析及び濃縮晶析することで当該核酸を晶析し、析出した結晶を固液分離したときに得られる母液およびその濃縮液を例示することができる。これら発酵副生液には、固形分として、各種アミノ酸(濃縮液で5〜14重量%含有)、各種核酸の他、糖類、発酵菌体、有機態窒素、無機態窒素、ビタミン等の植物成長に必要な栄養分が多量に含まれており(固形分含量は30〜50重量%)、これらのなかにはフェニルアラニン発酵副生液である「PAL」(登録番号:生第74220号)、グルタミン発酵副生液である「グルタミン」(神奈川県第712号)のようにすでに液体副産窒素肥料として肥料登録され市販されているものもある。また、本発明の効果を阻害しない限り、これらアミノ酸発酵副生液に、所望により、窒素、リン酸、カリウム、ミネラル等の一般に考えられる肥料成分をさらに加えることも可能である。実施例で使用したDsTx−ML及びDSCLは、グルタミン酸発酵副生液であり、NAMLはイノシン酸、グアニル酸発酵副生液である。DsTx−MLはpH調整に塩酸を、DSCLはpH調整に硫酸を使用している。
【0039】
微生物又は微生物抽出物の葉面散布資材中の含有量は、微生物又は微生物抽出物、及び他の葉面散布資材成分(水分を含む)の合計量で、乾燥物換算で0.01〜20重量%、さらに0.1〜10重量%が好ましい。
【0040】
葉面散布資材には、葉面への付着性を高めるため、農業上通常用いられる展着剤、及び/または界面活性剤を添加してもよい。展着剤、界面活性剤は特に制限はないが、展着剤としては、例えばアプローチBI(花王(株)。「アプローチ」は同社の登録商標である。)、ミックスパワー(シンジェンタ ジャパン(株)。「ミックスパワー」は同社の登録商標である。)などが挙げられる。界面活性剤としては非イオン性、陰イオン性、陽イオン性及び両イオン性のいずれも使用することが出来る。例を挙げると、ポリオキシエチレンアルキルエーテル、ポリオキシエチレンアルキルアリールエーテル、ポリオキシエチレン脂肪酸エステル、ソルビタン脂肪酸エステル、ポリオキシエチレンソルビタン脂肪酸エステル、オキシエチレンポリマー、オキシプロピレンポリマー、ポリオキシエチレンアルキルリン酸エステル、脂肪酸塩、アルキル硫酸エステル塩、アルキルスルホン酸塩、アルキルアリールスルホン酸塩、アルキルリン酸塩、アルキルリン酸エステル塩、ポリオキシエチレンアルキル硫酸エステル、第四級アンモニウム塩、オキシアルキルアミン、レシチン、サポニン等である。また、必要に応じてゼラチン、カゼイン、デンプン、寒天、ポリビニルアルコール、アルギン酸ソーダなどを補助剤として用いることが出来る。
【0041】
葉面散布資材を散布する場合、農業上通常用いられる葉面散布用肥料と混合してもよい。この場合、肥料成分としては特に制限はないが、溶解後アルカリ性を示すものについては亜鉛が塩として沈殿を起こすため好ましくない場合がある。混合する場合に好ましい肥料成分を例示すれば、尿素、燐酸アンモニウム、塩酸アンモニウム、硫酸アンモニウム、燐酸、ピロ燐酸などが挙げられる。中でも尿素の混用は亜鉛の吸収量を高める場合があるため好ましい(Mortvedt, J.J. et al., 1993.”Zinc
fertilizers” in Robson, A.D. (Ed.) Zinc
in soils and plants (p.33−44), Kluweracademic publishers, Dordrecht, the Netherland)。
【0042】
本発明の野菜を栽培する場合の土壌に施用する基肥、追肥は、野菜の種類に応じてその地域で通常行われている施肥量・施肥方法に準拠すればよい。また、環境を損わない範囲で土壌を亜鉛処理してもよい。土壌の亜鉛処理によって、野菜中の亜鉛含量をさらに若干増加させることが出来る。
【0043】
本発明の野菜を栽培する場合の栽植密度は、野菜の種類に応じてその地域で推奨されている密度でよいが、畦間(条間)については葉面散布資材が下部の葉にも容易に到達できるよう、30cm以上とすることが好ましい。
【0044】
葉面散布資材の散布方法は特に制限されないが、野菜の地上部全体に葉面散布資材が展着するようにすることが望ましい。人手により散布する場合は、葉面散布資材の噴霧口が葉表面ないしは裏面部位に向くような操作が望まれる。また、ブームスプレーヤーを使用する場合は、散布液量を1ヘクタール当たり100リットル以上、好ましくは200〜3000リットル、より好ましくは300〜2000リットルとすることが望ましい。また、静電気を利用することにより噴霧液の植物体への付着を促進させるいわゆる静電噴霧機や静電噴霧ノズル口を用いてもよい。
【0045】
葉茎菜類の葉面散布資材の散布時期については、収穫日から14日以内、より好ましくは収穫日から7日以内の時期が好ましい。散布は、収穫同日でもよいが、少なくとも前日までに行うことが好ましい。散布回数は、適宜設定することができるが、1日1回から2週間に1回が好ましい。さらに1週間に1回散布することがより好ましい。また、作物生育期間中での合計散布回数は1〜3回が好ましい。
【0046】
果実類の葉面散布資材の散布時期については着蕾期から開花期を経て果実が成熟する時期までがよく、特に開花期〜成熟直前までの時期が好ましい。具体的には収穫日から40日以内、好ましくは収穫日から1〜30日前が好ましい。葉面散布資材の散布間隔については、適宜設定することができるが、1日1回から2週間に1回が好ましい。さらに1〜2週間に1回散布することがより好ましい。また、作物生育期間中での合計散布回数は2〜10回が好ましい。
【0047】
亜鉛以外のミネラル、例えば鉄、銅、カルシウム、マグネシウム、バナジウムなども、上記と同様にして、ミネラルを含有する液を野菜の葉面に散布することにより、野菜の地上部又は果実中の含量を高めることができる。
【実施例】
【0048】
次に実施例を示して本発明を更に詳細に説明するが、本発明は以下の実施例に限定されるものではない。
【0049】
〔実施例1〕
ホウレンソウは、楽秋ほうれん草(アタリヤ(株))を用いた。栽培には、5cm角のロックウール(日東紡社製、サイズV 50x50x50mm、ポリエチレンフィルムカバー無し)を用いた。肥料として、OptMS Zn(−)無機塩類培養液(表1)を栽培開始時および播種15日目に1回与え、水のみを週2回与えた。播種、栽培は、人工気象室(23℃)で実施した。光強度は100μmol m-2 s-1程度とし、14時間明期、10時間暗期のサイクルで、49日間栽培した。
植物への各試料液の散布は15時から17時の間に行なった。散布量は、およそ1ml/1個体で、収穫の7日前、5日前、2日前にそれぞれ散布した。亜鉛の根圏施肥を行なう場合は、1ml/1個体となるように収穫の22日前ないしは7日前に施肥した。各試料液は表2に示した。表2中、DsTx−MLは、L−グルタミン酸発酵副生液である。また、亜鉛濃度は亜鉛換算の%(w/v)濃度である(以下の記載においても同様である
。)。葉面散布にあたっては、SPRAY−WORK HG AIR COMPRESSOR REVO((株)タミヤ社製)を用い、すべての葉面に十分散布溶液が行き届くように散布した。試験は各処理n=3(3株)で行なった。また、実験に使用した亜鉛には、全て硫酸亜鉛を用いた。
【0050】
【表1】

【0051】
収穫は播種後49日目に行い、各個体の地上部を分離し、乾燥機内で80℃、3日間乾燥させた。乾燥後の地上部は乳鉢で粉砕した後、0.1gを秤量し、0.1N塩酸10mLを加え、37℃で3時間の抽出を行った。抽出液を更に0.1N塩酸で15倍(v/v)希釈し、その液中の亜鉛含量をICP発光分光分析装置ICPS−8100((株)島津製作所社製)によって測定した。測定値から、乾物重あたりの亜鉛含有量を算出した。
その結果は図1に示した。根圏に亜鉛を施用することでは、地上部中の酸可溶性亜鉛は僅かな上昇を示すものの、対照である水との差は小さかった。一方、等量の亜鉛(0.1%Zn)を根圏施肥した場合と葉面散布した場合を比較すると、葉面散布した場合の酸可溶性亜鉛の上昇は、根圏施肥した場合の7〜8倍となり、葉面散布処理が有効であることが明らかであった。また、1/10量の亜鉛を葉面散布した場合でも、酸可溶性亜鉛の上昇は、根圏散布に比べて2〜8倍高値を示し、葉面散布処理がヒト、動物に吸収されやすい酸可溶性亜鉛の上昇に有効であることを示している。
【0052】
【表2】

【0053】
〔実施例2〕
キャベツは、金系201号((株)サカタのタネ)を用いた。栽培には、パワーソイル(関東肥料工業(株))を内径6cmのポリプロピレン製ポット(日本ポリプロ(株))に0.1Lずつ充填したポットを用いた。肥料として、OptMS Zn(−)無機塩類培養液(表1)を播種18日目、33日目に2回与え、水のみを週2回与えた。播種、栽培は、人工気象室(23℃)で実施した。光強度は120μmol m-2 s-1程度とし、14時間明期、10時間暗期のサイクルで、39日間栽培した。
【0054】
栽培植物への各試料液の散布は15時から17時の間に行なった。散布量は、およそ0.25ml/1個体で、収穫の7日前、5日前、2日前に3回(計0.75ml/1個体)散布した。ミネラルの根圏施肥を行なう場合は、0.75ml/1個体となるように収穫の20日前に施肥した。各試料液は表3に示した。葉面散布にあたっては、SPRAY−WORK HG AIR COMPRESSOR REVO((株)タミヤ社製)を用い、すべての葉面に十分散布溶液が行き届くように散布した。試験は各処理n=3(3株)で行なった。また実験に使用した亜鉛には、全て硫酸亜鉛を用いた。同様に実験に使用した鉄、マグネシウム、カルシウム、銅には、それぞれ硫酸鉄、硫酸マグネシウム、硫酸カルシウム、硫酸銅を用いた。
【0055】
収穫は播種後39日目に行い、各個体の地上部を分離し、乾燥機内で80℃、3日間乾燥させた。乾燥後の地上部は乳鉢で粉砕した後、エネルギー分散型蛍光X線分析装置EDX−900HS((株)島津製作所社製)によって亜鉛含量を測定した。測定値から、乾物重あたりの亜鉛含有量を算出した。
【0056】
その結果は図2(亜鉛含量)、図3(鉄含量)に示した。根圏への亜鉛施用の有無に関わらず、地上部の亜鉛は検出限界以下であった。一方、葉面散布した場合は地上部の亜鉛の検出が可能となることから、葉面散布処理が有効であることが明らかとなった。また、この葉面散布処理は、L−グルタミン酸発酵副生液の存在下では、等量の亜鉛を葉面散布した場合と比較して5倍以上の高値を示し、亜鉛の上昇に有効であることを示している。また、同様に地上部の鉄量も特にL−グルタミン酸発酵副生液の存在下では、等量の鉄を
葉面散布した場合と比較して約2倍の高値を示し、鉄の上昇に有効であることを示している。これらの結果から、亜鉛のみでなく、鉄などのミネラル上昇にも葉面散布処理、特に発酵副生液を共存させた葉面散布処理が有効であることが示された。
【0057】
なお、「五訂増補日本食品標準成分表」による亜鉛高含有食品として知られているかき(生)中の平均的な亜鉛含量は132mg/kg、牛レバー(生)中の平均的な亜鉛含量は38mg/kgとされており、この点から考えると本実施例の亜鉛葉面散布によって牛レバーの2〜3倍、かきに匹敵する亜鉛含量をもつキャベツが得られたこととなる。また、L−グルタミン酸発酵副生液を亜鉛と併用した場合は、牛レバーの10〜20倍、かきの4〜5倍の亜鉛含量をもつキャベツが得られたこととなる。
【0058】
【表3】

【0059】
〔実施例3〕発酵副生液の展着性の評価
(表面張力値試験)
発酵副生液の展着剤としての効力の目安として、表面張力値をウイルヘルミイ(Wihelmy)法(J. Physiol. (1979), 295, 217−227)にて測定した。測定には、表面張力測定装置CBVP−A3(協和界面科学(株))を用いた。測定したサンプルは、市販の展着剤アプローチBI(花王(株))、グルタミン酸発酵副生液(DsTx−ML、DSCL)、核酸発酵副生液(NAML)のそれぞれ希釈溶液である。
【0060】
試験結果は図4に示すとおりである。この試験結果から明らかなように、発酵副生液は、0.2%〜2%という低濃度においても市販の展着剤に匹敵する表面張力の低下作用を有し、濡れ難い植物であるキャベツなどへの展着において有利である。
【0061】
〔実施例4〕
トマトはマイクロトムを用いた。栽培には、パワーソイル(関東肥料工業(株))を内径6cmのポリプロピレン製ポット(日本ポリプロ(株))に0.1Lずつ充填したポッ
トを用いた。肥料として、OptMS Zn(−)無機塩類培養液(表1)を播種20日目、47日目に2回与え、水のみを週2回与えた。播種、栽培は、人工気象室(23℃)で実施した。光強度は120μmol m-2 s-1程度とし、14時間明期、10時間暗期のサイクルで、78日間栽培した。約49日後に開花し、62日後に結実した。
【0062】
栽培植物への各試料液の散布は15時から17時の間に行なった。散布量は、およそ0.5ml/1個体で、表4に記載したタイミングでそれぞれ散布した。各試料液は表4に示した。葉面散布にあたっては、SPRAY−WORK HG AIR COMPRESSOR REVO((株)タミヤ社製)を用い、すべての葉面に十分散布溶液が行き届くように散布した。試験は各処理n=5(5株)で行なった。また実験に使用した亜鉛は全て硫酸亜鉛を用いた。
【0063】
収穫は播種後78日目に行い、各固体の果実を収穫し、ミキサーで粉砕した。粉砕試料1gを秤量し、0.1N塩酸9mLを加え、37℃で3時間の抽出を行った。抽出液中の亜鉛含量をICP発光分光分析装置ICPS−8100((株)島津製作所社製)によって測定した。測定値から、新鮮重あたりの亜鉛含有量を算出した。
【0064】
その結果は図4に示した。亜鉛(0.01%Zn)を葉面散布した場合、水を葉面散布した場合と比較して酸可溶性亜鉛が上昇し、果実への亜鉛の蓄積においても、葉面散布処理が有効であることが明らかとなり、葉面散布処理がヒト、動物に吸収されやすい酸可溶性亜鉛の上昇に有効であることを示している。亜鉛散布のタイミングとしては、生育初期からの散布でも有効であるが、開花後の散布でも同様に有効であった。
【0065】
【表4】

【0066】
〔実施例5〕
コマツナは、コマツナ(サカタのタネ)を用いた。栽培には、5cm角のロックウール(日東紡社製、サイズV 50x50x50mm、ポリエチレンフィルムカバー無し)を用いた。肥料として、OptMS Zn(−)無機塩類培養液(表1)を栽培開始時および播種10日目に1回与え、水のみを週2回与えた。播種、栽培は、人工気象室(23℃)で実施した。光強度は120μmol m-2 s-1程度とし、14時間明期、10時間暗期のサイクルで、24日間栽培した。
植物への各試料液の散布は15時から17時の間に行なった。散布量は、およそ1ml/1個体で、収穫の5日前、2日前にそれぞれ散布した。亜鉛の根圏施肥を行なう場合は、1ml/1個体となるように収穫の22日前ないしは7日前に施肥した。各試料液は表5に示した。表5中、DsTx−MLは、L−グルタミン酸発酵副生液である。また、亜鉛濃度は亜鉛換算の%(w/v)濃度である(以下の記載においても同様である。)。葉
面散布にあたっては、SPRAY−WORK HG AIR COMPRESSOR REVO((株)タミヤ社製)を用い、すべての葉面に十分散布溶液が行き届くように散布した。試験は各処理n=3(3株)で行なった。また、実験に使用した亜鉛には、全て硫酸亜鉛を用いた。
【0067】
収穫は播種後24日目に行い、各個体の地上部を分離し、乾燥機内で80℃、3日間乾燥させた。乾燥後の地上部は乳鉢で粉砕した後、0.1gを秤量し、0.1N塩酸10mLを加え、37℃で3時間の抽出を行った。抽出液を更に0.1N塩酸で15倍(v/v)希釈し、その液中の亜鉛含量をICP発光分光分析装置ICPS−8100((株)島津製作所社製)によって測定した。測定値から、乾物重あたりの亜鉛含有量を算出した。
その結果は図6に示した。根圏に亜鉛を施用することでは、地上部中の酸可溶性亜鉛は僅かな上昇を示すものの、対照である水との差は小さかった。一方、等量の亜鉛(0.1%Zn)を根圏施肥した場合と葉面散布した場合を比較すると、葉面散布した場合の酸可溶性亜鉛の上昇は、根圏施肥した場合の2〜3倍となり、葉面散布処理が有効であることが明らかであった。また、1/10量の亜鉛を葉面散布した場合でも、酸可溶性亜鉛の上昇は、根圏散布に比べて約3倍高値を示し、葉面散布処理がヒト、動物に吸収されやすい酸可溶性亜鉛の上昇に有効であることを示している。また、この葉面散布処理は、L−グルタミン酸発酵副生液の存在下では、等量の亜鉛を葉面散布した場合と比較して3〜5倍以上の高値を示し、亜鉛の上昇に有効であることを示している。
【0068】
【表5】

【0069】
〔実施例6〕
レタスは、カキチシャ チマ・サンチュ(サカタのタネ)を用いた。栽培には、5cm角のロックウール(日東紡社製、サイズV 50x50x50mm、ポリエチレンフィルムカバー無し)を用いた。肥料として、OptMS Zn(−)無機塩類培養液(表1)を栽培開始時および播種10日目に1回与え、水のみを週2回与えた。播種、栽培は、人工気象室(23℃)で実施した。光強度は120μmol m-2 s-1程度とし、14時間明期、10時間暗期のサイクルで、27日間栽培した。
植物への各試料液の散布は15時から17時の間に行なった。散布量は、およそ1ml/1個体で、収穫の7日前、5日前、2日前にそれぞれ散布した。亜鉛の根圏施肥を行なう場合は、1ml/1個体となるように収穫の24日前ないしは7日前に施肥した。各試料液は表6に示した。表6中、DsTx−MLは、L−グルタミン酸発酵副生液である。また、亜鉛濃度は亜鉛換算の%(w/v)濃度である(以下の記載においても同様である。)。葉面散布にあたっては、SPRAY−WORK HG AIR COMPRESS
OR REVO((株)タミヤ社製)を用い、すべての葉面に十分散布溶液が行き届くように散布した。試験は各処理n=3(3株)で行なった。また、実験に使用した亜鉛には、全て硫酸亜鉛を用いた。
【0070】
収穫は播種後24日目に行い、各個体の地上部を分離し、乾燥機内で80℃、3日間乾燥させた。乾燥後の地上部は乳鉢で粉砕した後、0.1gを秤量し、0.1N塩酸10mLを加え、37℃で3時間の抽出を行った。抽出液を更に0.1N塩酸で15倍(v/v)希釈し、その液中の亜鉛含量をICP発光分光分析装置ICPS−8100((株)島津製作所社製)によって測定した。測定値から、乾物重あたりの亜鉛含有量を算出した。
その結果は図7に示した。根圏に亜鉛を施用することでは、地上部中の酸可溶性亜鉛は僅かな上昇を示すものの、対照である水との差は小さかった。一方、等量の亜鉛(0.1%Zn)を根圏施肥した場合と葉面散布した場合を比較すると、葉面散布した場合の酸可溶性亜鉛の上昇は、根圏施肥した場合の6〜10倍となり、葉面散布処理が有効であることが明らかであった。また、1/10量の亜鉛を葉面散布した場合でも、酸可溶性亜鉛の上昇は、根圏散布に比べて2倍以上高値を示し、葉面散布処理がヒト、動物に吸収されやすい酸可溶性亜鉛の上昇に有効であることを示している。また、この葉面散布処理は、L−グルタミン酸発酵副生液の存在下では、等量の亜鉛を葉面散布した場合と比較して約1.5倍の高値を示し、亜鉛の上昇に有効であることを示している。
【0071】
【表6】

【0072】
〔実施例7〕
ケールは、ケール(サカタのタネ)を用いた。栽培には、5cm角のロックウール(日東紡社製、サイズV 50x50x50mm、ポリエチレンフィルムカバー無し)を用いた。肥料として、OptMS Zn(−)無機塩類培養液(表1)を栽培開始時および播種10日目に1回与え、水のみを週2回与えた。播種、栽培は、人工気象室(23℃)で実施した。光強度は120μmol m-2 s-1程度とし、14時間明期、10時間暗期のサイクルで、27日間栽培した。
植物への各試料液の散布は15時から17時の間に行なった。散布量は、およそ1ml/1個体で、収穫の7日前、5日前、2日前にそれぞれ散布した。亜鉛の根圏施肥を行なう場合は、1ml/1個体となるように収穫の24日前ないしは7日前に施肥した。各試
料液は表7に示した。表7中、DsTx−MLは、L−グルタミン酸発酵副生液である。また、亜鉛濃度は亜鉛換算の%(w/v)濃度である(以下の記載においても同様である。)。葉面散布にあたっては、SPRAY−WORK HG AIR COMPRESSOR REVO((株)タミヤ社製)を用い、すべての葉面に十分散布溶液が行き届くように散布した。試験は各処理n=3(3株)で行なった。また、実験に使用した亜鉛には、全て硫酸亜鉛を用いた。
【0073】
収穫は播種後24日目に行い、各個体の地上部を分離し、乾燥機内で80℃、3日間乾燥させた。乾燥後の地上部は乳鉢で粉砕した後、0.1gを秤量し、0.1N塩酸10mLを加え、37℃で3時間の抽出を行った。抽出液を更に0.1N塩酸で15倍(v/v)希釈し、その液中の亜鉛含量をICP発光分光分析装置ICPS−8100((株)島津製作所社製)によって測定した。測定値から、乾物重あたりの亜鉛含有量を算出した。
その結果は図8に示した。根圏に亜鉛を施用することでは、地上部中の酸可溶性亜鉛は僅かな上昇を示すものの、対照である水との差は小さかった。一方、等量の亜鉛(0.1%Zn)を根圏施肥した場合と葉面散布した場合を比較すると、葉面散布した場合の酸可溶性亜鉛の上昇は、根圏施肥した場合の3〜4倍となり、葉面散布処理が有効であることが明らかであった。これらの結果は、葉面散布処理がヒト、動物に吸収されやすい酸可溶性亜鉛の上昇に有効であることを示している。また、この葉面散布処理は、L−グルタミン酸発酵副生液の存在下では、等量の亜鉛を葉面散布した場合と比較して2〜6倍の高値を示し、亜鉛の上昇に有効であることを示している。
【0074】
【表7】

【特許請求の範囲】
【請求項1】
地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するホウレンソウ。
【請求項2】
亜鉛含有量が200mg/100g以下である、請求項1に記載のホウレンソウ。
【請求項3】
地上部に酸可溶性亜鉛を5mg/100g(乾燥重)以上含有するキャベツ。
【請求項4】
亜鉛含有量が100mg/100g(乾燥重)以下である、請求項3に記載のキャベツ。
【請求項5】
果実に酸可溶性亜鉛を0.15mg/100g(新鮮重)以上含有するトマト。
【請求項6】
亜鉛含有量が1mg/100g(新鮮重)以下である、請求項5に記載のトマト。
【請求項7】
地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するコマツナ。
【請求項8】
亜鉛含有量が500mg/100g(乾燥重)以下である、請求項7に記載のコマツナ。
【請求項9】
地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するレタス。
【請求項10】
亜鉛含有量が200mg/100g以下(乾燥重)である、請求項9に記載のレタス。
【請求項11】
地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するケール。
【請求項12】
亜鉛含有量が200mg/100g(乾燥重)以下である、請求項11に記載のケール。
【請求項13】
亜鉛を0.001〜2重量%含有する液を、収穫日の0〜14日前にホウレンソウの葉面に散布することを特徴とする、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するホウレンソウの製造法。
【請求項14】
亜鉛を0.05〜2重量%含有する液を、収穫日の0〜14日前にキャベツの葉面に散布することを特徴とする、地上部に酸可溶性亜鉛を5mg/100g(乾燥重)以上含有するキャベツの製造法。
【請求項15】
亜鉛を0.05〜2重量%含有する液を、収穫日の0〜40日前にトマトの葉面に散布することを特徴とする、果実中に酸可溶性亜鉛を0.15mg/100g(新鮮重)以上含有するトマトの製造法。
【請求項16】
亜鉛を0.001〜2重量%含有する液を、収穫日の0〜14日前にコマツナの葉面に散布することを特徴とする、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するコマツナの製造法。
【請求項17】
亜鉛を0.001〜2重量%含有する液を、収穫日の0〜14日前にレタスの葉面に散布することを特徴とする、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するレタスの製造法。
【請求項18】
亜鉛を0.001〜2重量%含有する液を、収穫日の0〜14日前にケールの葉面に散
布することを特徴とする、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するケールの製造法。
【請求項19】
亜鉛を含有する液が、さらに微生物又は微生物抽出物を含有する、請求項13〜18のいずれか一項に記載の方法。
【請求項20】
亜鉛を含有する液の散布量が、1ヘクタール当たり500リットル以上である、請求項13〜19のいずれか一項に記載の方法。
【請求項21】
ミネラルを含有する液を野菜の葉面に散布することにより、野菜の地上部又は果実中のミネラル含量を高める方法。
【請求項22】
酸可溶性亜鉛を高含有する野菜の製造に用いられる野菜製造用資材であって、亜鉛を0.001〜2重量%含有し、使用に際して葉面散布される、野菜製造用資材。
【請求項23】
さらに、微生物又は微生物抽出物を含有する、前記野菜製造用資材。
【請求項1】
地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するホウレンソウ。
【請求項2】
亜鉛含有量が200mg/100g以下である、請求項1に記載のホウレンソウ。
【請求項3】
地上部に酸可溶性亜鉛を5mg/100g(乾燥重)以上含有するキャベツ。
【請求項4】
亜鉛含有量が100mg/100g(乾燥重)以下である、請求項3に記載のキャベツ。
【請求項5】
果実に酸可溶性亜鉛を0.15mg/100g(新鮮重)以上含有するトマト。
【請求項6】
亜鉛含有量が1mg/100g(新鮮重)以下である、請求項5に記載のトマト。
【請求項7】
地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するコマツナ。
【請求項8】
亜鉛含有量が500mg/100g(乾燥重)以下である、請求項7に記載のコマツナ。
【請求項9】
地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するレタス。
【請求項10】
亜鉛含有量が200mg/100g以下(乾燥重)である、請求項9に記載のレタス。
【請求項11】
地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するケール。
【請求項12】
亜鉛含有量が200mg/100g(乾燥重)以下である、請求項11に記載のケール。
【請求項13】
亜鉛を0.001〜2重量%含有する液を、収穫日の0〜14日前にホウレンソウの葉面に散布することを特徴とする、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するホウレンソウの製造法。
【請求項14】
亜鉛を0.05〜2重量%含有する液を、収穫日の0〜14日前にキャベツの葉面に散布することを特徴とする、地上部に酸可溶性亜鉛を5mg/100g(乾燥重)以上含有するキャベツの製造法。
【請求項15】
亜鉛を0.05〜2重量%含有する液を、収穫日の0〜40日前にトマトの葉面に散布することを特徴とする、果実中に酸可溶性亜鉛を0.15mg/100g(新鮮重)以上含有するトマトの製造法。
【請求項16】
亜鉛を0.001〜2重量%含有する液を、収穫日の0〜14日前にコマツナの葉面に散布することを特徴とする、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するコマツナの製造法。
【請求項17】
亜鉛を0.001〜2重量%含有する液を、収穫日の0〜14日前にレタスの葉面に散布することを特徴とする、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するレタスの製造法。
【請求項18】
亜鉛を0.001〜2重量%含有する液を、収穫日の0〜14日前にケールの葉面に散
布することを特徴とする、地上部に酸可溶性亜鉛を10mg/100g(乾燥重)以上含有するケールの製造法。
【請求項19】
亜鉛を含有する液が、さらに微生物又は微生物抽出物を含有する、請求項13〜18のいずれか一項に記載の方法。
【請求項20】
亜鉛を含有する液の散布量が、1ヘクタール当たり500リットル以上である、請求項13〜19のいずれか一項に記載の方法。
【請求項21】
ミネラルを含有する液を野菜の葉面に散布することにより、野菜の地上部又は果実中のミネラル含量を高める方法。
【請求項22】
酸可溶性亜鉛を高含有する野菜の製造に用いられる野菜製造用資材であって、亜鉛を0.001〜2重量%含有し、使用に際して葉面散布される、野菜製造用資材。
【請求項23】
さらに、微生物又は微生物抽出物を含有する、前記野菜製造用資材。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【公開番号】特開2013−48558(P2013−48558A)
【公開日】平成25年3月14日(2013.3.14)
【国際特許分類】
【出願番号】特願2009−283348(P2009−283348)
【出願日】平成21年12月14日(2009.12.14)
【出願人】(000000066)味の素株式会社 (887)
【Fターム(参考)】
【公開日】平成25年3月14日(2013.3.14)
【国際特許分類】
【出願日】平成21年12月14日(2009.12.14)
【出願人】(000000066)味の素株式会社 (887)
【Fターム(参考)】
[ Back to top ]

