金属ナノ粒子の製造方法
【課題】シングルナノサイズで単分散性を有する金属ナノ粒子を連続的に製造可能な金属ナノ粒子の製造方法を提供する。
【解決手段】第1混合工程P1で得られたヒドラジン錯体を含む溶液と、アルカリ溶液とが、第2混合工程P2において、それらの噴射流を相互に衝突させることで瞬時に混合されることから、アルカリ下において開始される粒成長の時間が大幅に短縮されるので、シングルナノサイズで単分散性を有する優れた金属ナノ粒子が得られる。また、ヒドラジンを還元剤とする金属ナノ粒子の生成機構は、ヒドラジン錯体とアルカリとの間の配位子交換反応から放出されたヒドラジンによる水酸化物の還元であることから、金属塩溶液から直接に金属ナノ粒子を製造する方法と比較して、溶液中での還元剤濃度を低くすることができるので、得られた金属ナノ粒子はより少ない凝集性とより良い分散性を得ることができる。
【解決手段】第1混合工程P1で得られたヒドラジン錯体を含む溶液と、アルカリ溶液とが、第2混合工程P2において、それらの噴射流を相互に衝突させることで瞬時に混合されることから、アルカリ下において開始される粒成長の時間が大幅に短縮されるので、シングルナノサイズで単分散性を有する優れた金属ナノ粒子が得られる。また、ヒドラジンを還元剤とする金属ナノ粒子の生成機構は、ヒドラジン錯体とアルカリとの間の配位子交換反応から放出されたヒドラジンによる水酸化物の還元であることから、金属塩溶液から直接に金属ナノ粒子を製造する方法と比較して、溶液中での還元剤濃度を低くすることができるので、得られた金属ナノ粒子はより少ない凝集性とより良い分散性を得ることができる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、ナノメートルサイズで粒子分布の狭い単分散性を有する優れた金属ナノ粒子を連続的に製造可能な方法に関するものである。
【背景技術】
【0002】
特許文献1および特許文献2では、平行層流型マイクロリアクターを用いて単分散性を有する銀或いは白金の金属ナノ粒子を連続的に形成する方法が提案されている。この方法は、金属塩溶液を通す第1の流路と還元剤溶液を通る第2の流路とを形成し、それら金属塩溶液および還元剤溶液がそれぞれ薄い厚みの層状を成して流れる領域内の少なくとも一箇所において2溶液の接触界面を形成し、その接触界面を有する部分の2溶液の薄い層状の流れの厚さを、接触界面の法線方向で1〜500μmとし、その接触界面において金属イオンと還元剤とを相互に拡散且つ移動させ、金属イオンと還元剤とを相互に反応させることで、連続的に金属ナノ粒子を製造する。しかし、この方法では、酸化し難い安定な金属である銀、白金等の金属ナノ粒子の製造を対象としていて、ヒドラジンを還元剤とした液相法で金属ナノ粒子を製造する場合には反応時間が長くなり過ぎるので、ブロードな分布の金属ナノ粒子しか得られないという問題がある。
【0003】
これに対し、特許文献3では、金属として不安定なニッケルのナノ粒子を狭い粒子分布且つ優れた単分散性で得ることを目的とした製造方法が提案されている。この製造方法は、ニッケル前駆体、界面活性剤、疎水性溶媒を含む逆マイクロエマルジョン水溶液に、ヒドラジン水和物を添加して30分混合することでニッケル−ヒドラジン着物を形成し、そのニッケル−ヒドラジン着物を含む逆マイクロエマルジョンに還元剤(NaBH4)を添加して1時間混合することでニッケルナノ粒子を形成するものである。
【先行技術文献】
【特許文献】
【0004】
【特許文献1】特開2003−192344号公報
【特許文献2】特開2003−193119号公報
【特許文献3】特開2007−277709号公報
【発明の概要】
【発明が解決しようとする課題】
【0005】
しかしながら、上記特許文献3に記載のニッケルナノ粒子の製造方法では、100nm以下、好ましくは10乃至50nmの狭い粒度分布を有するニッケルナノ粒子が得られるとされているが、それは未だ大きな粒径に過ぎず、シングルナノサイズすなわち1桁のナノサイズで単分散性を有する金属ナノ粒子が得られないという、欠点があった。すなわち、攪拌機を備えた反応容器内に金属イオンを溶解した溶液にヒドラジン溶液を添加した後、アルカリを添加して還元反応させる、ヒドラジンを還元剤とした液相法で製造する金属ナノ粒子の製造方法では、いずれの攪拌方法を用いてもアルカリの添加によって還元が開始して核形成と粒成長とが同時に発生することから、20nm〜1μmサイズの金属粒子が生成され、シングルナノサイズで単分散性を有する金属ナノ粒子を得ることが困難であった。
【0006】
本発明は、以上の事情を背景として為されたものであって、その目的とするところは、シングルナノサイズで単分散性を有する金属ナノ粒子を連続的に製造可能な金属ナノ粒子の製造方法を提供することにある。
【課題を解決するための手段】
【0007】
すなわち、本発明者等は、以上の事情を背景として種々研究を重ねた結果、金属イオンを溶解した金属塩溶液にヒドラジン溶液を混合後、直ちにその混合液とアルカリの溶液とを瞬時に均一混合させることが、還元反応時間を可及的に短縮することにつながり、シングルナノサイズで単分散性を有する金属ナノ粒子を得るために有効であるという考え方に到達した。そして、それを実現するために中心衝突型マイクロリアクターを用いて、中央に位置する反応室に向かってその反応室に連通する複数のマイクロチャネル(噴射通路)を通して上記混合液とアルカリの溶液とを噴射し、相互に衝突させて瞬時に混合させると、従来では製造困難であったシングルナノサイズで単分散性を有する金属ナノ粒子が得られるという事実を見いだした。本発明はその知見に基づいて為されたものである。
【0008】
すなわち、本発明の要旨とするところは、(a)金属イオンを溶解した金属塩溶液にヒドラジン溶液を混合して得たヒドラジン錯体を、アルカリ溶液によって還元することにより金属ナノ粒子を製造する金属ナノ粒子の製造方法であって、(b)前記金属イオンを溶解した金属塩溶液に前記ヒドラジン溶液を混合して前記ヒドラジン錯体を生成する第1混合工程と、(c)第1混合工程で得られた前記ヒドラジン錯体を含む溶液の噴流とアルカリ溶液の噴流とを相互に衝突させることにより、該前記ヒドラジン錯体を含む溶液とアルカリ溶液とを混合して前記金属ナノ粒子を生成する第2混合工程とを、含むことにある。
【発明の効果】
【0009】
本発明の金属ナノ粒子の製造方法によれば、第1混合工程で得られた前記ヒドラジン錯体を含む溶液とアルカリ溶液とが、第2混合工程において、それらの噴射流を相互に衝突させることで瞬時に混合されることから、アルカリ下において開始される粒成長の時間が大幅に短縮されるので、シングルナノサイズで単分散性を有する優れた金属ナノ粒子が得られる。また、ヒドラジン溶液を還元剤とする金属ナノ粒子の生成機構は、ヒドラジン錯体とアルカリとの間の配位子交換反応から放出されたヒドラジンによる水酸化物の還元であることから、金属塩溶液から直接に金属ナノ粒子を製造する方法と比較して、溶液中での還元剤濃度を低くすることができるので、得られた金属ナノ粒子はより少ない凝集性とより良い分散性を得ることができる。
【0010】
ここで、好適には、前記第2混合工程は、中心衝突型マイクロリアクターを用いて前記第1混合工程で得られた前記ヒドラジン錯体を含む溶液とアルカリ溶液とを混合する。このようにすれば、第2混合工程で、前記ヒドラジン錯体を含む溶液とアルカリ溶液とが、中心衝突型マイクロリアクターにおいて、それらの噴射流を相互に衝突させることで瞬時に混合されることから、アルカリ下において開始される粒成長の時間が大幅に短縮されるので、シングルナノサイズで単分散性を有する優れた金属ナノ粒子が得られる。
【0011】
また、好適には、前記金属塩溶液は、ニッケル、鉄、コバルト、銅のいずれかの金属イオンが溶解した溶液である。このような、酸化容易性を有するなどの比較的不安定な金属であっても、シングルナノサイズで単分散性を有する優れた金属ナノ粒子が得られる。
【0012】
また、好適には、前記金属ナノ粒子は、5nm以下の平均粒径を有するものであるので、シングルナノサイズで単分散性を有する優れた金属ナノ粒子が得られる。
【0013】
また、好適には、前記第1混合工程は、中心衝突型マイクロリアクターを用いて前記金属塩溶液と前記ヒドラジン溶液とを混合する。このようにすれば、第1混合工程で、前記金属塩溶液とヒドラジン溶液とが、中心衝突型マイクロリアクターにおいて、それらの噴射流を相互に衝突させることで瞬時に混合されることから、ヒドラジン錯体が生成されるときに核生成が短時間で均一に行なわれるので、その混合溶液を直ちにアルカリ下で還元反応させることによりシングルナノサイズでたとえば変動係数が0.21以下の単分散性を有する優れた金属ナノ粒子が得られる。
【0014】
また、前記金属塩溶液としては、硝酸塩、硫酸塩、アンモニウム塩、炭酸塩、ハロゲン塩などの無機塩類の他、カルボン酸塩、水酸化物などが用いられる。この金属塩の濃度は、25mM程度が望ましく、2種類以上の金属塩を組み合わせることで、合金やコアシェル型のナノ粒子を製造することができる。コアシェル型のナノ粒子を製造する場合は、第2混合工程の後に、外皮を構成する金属イオンを溶解した金属塩溶液をさらに混合させる。
【0015】
また、前記ヒドラジン濃度は、金属塩溶液中の金属イオン濃度に対して20倍程度に高いことが望ましい。ヒドラジン濃度が金属イオン濃度よりも低いと核生成する金属が少なく、金属塩溶液中に残存する金属イオンが多くなって核生成とその後につづく粒成長とを分離できなくなり、結果として単分散な金属ナノ粒子を得ることができなくなる。反対に、ヒドラジン濃度が高すぎると核生成した金属が重合し過ぎて大きな粒径の金属粒子が含まれるようになる。
【0016】
また、前記アルカリ溶液としては、水酸化ナトリウム溶液が好適に用いられるが、リチウム、カリウム、ルビシウム、セシウムなどのアルカリ金属の水酸化物を水に溶解させたものであればよい。
【0017】
また、前記金属イオンを溶解した金属塩溶液とヒドラジン溶液とを混合して生成されたヒドラジン錯体をアルカリ溶液中で還元するまでの時間は、金属塩溶液とヒドラジン溶液とを均一に混合させてヒドラジン錯体を十分に生成させるまでの時間は必要であるが、可及的に短い時間であることが望ましい。前記第1混合工程において中心衝突型マイクロリアクターを用いて金属塩溶液とヒドラジン溶液とが混合される場合は、0.05秒乃至1.5秒の範囲内が望ましい。前記第1混合工程においてY字型コネクタを用いて金属塩溶液とヒドラジン溶液とが混合される場合は、1.0秒乃至1.5秒の範囲内が望ましい。
【0018】
また、前記金属塩溶液には、金属ナノ粒子を表面に吸着させる安定化剤(分散剤)を含有させることが望ましい。安定化剤により粒子表面を表面修飾した状態で溶媒中に分散することができ、安定な金属ナノ粒子含有分散液すなわちコロイド溶液が得られる。この場合の安定化剤の添加量は、コロイドの分散性を十分に高める程度でよく、特に制限はない。安定化剤としては、例えばヘキサデシルトリメチルアンモニウムブロマイドのようなアンモニウム塩、例えばドデシルベンゼンスルホン酸ナトリウムのようなスルホン酸塩、例えばペンタエチレングリコールドデシルエーテルのようなエーテル類、ポリビニルビロリドンなどが、好適に用いられる。
【0019】
また、第1混合工程および第2混合工程、特に第2混合工程における混合操作は、分子拡散、乱流混合或いは層流混合に分類される。分子拡散は、Fickの法則に支配され、混合時間をt、拡散距離をd、拡散定数をDとすると、t=d2/Dにより表わされるので、拡散距離dを短くすることで効果的に拡散時間tを短縮できる。この拡散距離dを短くしたマイクロ流路での混合では、分子拡散か層流拡散にならざるを得ないが、層流の厚みを小さくすることに限界がある。このため、第1混合工程および第2混合工程、特に第2混合工程では、噴射型混合器の一種である中心衝突型マイクロリアクターすなわち中心衝突型マイクロミキサーが好適に用いられる。この中心衝突型マイクロリアクターでは、200〜600μmφの混合室と、100〜200μmの幅寸法を有してその混合室の周囲からその混合室に連通する径方向の少なくとも1対のマイクロ流路とが放射状に設けられ、そのマイクロ流路を通してヒドラジン錯体を含む溶液とアルカリ溶液とを噴射することで、両液が混合室内で衝突して乱流が発生させられ、瞬時に均一混合されるようになっている。
【図面の簡単な説明】
【0020】
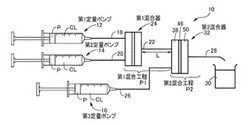
【図1】本発明方法を実施するための第1実施例の混合装置の構成を模式的に示す図である。
【図2】図1の中心衝突型マイクロリアクターの構成を、一部を切り欠いて説明する正面図である。
【図3】図1の混合装置において第1混合器から吐出されたヒドラジン錯体を含む溶液の流路長すなわちヒドラジン錯体の滞留長を変化させてニッケルナノ粒子を生成したときに、得られたニッケルナノ粒子の平均粒径および変動係数を示す図表である。
【図4】図3の混合装置を用いて、ヒドラジン錯体の滞留長が1cmである場合に得られたニッケルナノ粒子の粒度分布を示す図である。
【図5】図3の混合装置を用いて、ヒドラジン錯体の滞留長が3cmである場合に得られたニッケルナノ粒子の粒度分布を示す図である。
【図6】図3の混合装置を用いて、ヒドラジン錯体の滞留長が20cmである場合に得られたニッケルナノ粒子の粒度分布を示す図である。
【図7】図3の混合装置を用いて、ヒドラジン錯体の滞留長が3cmである場合に得られたニッケルナノ粒子を透過型電子顕微鏡TEMで観察したときの写真を示す図である。
【図8】図3の混合装置を用いて、ヒドラジン錯体の滞留長が40cmである場合に得られたニッケルナノ粒子の粒度分布を示す図である。
【図9】本発明の第2実施例の混合装置を模式的に示す図であって、図1に相当する図である。
【図10】図1の混合装置を用いてヒドラジン濃度を低くしてニッケルナノ粒子を生成した比較例1において、得られたニッケルナノ粒子の粒度分布を示す図である。
【図11】比較例2の混合装置の構成を模式的に示す図である。
【図12】図11の比較例2の混合装置を用いて得られたニッケルナノ粒子の粒度分布を示す図である。
【図13】比較例3の混合装置の構成を模式的に示す図である。
【発明を実施するための形態】
【0021】
以下、本発明の一適用例を図面を参照して詳細に説明する。なお、以下の実施例において装置を説明する図は適宜簡略化された模式図であって、各部の寸法比および形状等は必ずしも正確に描かれていない。
【実施例1】
【0022】
図1は、本発明方法が適用される一例の、金属ナノ粒子製造用の反応装置すなわち混合装置10の構成を説明する図である。図1において、混合装置10は、一定濃度の金属塩溶液たとえば塩化ニッケル溶液(NiCl2)と安定化剤溶液(CTAB)溶液との混合液を一定流量で吐出する第1定量ポンプ12と、塩化ニッケル溶液よりも大きく設定された一定流量で且つ塩化ニッケル溶液の濃度よりも高く設定された一定濃度のヒドラジン溶液(N2H4)を吐出する第2定量ポンプ14と、一定流量でアルカリ溶液(NaOH)を吐出する第3定量ポンプ16と、第1定量ポンプ12に第1接続管18を介して接続されるとともに第2定量ポンプ14に第2接続管20を介して接続され、第1定量ポンプ12から吐出された塩化ニッケル溶液と第2定量ポンプ14から吐出されたヒドラジン溶液とを瞬時に混合して混合溶液を第3接続管22を通して出力する第1混合器24と、第3接続管22を介して第1混合器24と接続され且つ第4接続管26を介して第3定量ポンプ16と接続され、第1混合器24から出力されたヒドラジン錯体を含む溶液と第3定量ポンプ16から吐出されたアルカリ溶液とを瞬時に混合して反応生成されたニッケルナノ粒子を含むコロイド溶液を第5接続管28を通して出力槽30へ出力してそれに貯留させる第2混合器32とを備えている。上記CTABは、安定化剤或いは界面活性剤として機能する臭化ヘキサデシルトリメチルアンモニウムである。
【0023】
上記第1定量ポンプ12、第2定量ポンプ14、および第3定量ポンプ16は、溶液が収容されたシリンダCLとそのシリンダCLに摺動可能に嵌合されてシリンダCL内の溶液を押し出すピストンPと、そのピストンPを一定速度で駆動する図示しない駆動装置とを備え、単位時間あたりに一定の容積を吐出するシリンダ型定量ポンプにより構成されている。しかし、上記第1定量ポンプ12、第2定量ポンプ14、および第3定量ポンプ16は、内接型ギヤポンプ、外接型ギヤポンプなどの単位時間あたりに一定の容積を吐出する定量ポンプであってもよい。
【0024】
上記第1混合器24および第2混合器32は、入力された2液の噴流を相互に衝突させることで瞬時に混合する衝突混合型混合器の一種である中心衝突型マイクロリアクターからそれぞれ同様に構成されている。第2混合器32に代表させて図2を用いて中心衝突型マイクロリアクターの構成を説明する。図2に示すように、第2混合器32は、第3接続管22および第4接続管26の一方および他方に連通する内周環状溝34および外周環状溝36が同心円状に形成された円形の入力側プレート38と、200乃至600μmφ程度の径を有する混合室40が中央部に形成され、その混合室40の外周側に放射状に設けられてその混合室40と内周環状溝34および外周環状溝36との間をそれぞれ連通させる100乃至200μm幅の複数本の短マイクロチャネル42および長マイクロチャネル44とが周方向において交互に形成された円形の中間プレート46と、その混合室40と連通する出力ポート48が中央部に貫通して形成された円形の出力側プレート50とが、密着して重ねられた状態で相互に固定されることにより構成されている。好適には、上記短マイクロチャネル42および長マイクロチャネル44は中心点を通る直線上に位置しており、短マイクロチャネル42の混合室40への開口と長マイクロチャネル44の混合室40への開口とが、対を成して相互に対向している。
【0025】
上記第2混合器32では、第3接続管22からのヒドラジン錯体を含む溶液がたとえば内周環状溝34を通して短マイクロチャネル42の外周端へ供給され、第4接続管26からアルカリ溶液がたとえば外周環状溝36を通して長マイクロチャネル44の外周端へ供給されると、ヒドラジン錯体を含む溶液が短マイクロチャネル42を通して混合室40へ噴射されると同時に、アルカリ溶液が長マイクロチャネル44を通して混合室40へ噴射される。混合室40内では、ヒドラジン錯体を含む溶液の噴流とアルカリ溶液の噴流とが相互に衝突することで無数の拡散、剪断、乱流が発生して瞬時に混合が行なわれ、アルカリ下で開始される還元により生成されたニッケルナノ粒子を含むコロイド溶液が出力ポート48を通して流出させられるようになっている。この2液の噴流の衝突による瞬時の混合は、還元により発生するニッケルナノ粒子の成長を開始させるが直ちにその成長を完了させる。
【0026】
以上のように構成されたニッケルナノ粒子製造用の反応装置すなわち混合装置10では、第1定量ポンプ12から第1の一定流量でたとえば50mMの塩化ニッケル溶液が吐出され、第2定量ポンプ14から第1の一定流量よりも大きく設定された第2の一定流量で塩化ニッケル溶液の濃度よりも高濃度たとえば1500mMのヒドラジン溶液が吐出されると、中心衝突型マイクロリアクターから構成された第1混合器24では、供給された塩化ニッケル溶液の噴流とヒドラジン溶液の噴流とが相互に衝突させられて混合室40内で瞬時に均一混合され、ヒドラジン錯体が生成される。この第1混合器24において塩化ニッケル溶液とヒドラジン溶液とを混合させてヒドラジン錯体を発生させる工程P1が、第1混合工程に対応している。
【0027】
次いで、上記ヒドラジン錯体を含む溶液が第3接続管22を通して第2混合器32へ供給され、第3定量ポンプ16から一定流量でたとえば60mMのアルカリ溶液が第2混合器32へ供給されると、中心衝突型マイクロリアクターから構成された第2混合器32では、供給されたヒドラジン錯体を含む溶液の噴流とアルカリ溶液の噴流とが相互に衝突させられて混合室40内で瞬時に均一混合され、ニッケルナノ粒子が均一に生成される。この第2混合器32において、ヒドラジン錯体を含む溶液とアルカリ溶液とを混合させて還元を開始させることでニッケルナノ粒子を発生させる工程が、第2混合工程P2に対応している。
【0028】
混合室40から吐出されたニッケルナノ粒子を含むコロイド溶液は、第5接続管28を通して出力槽30内に貯留される。出力槽30内に貯留されたニッケルコロイド溶液からは、遠心分離機を用いてニッケルナノ粒子を分離することができる。分離されたニッケルナノ粒子は、アセトンおよび蒸留水を用いて洗浄した後に乾燥することで、乾粉状態とされることができる。このようにして得られたニッケルナノ粒子は、5nm以下の平均粒径を有するシングルナノサイズであって、その粒度分布において優れた単分散性を示す。
【0029】
上述のように、本実施例の金属ナノ粒子の製造方法によれば、第1混合工程P1で得られたヒドラジン錯体を含む溶液と、アルカリ溶液とが、第2混合工程P2において、それらの噴射流を相互に衝突させることで瞬時に混合されることから、アルカリ下において開始される粒成長の時間が大幅に短縮されるので、シングルナノサイズで単分散性を有する優れた金属ナノ粒子が得られる。また、ヒドラジンを還元剤とする金属ナノ粒子の生成機構は、ヒドラジン錯体とアルカリとの間の配位子交換反応から放出されたヒドラジンによる水酸化物の還元であることから、金属塩溶液から直接に金属ナノ粒子を製造する方法と比較して、溶液中での還元剤濃度を低くすることができるので、得られた金属ナノ粒子はより少ない凝集性とより良い分散性を得ることができる。
【0030】
また、本実施例の金属ナノ粒子の製造方法によれば、第2混合工程P2は、図2に示す中心衝突型マイクロリアクターから構成される第2混合器32を用いて、第1混合工程P1で得られたヒドラジン錯体を含む溶液とアルカリ溶液とが、それらの噴射流を相互に衝突させることで瞬時に混合されることから、アルカリ下において開始される粒成長の時間が大幅に短縮されるので、シングルナノサイズで単分散性を有する優れた金属ナノ粒子が得られる。
【0031】
また、本実施例の金属ナノ粒子の製造方法によれば、前記金属塩溶液は、ニッケル、鉄、コバルト、銅のいずれかの金属イオンが溶解した溶液であってもよいので、このような酸化容易性を有するなどの比較的不安定な金属であっても、シングルナノサイズで単分散性を有する優れた金属ナノ粒子が得られる。
【0032】
また、本実施例の金属ナノ粒子の製造方法によれば、第1混合工程P1は、図2に示す中心衝突型マイクロリアクターから構成される第1混合器24を用いて金属塩溶液とヒドラジン溶液とを、それらの噴射流を相互に衝突させることで瞬時に混合することから、ヒドラジン錯体が生成されるときに核生成が短時間で均一に行なわれるので、その混合溶液を直ちにアルカリ下で還元反応させることによりシングルナノサイズで単分散性を有する優れた金属ナノ粒子が得られる。
【0033】
因みに、第1混合器24と第2混合器32との間の第3接続管22の流路長Lを1cm、3cm、20cm、40cmとした4種類の混合装置10において、それぞれ、150mMの塩化ニッケル溶液5ml/minと150mMの臭化ヘキサデシルトリメチルアンモニウム溶液5ml/minとの混合液を第1定量ポンプ12から一定流速10ml/minで吐出させ、1500mMのヒドラジン溶液を第2定量ポンプ14から一定流速10ml/minで吐出させ、60mMのナトリウム溶液を第3定量ポンプ16から一定流速10ml/minで吐出させる実験を、常温において行なった。この実験では、混合液中において、塩化ニッケルの濃度に比較して、ヒドラジンの濃度が十分に高くされており、具体的には20倍とされている。
【0034】
図3は上記の実験の結果を示している。図3において、平均粒径は、透過型電子顕微鏡写真TEM上に表わされたニッケルナノ粒子の大きさをスケールを用いて200個分計測した平均値Davである。また、変動係数CVは、上記スケールを用いて計測されたニッケルナノ粒子の大きさを示す分布の標準偏差σを上記平均粒径Davで除した値(割合)である。
【0035】
図3において、流路長Lが1cm、3cm、20cmである場合においては、図4、図5、図6に示す粒度分布に示されるように、平均粒径Davが4nm以下のシングルナノサイズであって、変動係数CVが0.21以下の単分散性に優れたニッケルナノ粒子が得られた。また、流路長Lが3cmであるときに得られたニッケルナノ粒子を示す図7の透過型電子顕微鏡写真TEMで代表されるように、大きなニッケルナノ粒子の混在のない均一なものであった。
【0036】
これに対して、流路長Lが40cmである場合においては、図8に示す粒度分布に示されるように、ニッケルナノ粒子は、平均粒径Davが4nmを超えるシングルナノサイズであって、変動係数CVが基準とする0.22を超える0.32であった。この場合の分布は、平均粒径Davの倍以上の10nmの粒子を含むブロードなものであって、均一なシングルナノサイズとは言い難いものであった。流路長Lが40cmである場合は、第3接続管22内でのヒドラジン錯体の滞留時間が2秒に対応していて、生成された核が滞留中に重合によって大きくなったものが含まれたためであると考えられる。従って、滞留時間は1.5秒すなわち第3接続管22の流路長Lは30cm以下が望ましい。
【実施例2】
【0037】
図9は、本発明方法が適用される他の形式の金属ナノ粒子製造用の反応装置すなわち混合装置60の構成を示している。この混合装置60は、前述の混合装置10と比較して、第1混合器25が中心衝突型マイクロリアクターから構成されておらず、Y字管から構成されている点で相違し、他は同様に構成されているので、同一の符号を付して説明を省略する。
【0038】
第1混合器25は、第1定量ポンプ12に第1接続管18を介して接続されるとともに第2定量ポンプ14に第2接続管20を介して接続され、第1定量ポンプ12から吐出された塩化ニッケル溶液と第2定量ポンプ14から吐出されたヒドラジン溶液とを混合した混合溶液を第3接続管22を通して第2混合器32へ出力する。第1混合器25は、Y字管から構成されていることから、中心衝突型マイクロリアクターから構成された第1混合器24に比較して、第1定量ポンプ12から吐出された塩化ニッケル溶液と第2定量ポンプ14から吐出されたヒドラジン溶液との混合に時間を要し、核生成させるための時間が必要とされる。このため、第1混合器25から第2混合器32への第3接続管22は、1秒(流路長Lが20cm)以上の搬送時間となるように、且つ、生成された核が重合して大きなニッケルナノ粒子が発生しないように1.5秒(流路長Lが30cm)以下の搬送時間となるように、その長さが決定されている。このように構成された混合装置60においても、前述の実施例の混合装置10と同様の効果が得られる。
【0039】
因みに、第1混合器25と第2混合器32との間の第3接続管22の流路長Lを10cm、20cm、40cmとした3種類の混合装置60において、それぞれ、150mMの塩化ニッケル溶液5ml/minと150mMの臭化ヘキサデシルトリメチルアンモニウム溶液5ml/minとの混合液を第1定量ポンプ12から一定流速10ml/minで吐出させ、1500mMのヒドラジン溶液を第2定量ポンプ14から一定流速10ml/minで吐出させ、60mMのナトリウム溶液を第3定量ポンプ16から一定流速10ml/minで吐出させる実験を、常温において行なった。この結果、流路長Lがを10cmである場合は、ニッケルナノ粒子は合成されなかった。第1混合器25における塩化ニッケル溶液とヒドラジン溶液との混合後の滞留時間が短いままアルカリ溶液と混合されたので、核生成ができなかったと推定される。、また、流路長Lがを30cmよりも長い40cmである場合は、大きな粒径のニッケルナノ粒子が混在して、単分散なニッケルナノ粒子を得ることができなかった。
【0040】
(比較例1)
第3接続管22の流路長Lが3cmである図1の混合装置10において、それぞれ、150mMの塩化ニッケル溶液5ml/minと150mMの臭化ヘキサデシルトリメチルアンモニウム溶液5ml/minとの混合液を第1定量ポンプ12から一定流速10ml/minで吐出させ、375mMのヒドラジン溶液を第2定量ポンプ14から一定流速10ml/minで吐出させ、60mMのナトリウム溶液を第3定量ポンプ16から一定流速10ml/minで吐出させる実験を、常温において行なった。すなわち、前述の図1の混合装置10における実験と比較して、第2定量ポンプ14から吐出されるヒドラジン溶液の濃度を1500mMから375mMへ減少させた他は同一の条件で実験を行なった。図10は、この実験の結果を示している。図11から明らかなように、平均粒径Davは4nmより大きい4.4nmであって、変動係数DVは、0.22より大きい0.24である分布のニッケルナノ粒子が得られた。ヒドラジン溶液の濃度が十分でないため、核生成およびそれに続く還元が不十分であるためと考えられる。
【0041】
(比較例2)
図11は、比較例2において用いられた金属ナノ粒子製造用の混合装置70の構成を示している。この混合装置70は、前述の混合装置10と比較して、第2混合器33が中心衝突型マイクロリアクターから構成されておらず、Y字管から構成されている点で相違し、他は同様に構成されているので、同一の符号を付して説明を省略する。
【0042】
第2混合器33は、第1混合器24に第3接続管22を介して接続されるとともに第3定量ポンプ16に第4接続管26を介して接続され、第1混合器24から吐出されたヒドラジン錯体を含む溶液と第3定量ポンプ16から吐出されたアルカリ溶液とを混合して混合溶液を第5接続管28を通して出力槽30へ出力する。第2混合器33は、Y字管から構成されていることから、中心衝突型マイクロリアクターから構成された第2混合器32に比較して、ヒドラジン錯体を含む溶液とアルカリ溶液との混合に時間を要する。
【0043】
上記混合装置70において、150mMの塩化ニッケル溶液5ml/minと150mMの臭化ヘキサデシルトリメチルアンモニウム溶液5ml/minとの混合液を第1定量ポンプ12から一定流速10ml/minで吐出させ、1500mMのヒドラジン溶液10mlを第2定量ポンプ14から一定流速10ml/minで吐出させ、60mMのナトリウム溶液を第3定量ポンプ16から一定流速10ml/minで吐出させる実験を、常温において行なった。図12は、この実験結果を示している。図12から明らかなように、平均粒径Davは4nmより小さい3.8nmであるが、変動係数DVは、0.22より大きい0.25である分布のニッケルナノ粒子が得られた。ヒドラジン錯体を含む溶液とアルカリ溶液との混合に時間を要するため、ニッケルナノ粒子の成長のばらつきが発生したものと考えられる。
【0044】
(比較例3)
図13は、本比較例3で用いた混合装置80を示している。この混合装置80は、150mMの塩化ニッケル溶液NiCl25ml/minと150mMのポリビニルアルコールPVA溶液5ml/minとの混合液を一定流速10ml/minで吐出する第1定量ポンプ82と、水素化ホウ素ナトリウム溶液NaBH4を一定流速10ml/minで吐出する第2定量ポンプ84と、それら塩化ニッケル溶液およびポリビニルアルコール溶液の混合液と水素化ホウ素ナトリウム溶液とを瞬時に混合する、中心衝突型マイクロリアクターから構成された混合器86とを、備えている。上記ポリビニルアルコールPVAは、保護剤として用いられ、水素化ホウ素ナトリウム溶液NaBH4は、還元剤として用いられており、シェル形成時に先立って加水分解によって容易に除去できる特徴がある。
【0045】
上記混合装置80を用いて得られたニッケルナノ粒子は、粒子形状が球形でないものが多く歪んでおり、50nm以上の粒径の巨大粒子が含まれていて、粒度分布がブロードであった。
【0046】
(比較例4)
水酸化ホウ素ナトリウム溶液NaBH4を還元剤として用いる比較例3において、保護材として用いるポリビニルアルコールPVA溶液5ml/minに替えて、臭化ヘキサデシルトリメチルアンモニウムCTAB溶液5ml/minを用いて、他は比較例3と同様の条件で混合装置80において混合した。この比較例4では、単分散なニッケルナノ粒子を得られなかった。このため、水酸化ホウ素ナトリウム溶液NaBH4を還元剤として用いる場合は、単分散なニッケルナノ粒子を得ることが困難であると推定される。
【0047】
以上、本発明の一実施例を図面に基づいて詳細に説明したが、これはあくまでも一実施形態であり、本発明は当業者の知識に基づいて種々の変更、改良を加えた態様で実施することができる。
【符号の説明】
【0048】
10、60:混合装置
12:第1定量ポンプ
14:第2定量ポンプ
16:第3定量ポンプ
24、25:第1混合器
32、33:第2混合器
【技術分野】
【0001】
本発明は、ナノメートルサイズで粒子分布の狭い単分散性を有する優れた金属ナノ粒子を連続的に製造可能な方法に関するものである。
【背景技術】
【0002】
特許文献1および特許文献2では、平行層流型マイクロリアクターを用いて単分散性を有する銀或いは白金の金属ナノ粒子を連続的に形成する方法が提案されている。この方法は、金属塩溶液を通す第1の流路と還元剤溶液を通る第2の流路とを形成し、それら金属塩溶液および還元剤溶液がそれぞれ薄い厚みの層状を成して流れる領域内の少なくとも一箇所において2溶液の接触界面を形成し、その接触界面を有する部分の2溶液の薄い層状の流れの厚さを、接触界面の法線方向で1〜500μmとし、その接触界面において金属イオンと還元剤とを相互に拡散且つ移動させ、金属イオンと還元剤とを相互に反応させることで、連続的に金属ナノ粒子を製造する。しかし、この方法では、酸化し難い安定な金属である銀、白金等の金属ナノ粒子の製造を対象としていて、ヒドラジンを還元剤とした液相法で金属ナノ粒子を製造する場合には反応時間が長くなり過ぎるので、ブロードな分布の金属ナノ粒子しか得られないという問題がある。
【0003】
これに対し、特許文献3では、金属として不安定なニッケルのナノ粒子を狭い粒子分布且つ優れた単分散性で得ることを目的とした製造方法が提案されている。この製造方法は、ニッケル前駆体、界面活性剤、疎水性溶媒を含む逆マイクロエマルジョン水溶液に、ヒドラジン水和物を添加して30分混合することでニッケル−ヒドラジン着物を形成し、そのニッケル−ヒドラジン着物を含む逆マイクロエマルジョンに還元剤(NaBH4)を添加して1時間混合することでニッケルナノ粒子を形成するものである。
【先行技術文献】
【特許文献】
【0004】
【特許文献1】特開2003−192344号公報
【特許文献2】特開2003−193119号公報
【特許文献3】特開2007−277709号公報
【発明の概要】
【発明が解決しようとする課題】
【0005】
しかしながら、上記特許文献3に記載のニッケルナノ粒子の製造方法では、100nm以下、好ましくは10乃至50nmの狭い粒度分布を有するニッケルナノ粒子が得られるとされているが、それは未だ大きな粒径に過ぎず、シングルナノサイズすなわち1桁のナノサイズで単分散性を有する金属ナノ粒子が得られないという、欠点があった。すなわち、攪拌機を備えた反応容器内に金属イオンを溶解した溶液にヒドラジン溶液を添加した後、アルカリを添加して還元反応させる、ヒドラジンを還元剤とした液相法で製造する金属ナノ粒子の製造方法では、いずれの攪拌方法を用いてもアルカリの添加によって還元が開始して核形成と粒成長とが同時に発生することから、20nm〜1μmサイズの金属粒子が生成され、シングルナノサイズで単分散性を有する金属ナノ粒子を得ることが困難であった。
【0006】
本発明は、以上の事情を背景として為されたものであって、その目的とするところは、シングルナノサイズで単分散性を有する金属ナノ粒子を連続的に製造可能な金属ナノ粒子の製造方法を提供することにある。
【課題を解決するための手段】
【0007】
すなわち、本発明者等は、以上の事情を背景として種々研究を重ねた結果、金属イオンを溶解した金属塩溶液にヒドラジン溶液を混合後、直ちにその混合液とアルカリの溶液とを瞬時に均一混合させることが、還元反応時間を可及的に短縮することにつながり、シングルナノサイズで単分散性を有する金属ナノ粒子を得るために有効であるという考え方に到達した。そして、それを実現するために中心衝突型マイクロリアクターを用いて、中央に位置する反応室に向かってその反応室に連通する複数のマイクロチャネル(噴射通路)を通して上記混合液とアルカリの溶液とを噴射し、相互に衝突させて瞬時に混合させると、従来では製造困難であったシングルナノサイズで単分散性を有する金属ナノ粒子が得られるという事実を見いだした。本発明はその知見に基づいて為されたものである。
【0008】
すなわち、本発明の要旨とするところは、(a)金属イオンを溶解した金属塩溶液にヒドラジン溶液を混合して得たヒドラジン錯体を、アルカリ溶液によって還元することにより金属ナノ粒子を製造する金属ナノ粒子の製造方法であって、(b)前記金属イオンを溶解した金属塩溶液に前記ヒドラジン溶液を混合して前記ヒドラジン錯体を生成する第1混合工程と、(c)第1混合工程で得られた前記ヒドラジン錯体を含む溶液の噴流とアルカリ溶液の噴流とを相互に衝突させることにより、該前記ヒドラジン錯体を含む溶液とアルカリ溶液とを混合して前記金属ナノ粒子を生成する第2混合工程とを、含むことにある。
【発明の効果】
【0009】
本発明の金属ナノ粒子の製造方法によれば、第1混合工程で得られた前記ヒドラジン錯体を含む溶液とアルカリ溶液とが、第2混合工程において、それらの噴射流を相互に衝突させることで瞬時に混合されることから、アルカリ下において開始される粒成長の時間が大幅に短縮されるので、シングルナノサイズで単分散性を有する優れた金属ナノ粒子が得られる。また、ヒドラジン溶液を還元剤とする金属ナノ粒子の生成機構は、ヒドラジン錯体とアルカリとの間の配位子交換反応から放出されたヒドラジンによる水酸化物の還元であることから、金属塩溶液から直接に金属ナノ粒子を製造する方法と比較して、溶液中での還元剤濃度を低くすることができるので、得られた金属ナノ粒子はより少ない凝集性とより良い分散性を得ることができる。
【0010】
ここで、好適には、前記第2混合工程は、中心衝突型マイクロリアクターを用いて前記第1混合工程で得られた前記ヒドラジン錯体を含む溶液とアルカリ溶液とを混合する。このようにすれば、第2混合工程で、前記ヒドラジン錯体を含む溶液とアルカリ溶液とが、中心衝突型マイクロリアクターにおいて、それらの噴射流を相互に衝突させることで瞬時に混合されることから、アルカリ下において開始される粒成長の時間が大幅に短縮されるので、シングルナノサイズで単分散性を有する優れた金属ナノ粒子が得られる。
【0011】
また、好適には、前記金属塩溶液は、ニッケル、鉄、コバルト、銅のいずれかの金属イオンが溶解した溶液である。このような、酸化容易性を有するなどの比較的不安定な金属であっても、シングルナノサイズで単分散性を有する優れた金属ナノ粒子が得られる。
【0012】
また、好適には、前記金属ナノ粒子は、5nm以下の平均粒径を有するものであるので、シングルナノサイズで単分散性を有する優れた金属ナノ粒子が得られる。
【0013】
また、好適には、前記第1混合工程は、中心衝突型マイクロリアクターを用いて前記金属塩溶液と前記ヒドラジン溶液とを混合する。このようにすれば、第1混合工程で、前記金属塩溶液とヒドラジン溶液とが、中心衝突型マイクロリアクターにおいて、それらの噴射流を相互に衝突させることで瞬時に混合されることから、ヒドラジン錯体が生成されるときに核生成が短時間で均一に行なわれるので、その混合溶液を直ちにアルカリ下で還元反応させることによりシングルナノサイズでたとえば変動係数が0.21以下の単分散性を有する優れた金属ナノ粒子が得られる。
【0014】
また、前記金属塩溶液としては、硝酸塩、硫酸塩、アンモニウム塩、炭酸塩、ハロゲン塩などの無機塩類の他、カルボン酸塩、水酸化物などが用いられる。この金属塩の濃度は、25mM程度が望ましく、2種類以上の金属塩を組み合わせることで、合金やコアシェル型のナノ粒子を製造することができる。コアシェル型のナノ粒子を製造する場合は、第2混合工程の後に、外皮を構成する金属イオンを溶解した金属塩溶液をさらに混合させる。
【0015】
また、前記ヒドラジン濃度は、金属塩溶液中の金属イオン濃度に対して20倍程度に高いことが望ましい。ヒドラジン濃度が金属イオン濃度よりも低いと核生成する金属が少なく、金属塩溶液中に残存する金属イオンが多くなって核生成とその後につづく粒成長とを分離できなくなり、結果として単分散な金属ナノ粒子を得ることができなくなる。反対に、ヒドラジン濃度が高すぎると核生成した金属が重合し過ぎて大きな粒径の金属粒子が含まれるようになる。
【0016】
また、前記アルカリ溶液としては、水酸化ナトリウム溶液が好適に用いられるが、リチウム、カリウム、ルビシウム、セシウムなどのアルカリ金属の水酸化物を水に溶解させたものであればよい。
【0017】
また、前記金属イオンを溶解した金属塩溶液とヒドラジン溶液とを混合して生成されたヒドラジン錯体をアルカリ溶液中で還元するまでの時間は、金属塩溶液とヒドラジン溶液とを均一に混合させてヒドラジン錯体を十分に生成させるまでの時間は必要であるが、可及的に短い時間であることが望ましい。前記第1混合工程において中心衝突型マイクロリアクターを用いて金属塩溶液とヒドラジン溶液とが混合される場合は、0.05秒乃至1.5秒の範囲内が望ましい。前記第1混合工程においてY字型コネクタを用いて金属塩溶液とヒドラジン溶液とが混合される場合は、1.0秒乃至1.5秒の範囲内が望ましい。
【0018】
また、前記金属塩溶液には、金属ナノ粒子を表面に吸着させる安定化剤(分散剤)を含有させることが望ましい。安定化剤により粒子表面を表面修飾した状態で溶媒中に分散することができ、安定な金属ナノ粒子含有分散液すなわちコロイド溶液が得られる。この場合の安定化剤の添加量は、コロイドの分散性を十分に高める程度でよく、特に制限はない。安定化剤としては、例えばヘキサデシルトリメチルアンモニウムブロマイドのようなアンモニウム塩、例えばドデシルベンゼンスルホン酸ナトリウムのようなスルホン酸塩、例えばペンタエチレングリコールドデシルエーテルのようなエーテル類、ポリビニルビロリドンなどが、好適に用いられる。
【0019】
また、第1混合工程および第2混合工程、特に第2混合工程における混合操作は、分子拡散、乱流混合或いは層流混合に分類される。分子拡散は、Fickの法則に支配され、混合時間をt、拡散距離をd、拡散定数をDとすると、t=d2/Dにより表わされるので、拡散距離dを短くすることで効果的に拡散時間tを短縮できる。この拡散距離dを短くしたマイクロ流路での混合では、分子拡散か層流拡散にならざるを得ないが、層流の厚みを小さくすることに限界がある。このため、第1混合工程および第2混合工程、特に第2混合工程では、噴射型混合器の一種である中心衝突型マイクロリアクターすなわち中心衝突型マイクロミキサーが好適に用いられる。この中心衝突型マイクロリアクターでは、200〜600μmφの混合室と、100〜200μmの幅寸法を有してその混合室の周囲からその混合室に連通する径方向の少なくとも1対のマイクロ流路とが放射状に設けられ、そのマイクロ流路を通してヒドラジン錯体を含む溶液とアルカリ溶液とを噴射することで、両液が混合室内で衝突して乱流が発生させられ、瞬時に均一混合されるようになっている。
【図面の簡単な説明】
【0020】
【図1】本発明方法を実施するための第1実施例の混合装置の構成を模式的に示す図である。
【図2】図1の中心衝突型マイクロリアクターの構成を、一部を切り欠いて説明する正面図である。
【図3】図1の混合装置において第1混合器から吐出されたヒドラジン錯体を含む溶液の流路長すなわちヒドラジン錯体の滞留長を変化させてニッケルナノ粒子を生成したときに、得られたニッケルナノ粒子の平均粒径および変動係数を示す図表である。
【図4】図3の混合装置を用いて、ヒドラジン錯体の滞留長が1cmである場合に得られたニッケルナノ粒子の粒度分布を示す図である。
【図5】図3の混合装置を用いて、ヒドラジン錯体の滞留長が3cmである場合に得られたニッケルナノ粒子の粒度分布を示す図である。
【図6】図3の混合装置を用いて、ヒドラジン錯体の滞留長が20cmである場合に得られたニッケルナノ粒子の粒度分布を示す図である。
【図7】図3の混合装置を用いて、ヒドラジン錯体の滞留長が3cmである場合に得られたニッケルナノ粒子を透過型電子顕微鏡TEMで観察したときの写真を示す図である。
【図8】図3の混合装置を用いて、ヒドラジン錯体の滞留長が40cmである場合に得られたニッケルナノ粒子の粒度分布を示す図である。
【図9】本発明の第2実施例の混合装置を模式的に示す図であって、図1に相当する図である。
【図10】図1の混合装置を用いてヒドラジン濃度を低くしてニッケルナノ粒子を生成した比較例1において、得られたニッケルナノ粒子の粒度分布を示す図である。
【図11】比較例2の混合装置の構成を模式的に示す図である。
【図12】図11の比較例2の混合装置を用いて得られたニッケルナノ粒子の粒度分布を示す図である。
【図13】比較例3の混合装置の構成を模式的に示す図である。
【発明を実施するための形態】
【0021】
以下、本発明の一適用例を図面を参照して詳細に説明する。なお、以下の実施例において装置を説明する図は適宜簡略化された模式図であって、各部の寸法比および形状等は必ずしも正確に描かれていない。
【実施例1】
【0022】
図1は、本発明方法が適用される一例の、金属ナノ粒子製造用の反応装置すなわち混合装置10の構成を説明する図である。図1において、混合装置10は、一定濃度の金属塩溶液たとえば塩化ニッケル溶液(NiCl2)と安定化剤溶液(CTAB)溶液との混合液を一定流量で吐出する第1定量ポンプ12と、塩化ニッケル溶液よりも大きく設定された一定流量で且つ塩化ニッケル溶液の濃度よりも高く設定された一定濃度のヒドラジン溶液(N2H4)を吐出する第2定量ポンプ14と、一定流量でアルカリ溶液(NaOH)を吐出する第3定量ポンプ16と、第1定量ポンプ12に第1接続管18を介して接続されるとともに第2定量ポンプ14に第2接続管20を介して接続され、第1定量ポンプ12から吐出された塩化ニッケル溶液と第2定量ポンプ14から吐出されたヒドラジン溶液とを瞬時に混合して混合溶液を第3接続管22を通して出力する第1混合器24と、第3接続管22を介して第1混合器24と接続され且つ第4接続管26を介して第3定量ポンプ16と接続され、第1混合器24から出力されたヒドラジン錯体を含む溶液と第3定量ポンプ16から吐出されたアルカリ溶液とを瞬時に混合して反応生成されたニッケルナノ粒子を含むコロイド溶液を第5接続管28を通して出力槽30へ出力してそれに貯留させる第2混合器32とを備えている。上記CTABは、安定化剤或いは界面活性剤として機能する臭化ヘキサデシルトリメチルアンモニウムである。
【0023】
上記第1定量ポンプ12、第2定量ポンプ14、および第3定量ポンプ16は、溶液が収容されたシリンダCLとそのシリンダCLに摺動可能に嵌合されてシリンダCL内の溶液を押し出すピストンPと、そのピストンPを一定速度で駆動する図示しない駆動装置とを備え、単位時間あたりに一定の容積を吐出するシリンダ型定量ポンプにより構成されている。しかし、上記第1定量ポンプ12、第2定量ポンプ14、および第3定量ポンプ16は、内接型ギヤポンプ、外接型ギヤポンプなどの単位時間あたりに一定の容積を吐出する定量ポンプであってもよい。
【0024】
上記第1混合器24および第2混合器32は、入力された2液の噴流を相互に衝突させることで瞬時に混合する衝突混合型混合器の一種である中心衝突型マイクロリアクターからそれぞれ同様に構成されている。第2混合器32に代表させて図2を用いて中心衝突型マイクロリアクターの構成を説明する。図2に示すように、第2混合器32は、第3接続管22および第4接続管26の一方および他方に連通する内周環状溝34および外周環状溝36が同心円状に形成された円形の入力側プレート38と、200乃至600μmφ程度の径を有する混合室40が中央部に形成され、その混合室40の外周側に放射状に設けられてその混合室40と内周環状溝34および外周環状溝36との間をそれぞれ連通させる100乃至200μm幅の複数本の短マイクロチャネル42および長マイクロチャネル44とが周方向において交互に形成された円形の中間プレート46と、その混合室40と連通する出力ポート48が中央部に貫通して形成された円形の出力側プレート50とが、密着して重ねられた状態で相互に固定されることにより構成されている。好適には、上記短マイクロチャネル42および長マイクロチャネル44は中心点を通る直線上に位置しており、短マイクロチャネル42の混合室40への開口と長マイクロチャネル44の混合室40への開口とが、対を成して相互に対向している。
【0025】
上記第2混合器32では、第3接続管22からのヒドラジン錯体を含む溶液がたとえば内周環状溝34を通して短マイクロチャネル42の外周端へ供給され、第4接続管26からアルカリ溶液がたとえば外周環状溝36を通して長マイクロチャネル44の外周端へ供給されると、ヒドラジン錯体を含む溶液が短マイクロチャネル42を通して混合室40へ噴射されると同時に、アルカリ溶液が長マイクロチャネル44を通して混合室40へ噴射される。混合室40内では、ヒドラジン錯体を含む溶液の噴流とアルカリ溶液の噴流とが相互に衝突することで無数の拡散、剪断、乱流が発生して瞬時に混合が行なわれ、アルカリ下で開始される還元により生成されたニッケルナノ粒子を含むコロイド溶液が出力ポート48を通して流出させられるようになっている。この2液の噴流の衝突による瞬時の混合は、還元により発生するニッケルナノ粒子の成長を開始させるが直ちにその成長を完了させる。
【0026】
以上のように構成されたニッケルナノ粒子製造用の反応装置すなわち混合装置10では、第1定量ポンプ12から第1の一定流量でたとえば50mMの塩化ニッケル溶液が吐出され、第2定量ポンプ14から第1の一定流量よりも大きく設定された第2の一定流量で塩化ニッケル溶液の濃度よりも高濃度たとえば1500mMのヒドラジン溶液が吐出されると、中心衝突型マイクロリアクターから構成された第1混合器24では、供給された塩化ニッケル溶液の噴流とヒドラジン溶液の噴流とが相互に衝突させられて混合室40内で瞬時に均一混合され、ヒドラジン錯体が生成される。この第1混合器24において塩化ニッケル溶液とヒドラジン溶液とを混合させてヒドラジン錯体を発生させる工程P1が、第1混合工程に対応している。
【0027】
次いで、上記ヒドラジン錯体を含む溶液が第3接続管22を通して第2混合器32へ供給され、第3定量ポンプ16から一定流量でたとえば60mMのアルカリ溶液が第2混合器32へ供給されると、中心衝突型マイクロリアクターから構成された第2混合器32では、供給されたヒドラジン錯体を含む溶液の噴流とアルカリ溶液の噴流とが相互に衝突させられて混合室40内で瞬時に均一混合され、ニッケルナノ粒子が均一に生成される。この第2混合器32において、ヒドラジン錯体を含む溶液とアルカリ溶液とを混合させて還元を開始させることでニッケルナノ粒子を発生させる工程が、第2混合工程P2に対応している。
【0028】
混合室40から吐出されたニッケルナノ粒子を含むコロイド溶液は、第5接続管28を通して出力槽30内に貯留される。出力槽30内に貯留されたニッケルコロイド溶液からは、遠心分離機を用いてニッケルナノ粒子を分離することができる。分離されたニッケルナノ粒子は、アセトンおよび蒸留水を用いて洗浄した後に乾燥することで、乾粉状態とされることができる。このようにして得られたニッケルナノ粒子は、5nm以下の平均粒径を有するシングルナノサイズであって、その粒度分布において優れた単分散性を示す。
【0029】
上述のように、本実施例の金属ナノ粒子の製造方法によれば、第1混合工程P1で得られたヒドラジン錯体を含む溶液と、アルカリ溶液とが、第2混合工程P2において、それらの噴射流を相互に衝突させることで瞬時に混合されることから、アルカリ下において開始される粒成長の時間が大幅に短縮されるので、シングルナノサイズで単分散性を有する優れた金属ナノ粒子が得られる。また、ヒドラジンを還元剤とする金属ナノ粒子の生成機構は、ヒドラジン錯体とアルカリとの間の配位子交換反応から放出されたヒドラジンによる水酸化物の還元であることから、金属塩溶液から直接に金属ナノ粒子を製造する方法と比較して、溶液中での還元剤濃度を低くすることができるので、得られた金属ナノ粒子はより少ない凝集性とより良い分散性を得ることができる。
【0030】
また、本実施例の金属ナノ粒子の製造方法によれば、第2混合工程P2は、図2に示す中心衝突型マイクロリアクターから構成される第2混合器32を用いて、第1混合工程P1で得られたヒドラジン錯体を含む溶液とアルカリ溶液とが、それらの噴射流を相互に衝突させることで瞬時に混合されることから、アルカリ下において開始される粒成長の時間が大幅に短縮されるので、シングルナノサイズで単分散性を有する優れた金属ナノ粒子が得られる。
【0031】
また、本実施例の金属ナノ粒子の製造方法によれば、前記金属塩溶液は、ニッケル、鉄、コバルト、銅のいずれかの金属イオンが溶解した溶液であってもよいので、このような酸化容易性を有するなどの比較的不安定な金属であっても、シングルナノサイズで単分散性を有する優れた金属ナノ粒子が得られる。
【0032】
また、本実施例の金属ナノ粒子の製造方法によれば、第1混合工程P1は、図2に示す中心衝突型マイクロリアクターから構成される第1混合器24を用いて金属塩溶液とヒドラジン溶液とを、それらの噴射流を相互に衝突させることで瞬時に混合することから、ヒドラジン錯体が生成されるときに核生成が短時間で均一に行なわれるので、その混合溶液を直ちにアルカリ下で還元反応させることによりシングルナノサイズで単分散性を有する優れた金属ナノ粒子が得られる。
【0033】
因みに、第1混合器24と第2混合器32との間の第3接続管22の流路長Lを1cm、3cm、20cm、40cmとした4種類の混合装置10において、それぞれ、150mMの塩化ニッケル溶液5ml/minと150mMの臭化ヘキサデシルトリメチルアンモニウム溶液5ml/minとの混合液を第1定量ポンプ12から一定流速10ml/minで吐出させ、1500mMのヒドラジン溶液を第2定量ポンプ14から一定流速10ml/minで吐出させ、60mMのナトリウム溶液を第3定量ポンプ16から一定流速10ml/minで吐出させる実験を、常温において行なった。この実験では、混合液中において、塩化ニッケルの濃度に比較して、ヒドラジンの濃度が十分に高くされており、具体的には20倍とされている。
【0034】
図3は上記の実験の結果を示している。図3において、平均粒径は、透過型電子顕微鏡写真TEM上に表わされたニッケルナノ粒子の大きさをスケールを用いて200個分計測した平均値Davである。また、変動係数CVは、上記スケールを用いて計測されたニッケルナノ粒子の大きさを示す分布の標準偏差σを上記平均粒径Davで除した値(割合)である。
【0035】
図3において、流路長Lが1cm、3cm、20cmである場合においては、図4、図5、図6に示す粒度分布に示されるように、平均粒径Davが4nm以下のシングルナノサイズであって、変動係数CVが0.21以下の単分散性に優れたニッケルナノ粒子が得られた。また、流路長Lが3cmであるときに得られたニッケルナノ粒子を示す図7の透過型電子顕微鏡写真TEMで代表されるように、大きなニッケルナノ粒子の混在のない均一なものであった。
【0036】
これに対して、流路長Lが40cmである場合においては、図8に示す粒度分布に示されるように、ニッケルナノ粒子は、平均粒径Davが4nmを超えるシングルナノサイズであって、変動係数CVが基準とする0.22を超える0.32であった。この場合の分布は、平均粒径Davの倍以上の10nmの粒子を含むブロードなものであって、均一なシングルナノサイズとは言い難いものであった。流路長Lが40cmである場合は、第3接続管22内でのヒドラジン錯体の滞留時間が2秒に対応していて、生成された核が滞留中に重合によって大きくなったものが含まれたためであると考えられる。従って、滞留時間は1.5秒すなわち第3接続管22の流路長Lは30cm以下が望ましい。
【実施例2】
【0037】
図9は、本発明方法が適用される他の形式の金属ナノ粒子製造用の反応装置すなわち混合装置60の構成を示している。この混合装置60は、前述の混合装置10と比較して、第1混合器25が中心衝突型マイクロリアクターから構成されておらず、Y字管から構成されている点で相違し、他は同様に構成されているので、同一の符号を付して説明を省略する。
【0038】
第1混合器25は、第1定量ポンプ12に第1接続管18を介して接続されるとともに第2定量ポンプ14に第2接続管20を介して接続され、第1定量ポンプ12から吐出された塩化ニッケル溶液と第2定量ポンプ14から吐出されたヒドラジン溶液とを混合した混合溶液を第3接続管22を通して第2混合器32へ出力する。第1混合器25は、Y字管から構成されていることから、中心衝突型マイクロリアクターから構成された第1混合器24に比較して、第1定量ポンプ12から吐出された塩化ニッケル溶液と第2定量ポンプ14から吐出されたヒドラジン溶液との混合に時間を要し、核生成させるための時間が必要とされる。このため、第1混合器25から第2混合器32への第3接続管22は、1秒(流路長Lが20cm)以上の搬送時間となるように、且つ、生成された核が重合して大きなニッケルナノ粒子が発生しないように1.5秒(流路長Lが30cm)以下の搬送時間となるように、その長さが決定されている。このように構成された混合装置60においても、前述の実施例の混合装置10と同様の効果が得られる。
【0039】
因みに、第1混合器25と第2混合器32との間の第3接続管22の流路長Lを10cm、20cm、40cmとした3種類の混合装置60において、それぞれ、150mMの塩化ニッケル溶液5ml/minと150mMの臭化ヘキサデシルトリメチルアンモニウム溶液5ml/minとの混合液を第1定量ポンプ12から一定流速10ml/minで吐出させ、1500mMのヒドラジン溶液を第2定量ポンプ14から一定流速10ml/minで吐出させ、60mMのナトリウム溶液を第3定量ポンプ16から一定流速10ml/minで吐出させる実験を、常温において行なった。この結果、流路長Lがを10cmである場合は、ニッケルナノ粒子は合成されなかった。第1混合器25における塩化ニッケル溶液とヒドラジン溶液との混合後の滞留時間が短いままアルカリ溶液と混合されたので、核生成ができなかったと推定される。、また、流路長Lがを30cmよりも長い40cmである場合は、大きな粒径のニッケルナノ粒子が混在して、単分散なニッケルナノ粒子を得ることができなかった。
【0040】
(比較例1)
第3接続管22の流路長Lが3cmである図1の混合装置10において、それぞれ、150mMの塩化ニッケル溶液5ml/minと150mMの臭化ヘキサデシルトリメチルアンモニウム溶液5ml/minとの混合液を第1定量ポンプ12から一定流速10ml/minで吐出させ、375mMのヒドラジン溶液を第2定量ポンプ14から一定流速10ml/minで吐出させ、60mMのナトリウム溶液を第3定量ポンプ16から一定流速10ml/minで吐出させる実験を、常温において行なった。すなわち、前述の図1の混合装置10における実験と比較して、第2定量ポンプ14から吐出されるヒドラジン溶液の濃度を1500mMから375mMへ減少させた他は同一の条件で実験を行なった。図10は、この実験の結果を示している。図11から明らかなように、平均粒径Davは4nmより大きい4.4nmであって、変動係数DVは、0.22より大きい0.24である分布のニッケルナノ粒子が得られた。ヒドラジン溶液の濃度が十分でないため、核生成およびそれに続く還元が不十分であるためと考えられる。
【0041】
(比較例2)
図11は、比較例2において用いられた金属ナノ粒子製造用の混合装置70の構成を示している。この混合装置70は、前述の混合装置10と比較して、第2混合器33が中心衝突型マイクロリアクターから構成されておらず、Y字管から構成されている点で相違し、他は同様に構成されているので、同一の符号を付して説明を省略する。
【0042】
第2混合器33は、第1混合器24に第3接続管22を介して接続されるとともに第3定量ポンプ16に第4接続管26を介して接続され、第1混合器24から吐出されたヒドラジン錯体を含む溶液と第3定量ポンプ16から吐出されたアルカリ溶液とを混合して混合溶液を第5接続管28を通して出力槽30へ出力する。第2混合器33は、Y字管から構成されていることから、中心衝突型マイクロリアクターから構成された第2混合器32に比較して、ヒドラジン錯体を含む溶液とアルカリ溶液との混合に時間を要する。
【0043】
上記混合装置70において、150mMの塩化ニッケル溶液5ml/minと150mMの臭化ヘキサデシルトリメチルアンモニウム溶液5ml/minとの混合液を第1定量ポンプ12から一定流速10ml/minで吐出させ、1500mMのヒドラジン溶液10mlを第2定量ポンプ14から一定流速10ml/minで吐出させ、60mMのナトリウム溶液を第3定量ポンプ16から一定流速10ml/minで吐出させる実験を、常温において行なった。図12は、この実験結果を示している。図12から明らかなように、平均粒径Davは4nmより小さい3.8nmであるが、変動係数DVは、0.22より大きい0.25である分布のニッケルナノ粒子が得られた。ヒドラジン錯体を含む溶液とアルカリ溶液との混合に時間を要するため、ニッケルナノ粒子の成長のばらつきが発生したものと考えられる。
【0044】
(比較例3)
図13は、本比較例3で用いた混合装置80を示している。この混合装置80は、150mMの塩化ニッケル溶液NiCl25ml/minと150mMのポリビニルアルコールPVA溶液5ml/minとの混合液を一定流速10ml/minで吐出する第1定量ポンプ82と、水素化ホウ素ナトリウム溶液NaBH4を一定流速10ml/minで吐出する第2定量ポンプ84と、それら塩化ニッケル溶液およびポリビニルアルコール溶液の混合液と水素化ホウ素ナトリウム溶液とを瞬時に混合する、中心衝突型マイクロリアクターから構成された混合器86とを、備えている。上記ポリビニルアルコールPVAは、保護剤として用いられ、水素化ホウ素ナトリウム溶液NaBH4は、還元剤として用いられており、シェル形成時に先立って加水分解によって容易に除去できる特徴がある。
【0045】
上記混合装置80を用いて得られたニッケルナノ粒子は、粒子形状が球形でないものが多く歪んでおり、50nm以上の粒径の巨大粒子が含まれていて、粒度分布がブロードであった。
【0046】
(比較例4)
水酸化ホウ素ナトリウム溶液NaBH4を還元剤として用いる比較例3において、保護材として用いるポリビニルアルコールPVA溶液5ml/minに替えて、臭化ヘキサデシルトリメチルアンモニウムCTAB溶液5ml/minを用いて、他は比較例3と同様の条件で混合装置80において混合した。この比較例4では、単分散なニッケルナノ粒子を得られなかった。このため、水酸化ホウ素ナトリウム溶液NaBH4を還元剤として用いる場合は、単分散なニッケルナノ粒子を得ることが困難であると推定される。
【0047】
以上、本発明の一実施例を図面に基づいて詳細に説明したが、これはあくまでも一実施形態であり、本発明は当業者の知識に基づいて種々の変更、改良を加えた態様で実施することができる。
【符号の説明】
【0048】
10、60:混合装置
12:第1定量ポンプ
14:第2定量ポンプ
16:第3定量ポンプ
24、25:第1混合器
32、33:第2混合器
【特許請求の範囲】
【請求項1】
金属イオンを溶解した金属塩溶液にヒドラジン溶液を混合して得たヒドラジン錯体を、アルカリ溶液によって還元することにより金属ナノ粒子を製造する金属ナノ粒子の製造方法であって、
前記金属イオンを溶解した金属塩溶液に前記ヒドラジン溶液を混合して前記ヒドラジン錯体を生成する第1混合工程と、
該第1混合工程で得られた前記ヒドラジン錯体を含む溶液の噴流とアルカリ溶液の噴流とを相互に衝突させることにより、該ヒドラジン錯体を含む溶液と該アルカリ溶液とを混合して前記金属ナノ粒子を生成する第2混合工程と
を、含むことを特徴とする金属ナノ粒子の製造方法。
【請求項2】
前記第2混合工程は、中心衝突型マイクロリアクターを用いて前記第1混合工程で得られた前記ヒドラジン錯体を含む溶液とアルカリ溶液とを混合することを特徴とする請求項1の金属ナノ粒子の製造方法。
【請求項3】
前記金属塩溶液は、ニッケル、鉄、コバルト、銅のいずれかの金属イオンが溶解した溶液であることを特徴とする請求項1または2の金属ナノ粒子の製造方法。
【請求項4】
前記金属ナノ粒子は、5nm以下の平均粒径を有するものであることを特徴とする請求項1乃至3のいずれか1の金属ナノ粒子の製造方法。
【請求項5】
前記第1混合工程は、中心衝突型マイクロリアクターを用いて前記金属塩溶液とヒドラジン溶液とを混合することを特徴とする請求項1乃至4のいずれか1の金属ナノ粒子の製造方法。
【請求項1】
金属イオンを溶解した金属塩溶液にヒドラジン溶液を混合して得たヒドラジン錯体を、アルカリ溶液によって還元することにより金属ナノ粒子を製造する金属ナノ粒子の製造方法であって、
前記金属イオンを溶解した金属塩溶液に前記ヒドラジン溶液を混合して前記ヒドラジン錯体を生成する第1混合工程と、
該第1混合工程で得られた前記ヒドラジン錯体を含む溶液の噴流とアルカリ溶液の噴流とを相互に衝突させることにより、該ヒドラジン錯体を含む溶液と該アルカリ溶液とを混合して前記金属ナノ粒子を生成する第2混合工程と
を、含むことを特徴とする金属ナノ粒子の製造方法。
【請求項2】
前記第2混合工程は、中心衝突型マイクロリアクターを用いて前記第1混合工程で得られた前記ヒドラジン錯体を含む溶液とアルカリ溶液とを混合することを特徴とする請求項1の金属ナノ粒子の製造方法。
【請求項3】
前記金属塩溶液は、ニッケル、鉄、コバルト、銅のいずれかの金属イオンが溶解した溶液であることを特徴とする請求項1または2の金属ナノ粒子の製造方法。
【請求項4】
前記金属ナノ粒子は、5nm以下の平均粒径を有するものであることを特徴とする請求項1乃至3のいずれか1の金属ナノ粒子の製造方法。
【請求項5】
前記第1混合工程は、中心衝突型マイクロリアクターを用いて前記金属塩溶液とヒドラジン溶液とを混合することを特徴とする請求項1乃至4のいずれか1の金属ナノ粒子の製造方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図7】




【図2】


【図3】


【図4】


【図5】


【図6】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図7】


【公開番号】特開2013−108121(P2013−108121A)
【公開日】平成25年6月6日(2013.6.6)
【国際特許分類】
【出願番号】特願2011−252700(P2011−252700)
【出願日】平成23年11月18日(2011.11.18)
【出願人】(000004293)株式会社ノリタケカンパニーリミテド (449)
【出願人】(504132272)国立大学法人京都大学 (1,269)
【Fターム(参考)】
【公開日】平成25年6月6日(2013.6.6)
【国際特許分類】
【出願日】平成23年11月18日(2011.11.18)
【出願人】(000004293)株式会社ノリタケカンパニーリミテド (449)
【出願人】(504132272)国立大学法人京都大学 (1,269)
【Fターム(参考)】
[ Back to top ]

