Fターム[4H045AA10]の内容
Fターム[4H045AA10]の下位に属するFターム
抗原、抗体 (7,339)
Fターム[4H045AA10]に分類される特許
1 - 20 / 9,138
胃腸障害の治療のための方法および組成物
エリスロポエチンの製造方法およびエリスロポエチン産生細胞の単離方法
血圧降下剤
HODEに対する特異的抗体、酸化ストレスに起因する疾患の診断方法、キット、ハイブリドーマおよび免疫学的検出方法
活性リンフォトキシン−βレセプター免疫グロブリンキメラタンパク質の高レベルの発現およびそれらの精製のための方法
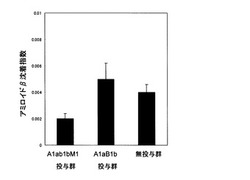
アルツハイマー病の予防および/または治療用ワクチン組成物
【課題】アルツハイマー病の予防および/または治療のためのワクチン組成物を提供すること。
【解決手段】アミロイドβペプチドのN末端部分に由来する5〜15個の連続したアミノ酸配列が、単一もしくは複数個反復して、種子貯蔵タンパクのアミノ酸配列中に挿入されたアミノ酸配列を有する融合タンパク質を含む、アルツハイマー病を予防および/または治療するためのワクチン組成物。
(もっと読む)
安定性が向上したFc結合性タンパク質
【課題】 医薬品、臨床検査薬、バイオセンサー、アフィニティーリガンド(分離剤)などの用途に使用可能なFc結合性タンパク質の、化学修飾による安定化方法を提供すること。
【解決手段】 Fc結合性タンパク質を化学修飾して負電荷を有する解離基を導入することで、アルカリ環境下における安定性が向上したFc結合性タンパク質を提供する。
(もっと読む)
新規重合体およびその製造方法
【課題】本発明は、良好な操作性と高い安全性を有する、優れた生体材料を提供することを課題とする。
【解決手段】下記式(1)で表されるペプチドユニットと多糖類由来の糖残基とを有する重合体。
−(Pro−Y−Gly)n− (1)
(式中、YはPro又はHypを表し、nは1以上の整数である。)
本発明によれば、コラーゲン様ポリペプチドの生体材料に適した種々の特徴と多糖類の高い親水性や酵素により分解されるという特徴とを併せ持つうえ、機械的強度が高く、吸水性を有する、安全な新規重合体が提供される。さらには、縮合反応において前記ペプチドオリゴマーと多糖類の仕込み量を変化させることにより、得られる重合体の吸水性や酵素分解性を制御できる。
(もっと読む)
グルコース親和性タンパク質の精製方法
【課題】試料から、グルコース親和性タンパク質を選択的に精製する方法を提供する。
【解決手段】吸着剤としてパラハイドロキシアセトフェノンを含むアフィニティカラムに、グルコース親和性タンパク質を含む試料を適用し、上記パラハイドロキシアセトフェノンに、上記グルコース親和性タンパク質を結合させる第1ステップと、グルコースを含む第1溶液により、上記アフィニティカラムに結合した上記グルコース親和性タンパク質の少なくとも一部を分離させ、少なくとも上記グルコースと上記グルコース親和性タンパク質とを含む第2溶液を得る第2ステップと、上記第2溶液から、上記グルコース親和性タンパク質の少なくとも一部を分離させる第3ステップと、を含む。
(もっと読む)
アルツハイマー病に関連する遺伝子配列およびタンパク質、ならびにその使用
【課題】アルツハイマー病に関連する遺伝子配列およびタンパク質、ならびにその使用を提供すること。
【解決手段】本発明は、2つのヒトプレセニリン遺伝子PS-1およびPS-2の同定、単離、配列決定、および特徴付けを記載する。これらの遺伝子の変異は、家族性アルツハイマー病をもたらす。マウス、C.elegans、およびD.melanogasterにおけるプレセニリン遺伝子ホ
モログもまた同定される。プレセニリンを含むかまたはそれに由来する核酸およびタンパク質は、アルツハイマー病のスクリーニングおよび診断、アルツハイマー病の処置のための治療剤の同定および開発、およびアルツハイマー病のモデルとして有用な細胞株およびトランスジェニック動物の産生に有用である。
(もっと読む)
ナノ粒子を利用した遺伝子発現調節法
【課題】効率のよく細胞ないし生体を近赤外光を用いて加熱すること。
【解決手段】カーボンナノホーン(CNH)に血清アルブミンが結合した複合体。
(もっと読む)
新規な非天然型アミノ酸、及びその利用
【課題】光クロスリンク能を持つ新規な非天然型アミノ酸、及びその利用を提供する。
【解決手段】本発明に係る化合物は、式(1)で示されるものである。
【化1】
(nは1以上で3以下の整数を表し、R1、R2、R3及びR4は、水素原子、ハロゲン原子、置換基を有しうる炭素数1〜3の炭化水素基、置換基を有しうるアジドメチル基、又はアセチル基を表し、R5は、置換基を有しうる炭素数1〜3のアルキル基、置換基を有しうるアジドメチル基、又は水素原子を表す)
(もっと読む)
免疫抑制剤として使用するためのデプシペプチドおよびその同族体
【課題】低い細胞障害特性および管理可能な副作用を伴う代替の免疫抑制剤を提供すること。
【解決手段】構造(I)を有するデプシペプチドおよびその同族体が開示される。ここで、m、n、p、q、X、R1、R2およびR3は本明細書中に定義されるとおりである。FR901228を含むこれらの化合物は、例えば、免疫抑制剤としての活性、ならびに、炎症、自己免疫もしくは免疫系関連疾患(移植片対宿主病を含む)を罹患もしくは罹患する危険性がある患者の予防または処置するための活性、ならびに、移植後の移植片/組織の生存を高めるための活性を有する。また、リンパ球の活性化、増殖を阻害するため、および/またはIL−2分泌を抑制するための方法が提供される。 (もっと読む)
(もっと読む)
キスペプチン拮抗薬及びその使用
【課題】本発明は、個体におけるキスペプチン活性により誘発され、かつ/または悪化した状態の治療用の薬剤の製造におけるキスペプチンの拮抗薬の使用に関する。本発明はまた、個体におけるキスペプチン活性により誘発され、かつ/または悪化した状態の治療において有用である、キスペプチンの拮抗薬として作用する可能性がある、定義された特定のペプチド分子を提供する。さらに、本発明は、キスペプチンの拮抗薬および/または定義されたペプチドを同定し、かつ/または使用する方法、ならびにその医薬組成物を提供する。
【解決手段】個体におけるキスペプチン活性により誘発され、かつ/または悪化した状態の治療用の薬剤の製造におけるキスペプチンの拮抗薬の使用。
(もっと読む)
改変タンパク質
【課題】グリコシルトランスフェラーゼによりペプチドおよびタンパク質を結合させる方法を提供する。
【解決手段】治療用タンパク質の便利な合成または半合成を可能にする手段および方法であって、改変の導入が上記の問題に対処している手段および方法。可溶性糖タンパク質誘導体の循環半減期を延長して、治療または予防のための循環する糖タンパク質の治療的有効レベルを維持するために必要な、注射剤の量および注射の頻度を減少させる方法。一定の治療的に活性な糖タンパク質の短いインビボ血漿半減期は、治療または予防に必要とされる可溶性タンパク質の頻度および量に起因して望ましくないものである。糖タンパク質構造を効果的に変化させ、また生物学的活性を実質的に維持して、このような糖タンパク質の循環半減期を延長するための手段。
(もっと読む)
コラーゲンペプチドの製造方法
【課題】本発明はコラーゲン臭などの不快臭がなく、不快味が残らないコラーゲンペプチド及びその製造方法を提供する。
【解決手段】本発明は、コラーゲンを酵素処理した後、得られた粗コラーゲンペプチド液に除臭剤を粗コラーゲンペプチド液に添加し、40℃〜90℃で一定時間攪拌することを特徴とするコラーゲンペプチドの製造方法とその製造方法により得られるコラーゲンペプチド及びコラーゲンペプチドの不快臭及び不快味の除去方法を提供する。なお、添加する除臭剤としては、活性白土、活性炭、アルミナ、シリカゲル、酸性白土、珪藻土の群から選択される1種又は2種以上を用いるのが好ましく、なかでも前記除臭剤である活性白土と活性炭との混合物を添加する場合には、活性白土と活性炭の比は3:1〜1:3の割合が適当である。
(もっと読む)
ウシ個体における枝肉重量及び体高を増加させる遺伝的能力を評価する遺伝子マーカー及びそれを用いた枝肉重量及び体高に関する遺伝的能力の評価方法
【課題】ウシ個体における枝肉重量、または、体高を増加させる遺伝的能力を評価する遺伝子マーカー、及び、そのマーカーを用いた評価方法を提供すること。
【解決手段】配列番号1の塩基配列から成るウシPTPDC1遺伝子のcDNAの964番目の塩基に対応する塩基、配列番号2の塩基配列から成るFGD3遺伝子のcDNAの47番目、556番目、または、557番目の塩基に対応する塩基、あるいは、配列番号3の塩基配列から成るウシSUSD3遺伝子のcDNAの53番目の塩基に対応する塩基を決定し、順に、G、C、T、G、Aである時に、そのウシ個体の枝肉重量、または、体高を増加させる遺伝的能力が、各塩基が野生型であるウシ個体より高いと評価し、枝肉の重量が重く、体高が高いと予測する。
(もっと読む)
金属抽出ペプチド(MAP)タグおよび関連する方法
【課題】画像化、研究、化学療法、およびキレーション療法(chelation therapy)等における種々の用途に有用な、選択的に金属に結合する能力を有する、短いペプチドモチーフおよびこのようなモチーフを使用するための方法を提供する。
【解決手段】特定の実施形態において、本発明は、新規なペプチドベースのタグもしくは金属の結合剤(MAPタグ)を提供する。上記MAPタグは、ポリペプチドもしくはタンパク質中に高親和性金属結合部位を直接コードするために使用され得る。本開示のMAPタグは、平面四角形および/もしくは四角錐の幾何的配置において金属に結合し得るそれらの能力によって特徴付けられる。
(もっと読む)
ペプチダーゼに対する耐性が向上しているGPL−1(グルカゴン様ペプチド−1)融合ペプチド
【課題】生物活性を有し、タンパク分解に対して耐性のあるペプチド分子に基づいたGLP−1を提供すること。
【解決手段】本発明は、GLP−1活性を有しており、インビボにおける安定性が向上している(特にジペプチジルペプチダーゼIVに対して耐性がある)融合ペプチドを提供する。前記融合ペプチドは、構成要素(I)として、N末端にGLP−1(7−35、7−36または7−37)の配列、および構成要素(II)として、C末端に少なくとも9アミノ酸のペプチド配列、またはその機能的な断片、変異体もしくは誘導体を含んでいる。構成要素(II)は、完全または部分的なIP2(介在性ペプチド2)であることが好ましい。好ましい実施の形態は、GLP−1(7−35、36または37)/IP2/GLP−1(7−35、36または37)またはGLP−2の配列を含んでいる。融合ペプチドは、組み換え細胞において、または合成的に生産されていてもよいし、様々な病気または疾患(例えば、1型糖尿病または2型糖尿病、アポトーシスが関連する病気、または、神経変性疾患など)を治療するための薬物を調製するために使用していてもよい。
(もっと読む)
TcおよびRe標識放射活性グリコシル化オクトレオチド誘導体
【課題】グリコシル化され、かつソマトスタチンレセプターに結合する新規放射活性オクトレオチド誘導体を提供すること。
【解決手段】核医学における診断および治療応用のための改良されたsst−レセプター結合ペプチド性リガンドを提供する。改良されたリガンドは、N−末端もしくはC−末端もしくはその両端に天然または非天然アミノ酸またはペプチド類似構造、炭水化物単位およびキレート化剤もしくは接合団を含有し、放射性同位体を結合または保持する放射性同位体の錯体形成物を提供する。該sst−またはSSTR−レセプター結合ペプチド性リガンドは、任意にペプチドにカップリング結合した1個以上の多機能リンカー単位、および/または糖部分および/またはキレート化剤および/または接合団を含有していてもよい。
(もっと読む)
1 - 20 / 9,138
[ Back to top ]