Fターム[4C204AB01]の内容
インドール系化合物 (20,061) | インドール系化合物の製造方法 (446) | 化合物の製造方法のみ (321)
Fターム[4C204AB01]の下位に属するFターム
インドール核合成 (84)
発酵による製造(酵素) (12)
ラセミ化方法 (2)
Fターム[4C204AB01]に分類される特許
81 - 100 / 223
カンナビノイド受容体リガンド
式I:
【化1】
(式中、R1、R2及びYは、明細書に定義された通りである)の化合物又はその薬学的に許容しうる塩(同様に明細書に定義された通りである)、及び化合物の製造を含む薬学的組成物。それらは、治療、特に疼痛管理に有用である。  (もっと読む)
(もっと読む)
バゼドキシフェンアセテートの結晶多形
【課題】結晶多形は、物質の同じ組成物が異なる格子配置で結晶化して、特定多形に特異的な異なる熱力学的特性及び安定性を生じさせる場合に起こる。より良好なバイオアベイラビリティー又はより良好な安定性を示すバゼドキシフェンアセテートの結晶多形の提供。
【解決手段】粉末X線回折データ、IRデータ及びDSCデータに従って特徴付けられるバゼドキシフェンアセテートの結晶多形(A形)およびそれを含有する組成物、その製造及びその使用。
(もっと読む)
新規なカルバゾール化合物、及びその重合体
【課題】溶解性に優れ、合成容易であって、電荷特性に優れる、新規なカルバゾール化合物および重合体を提供すること。
【解決手段】下記一般式(I)で示されるカルバゾール化合物である。

〔一般式(I)中、Ar1は、置換もしくは未置換の1価の芳香族基、又は複素環を含む芳香族基を表し、R1及びR2はそれぞれ独立に水素原子、アルキル基、置換もしくは未置換のアリール基、又は置換もしくは未置換のアラルキル基を表す。〕
(もっと読む)
オキシムエステル光重合開始剤
式(I)[式中、A1は、式(II)であり;A2は、式(III)であり;A3は、式(IV)であり;A4は、式(V)であり;w、x、yおよびzは、互いに独立して、0〜4の整数であり;ただし、x+y+zは、Qの結合価に対応して、2〜4の整数であることを条件とし;M1、M2、M3およびM4は、例えば、直接結合、COまたはOであり;Yは、例えば、直接結合またはSであり;Qは、(x+y)価の結合基であり;R1は、例えば、水素、C1〜C20アルキルまたはフェニルもしくはナフチルであり;R2およびR’’2は、例えば、水素またはC1〜C20アルキルであり;R3、R4、R’3、R’4、R’’3およびR’’4は、例えば、水素、ハロゲン、フェニルまたはC1〜C20アルキルであり;R24は、例えば直接結合である]の化合物は、光重合反応において予想外に良好な性能を発揮する。  (もっと読む)
(もっと読む)
π共役環状化合物およびその製造方法
【課題】新規なπ共役環状化合物の製造方法を提供すること。
【解決手段】イソインドール(1)から、イソインドールの1位置換体(2)を経て、π共役環状化合物(3)を製造する方法。 (もっと読む)
(もっと読む)
イソインドール類およびそのポリマー、並びにそれらの製造方法
【課題】イソインドール類を、簡便に得ることができる新規な製造方法を提供すること。
【解決手段】下記式(1)で示されるフタロニトリルを還元することを特徴とする、下記式(2)で示されるイソインドールの製造方法。 (もっと読む)
(もっと読む)
パーフルオロアルキル基を有する複素環化合物およびその製造方法
【課題】パーフルオロアルキル基を有する複素環化合物の製造方法を開発する。
【解決手段】
パーフルオロアルキル基を有する複素環化合物の製造方法は、
一般式(1)
[式中、Y1は、酸素原子等を示し、Y2、Y3、Y4およびY5は各々独立に、窒素原子、または、炭素数1から4のアルキル基等で置換されていても良い炭素原子を示す。]で表される複素環化合物を、一般式(2) R1aS(=O)R1b [式中、R1aおよびR1bは、炭素数1から12のアルキル基等を示す。]で表されるスルホキシド類、過酸化物、鉄化合物および酸の存在下に、一般式(3) Rf−X [式中、Rfは、炭素数1から6のパーフルオロアルキル基を示し、Xは、ハロゲン原子を示す。]で表されるハロゲン化パーフルオロアルキル類と反応させる。
(もっと読む)
O,O′,N,N′−テトラ(tert−ブトキシカルボニル)インジゴホワイト誘導体の製造方法
【課題】感圧記録体や感熱記録体用のロイコ染料として有用なO,O′,N,N′−テトラ(tert−ブトキシカルボニル)インジゴホワイト誘導体を、容易にかつ高収率で製造できる方法を提供することにある。
【解決手段】O,O′−ジ(tert−ブトキシカルボニル)インジゴホワイト誘導体と、二炭酸ジ−tert−ブチルエステルとを、塩基の存在下、有機溶媒中で反応させることを特徴とするO,O′,N,N′−テトラ(tert−ブトキシカルボニル)インジゴホワイト誘導体の製造方法。
(もっと読む)
カルバゾイルアルキル(メタ)アクリレートの製造方法
【課題】極めて高純度(好ましくは99重量%以上)なカルバゾイルアルキル(メタ)アクリレートを工業的な大量合成に適する方法で製造する方法を提供する。
【解決手段】本発明のカルバゾイルアルキル(メタ)アクリレートの製造方法は、N−(ヒドロキシアルキル)カルバゾールのエステル化反応によってカルバゾイルアルキル(メタ)アクリレートを製造する方法であって、該N−(ヒドロキシアルキル)カルバゾールは、晶析によって精製されたものである。
(もっと読む)
イミン化合物の製法
【課題】 回収再使用可能な触媒の存在下で、酸素を酸化剤として用いて、アミン化合物を酸化してイミン化合物を製造する方法を提供する。
【解決手段】 液相で、金のナノサイズクラスターをスチレン系高分子に担持させて成る酸化反応用高分子担持金クラスター触媒(特願2006-65982)の存在下で、アミン化合物を酸素又は空気雰囲気下で60〜180℃で加熱することにより、特定のイミン化合物を製造する。この高分子担持金クラスター触媒(特願2006-65982)は、金のナノサイズクラスターをスチレン系高分子に担持させて成り、該スチレン系高分子はスチレンモノマーをベースとし、その主鎖又はベンゼン環に架橋性官能基を有する親水性側鎖を有し、該架橋性官能基としてエポキシ基と水酸基を有する高分子であり、該スチレン系高分子のエポキシ基と水酸基とを架橋させて成る。
(もっと読む)
インドール化合物の製造方法
【課題】インドメタシンのような医薬品、または染料の骨格成分としても重要なインドール化合物を廉価、安全且つ効率よく製造する方法を提供すること。
【解決手段】インドリン化合物を、式(I)を満たす活性炭からなる触媒の存在下酸素と接触させるインドール化合物の製造方法。
4000<S×(Oco) (I)
但し、SはBET比表面積(m2/g)を、Ocoは加熱により一酸化炭素として脱離する表面酸素量の活性炭に対する重量%を示す。
(もっと読む)
5,5−二置換−3−ピロリン−2−オン誘導体の製造方法
【課題】合成中間体として有用な5,5−二置換−3−ピロリン−2−オン誘導体及びα,α−二置換−α−アミノ酸誘導体を簡便かつ経済的に製造する。
【解決手段】一般式(1)
(式中、Xはハロゲン原子を表し、R1及びR2は炭素数1〜8のアルキル基等を表し、R3及びR4は炭素数1〜8のアルキル基等を表す。)で示されるアクリル酸アミド誘導体を塩基と反応させ、5,5−二置換−3−ピロリン−2−オン誘導体を製造する。
(もっと読む)
縮合環化合物及びその製造方法
【課題】より簡単な方法で8員環以上の環を有する多環性の環状縮合化合物を製造すること、また、この製造方法により得られる多環性の環状縮合化合物を提供する。
【解決手段】下記の一般式(1A)で示される構造を有する縮合環化合物を提供する。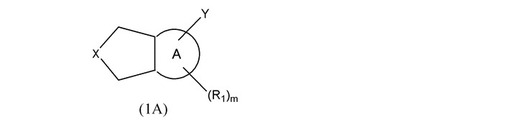
[式中、Xは炭素原子又はヘテロ原子含有基であり、Yは電子吸引基であり、R1はそれぞれ独立して水素、炭素数1〜20のアルキル基であり、環Aは8〜10員環であり、nは前記環Aが8員環である場合には0〜5の整数であり、前記環Aが9員環である場合には0〜6の整数であり、前記環Aが10員環である場合には0〜7の整数である。]
(もっと読む)
四置換ピロリジン類の製造法
【課題】短工程による四置換ピロリジン化合物類製造法の提供。
【解決手段】式(1)化合物と式(2)化合物とを付加反応させ式(3)化合物を生成させ、さらに置換基変換する式(3)で表される四置換ピロリジン類の製造法。

 (もっと読む)
(もっと読む)
5−アルキルオキシ−インドリン−2−オン誘導体、これらの調製およびV2バソプレシン受容体の選択的リガンドとしての治療におけるこれらの応用
本発明は、式(I)の化合物:
[式中、R0は、(C1−C4)アルキル、モノまたはポリフルオロ−(C1−C4)アルキル、シクロプロピルまたは−CH2−シクロプロピル、(C2−C4)アルケニルまたは(C2−C4)アルキニルであり;R1は、H、(C1−C5)アルキル、モノまたはポリフルオロ−(C1−C5)アルキル、ヒドロキシ−(C2−C5)アルキル、−(CH2)m−(C3−C5)シクロアルキルであり;Z1は、Hまたはハロゲン、(C1−C4)アルキル、モノまたはポリフルオロ−(C1−C4)アルキル、(C1−C4)アルコキシ、モノまたはポリフルオロ−(poIy[IuOrO−)(C1−C4)アルコキシ、場合によって置換されたシクロプロピルまたは−CH2−シクロプロピルであり;Z2は、ハロゲン原子またはT1W基を表し、T1は−(CH2)n−基であり、Wは、H、(C1−C4)アルキル、モノもしくはポリフルオロ−(C1−C4)アルキルまたは場合により置換されたシクロプロピルの1つまたは複数であり、またはWは−C(O)OR19であり、またはWは−C(O)NR6R7であり、またはWは−NR8C(O)R9基であり、またはWは−NR10R11であり、またはWは−OR12基であり;R4は、(C1−C4)アルキル、モノまたはポリフルオロ−(C1−C4)アルキル、OH、(C1−C4)アルコキシ、(C2−C4)アルケニル、ニトロ、COORCl、ベンジルオキシであり、またはR4は−C(O)NR13R14であり、またはR4は−NR15R16であり、またはR4は−NR17C(O)R18であり;R3およびR5は、Hまたは、ハロゲン、(C1−C4)アルキル、モノもしくはポリフルオロ−(C1−C4)アルキル、(C1−C4)アルコキシまたはモノもしくはポリフルオロ−(C1−C4)アルコキシであり;m=0、1または2;n=0または1]に関し、前記化合物は、シス/トランス異性体、またはこれらの混合物の形態の、これらの塩基、水和物、溶媒和状態である。本発明は、さらに、式(I)の化合物の調製方法および治療におけるそれらの使用にも関する。  (もっと読む)
(もっと読む)
四置換ピロリジン化合物の製造方法
【課題】選択的なエポキシ環開裂反応を用いることにより、毒性のある青酸を使用することなく、かつ短工程で四置換ピロリジン化合物の製造方法およびその製造中間体の提供。
【解決手段】特定の工程に従って、式(6)で示される化合物を製造する。
(式中、R1は、水素原子またはアミノ基の保護基を示し;R2は、置換基を有していてもよい炭素数1から6のアルキル基または置換基を有していてもよい炭素数6から10のアリール基を示し;nは、2から5の整数を示す。)
(もっと読む)
(1R,2S,5S)−N−[(1S)−3−アミノ−1−(シクロブチルメチル)−2,3−ジオキソプロピル]−3−[(2S)−2−[[[(1,1−ジメチルエチル)アミノ]カルボニル]−アミノ]−3,3−ジメチル−1−オキソブチル]−6,6−ジメチル−3−アザビシクロ[3.1.0]ヘキサン−2−カルボキサミドを調製するための方法
本発明は、スキーム(II)の方法を使用して、式(I)の化合物である(1R,2S,5S)−N−[(1S)−3−アミノ−1−(シクロブチルメチル)−2,3−ジオキソプロピル]−3−[(2S)−2−[[[(1,1−ジメチルエチル)アミノ]カルボニル]−アミノ]−3,3−ジメチル−1−オキソブチル]−6,6−ジメチル−3−アザビシクロ[3.1.0]ヘキサン−2−カルボキサミドを調製するための方法、および調製するのに有用な中間化合物を調製するための方法にも関する。
 (もっと読む)
(もっと読む)
パラジウム担持セピオライト触媒およびβ−アミノ酸類の製造方法
【課題】工業的に重要なβ−アミノ酸類の簡便で経済的で生産性の良い製造方法を提供する。
【解決手段】アミン類とアクリル酸エステル類とを反応させて、一般式(3)で表されるβ−アミノ酸類を製造する際に、パラジウム担持セピオライトから成るβ−アミノ酸類製造用触媒を用いる。
(式中、R1およびR2はそれぞれ独立して水素原子、炭素数が1から10のアルキル基または置換されていても良いフェニル基を示す。あるいは、R1とR2が結合する窒素原子と共に置換されていても良い環を形成していても良い。ただしR1とR2が同時に水素原子ではない。R3は炭素数1から10のアルキル基を示し、R4は水素原子または置換されていても良い炭素数1から4のアルキル基を示す。)
(もっと読む)
肝カルニチンパルミトイルトランスフェラーゼ(L−CPTI)としてのスルホンアミド誘導体
本発明は、式(I)[式中、R1、R2、R3、X及びYは、明細書及び請求項に定義された通りである]の新規なスルホンアミド誘導体、ならびにその生理学的に許容しうる塩及びエステルに関する。これらの化合物は、L−CPT1を阻害し、医薬として使用することができる。  (もっと読む)
(もっと読む)
4−メチルチオ−3−ブテニルイソチオシアナートの製造方法、その合成中間体、及びこれを含有する抗菌剤組成物
【課題】抗菌活性を有する4−メチルチオ−3−ブテニルイソチオシアナートのトランス体を優勢に合成すること。
【解決手段】まず、1−ハロゲノ−4−メチルチオブタン(化合物(VII))のメチルチオ基が結合した炭素原子上に、炭素原子−ハロゲン原子結合を生成させて、1,4−ジハロゲノ−1−メチルチオブタン(化合物(VI))を生成させ、この物質からハロゲン化水素(HX2)を脱離させることで、不飽和中間体である4−ハロゲノ−1−メチルチオ−1−ブテン(化合物(V))を生成させ、該不飽和中間体のハロゲン(X1)が結合する炭素原子において、炭素原子−窒素原子結合を生成させた後、脱保護することでアミン化合物(化合物(II))を得て、続いて、該アミン化合物をイソチオシアナート化することで、目的生成物である4−メチルチオ−3−ブテニルイソチオシアナート(化合物(I))のトランス体を優勢に合成する。
(もっと読む)
81 - 100 / 223
[ Back to top ]


